Clear Sky Science · de
Vergleichende Analyse von Deep-Mutational-Scanning-Datensätzen bei Enteroviren A und B identifiziert funktionelle Divergenz und therapeutische Zielstrukturen
Warum winzige RNA‑Viren für uns wichtig sind
Enteroviren sind eine große Gruppe winziger RNA‑Viren, die weltweit zirkulieren und meist nur leichte Erkältungen oder Magen-Darm-Beschwerden verursachen, aber gelegentlich Lähmungen, Herzzellschäden oder andere schwere Erkrankungen auslösen. Es gibt nur wenige Impfstoffe und noch weniger breit wirksame Medikamente gegen sie, zum Teil weil diese Viren sehr schnell evolvieren. Diese Studie stellt eine scheinbar einfache, aber praktisch bedeutsame Frage: Wenn diese Viren mutieren, welche Teile ihrer Maschinerie können sich frei verändern, und welche sind so essenziell, dass die Evolution sie nahezu unverändert hält? Die Antworten weisen auf neue Strategien zur Entwicklung von Therapien hin, denen das Virus nur schwer ausweichen kann.
Das virale Regelwerk lesen, Mutation für Mutation
Die Forschenden konzentrierten sich auf zwei humane Enteroviren mit sehr unterschiedlichen Krankheitsbildern: Enterovirus A71, das mit schweren neurologischen Erkrankungen bei Kindern verknüpft ist, und Coxsackievirus B3, das mit Herzentzündungen und sogar Bauchspeicheldrüsenkrebs assoziiert wird. Mit einer Methode namens Deep Mutational Scanning erzeugten sie Virusbibliotheken, in denen nahezu jede Position in den viralen Proteinen systematisch verändert wurde. Diese Mutanten durften Zellen in Kultur infizieren, und mittels Hochdurchsatzsequenzierung wurde gemessen, wie sich jede Veränderung auf das Virenwachstum auswirkte. Durch den Vergleich jedes Mutanten mit dem Ursprungsvirus erstellte das Team eine detaillierte Karte der Stellen im viralen Proteom, die Veränderungen tolerieren, und derjenigen, die stark eingeschränkt sind. 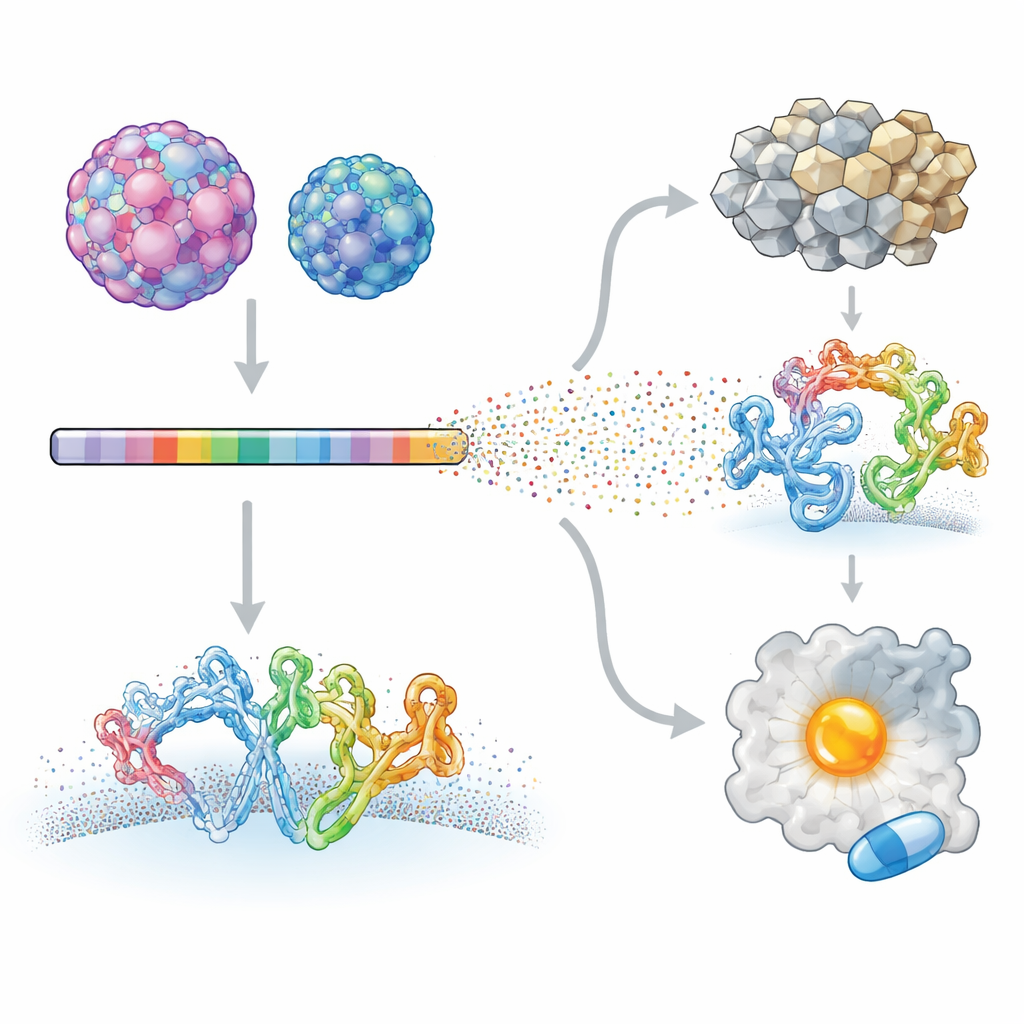
Geteilte harte Grenzen und virus-spezifische Flexibilität
Trotz eines gemeinsamen Aminosäureanteils von nur etwa der Hälfte zeigten die beiden Viren bemerkenswert ähnliche Gesamtmuster der Einschränkung. Die internen enzymatischen ‚Arbeitstiere‘, die das Genom kopieren, virale Proteine schneiden und RNA aufwinden, reagierten in beiden Viren sehr empfindlich auf Mutationen. Ebenso erwiesen sich versteckte Oberflächen, die die Proteinhülle oder Kapside zusammenhalten, als schwer veränderbar, ohne das Virus zu beschädigen. Im Gegensatz dazu waren viele außenliegende und mit dem Wirt interagierende Regionen freier in ihrer Variabilität und unterschieden sich häufig deutlich zwischen den beiden Spezies. Strukturelle Analysen zeigten, dass konservierte, mutationstolerante Regionen um aktive Zentren und Assemblierungsoberflächen gruppiert sind, während Regionen, die mit Wirtsrezeptoren, Membranen oder Immunmolekülen in Kontakt stehen, Hotspots artspezifischer Flexibilität darstellen.
Wie Viren Zellen erreichen und Abwehrmechanismen umgehen
Das Team zoomte anschließend in den molekularen Händedruck zwischen Virus und Wirt. Enterovirus A71 und Coxsackievirus B3 nutzen unterschiedliche zelluläre Rezeptoren zur Zellaufnahme, und die Studie fand, dass die genauen Kontaktflächen auf der Kapsidoberfläche zu den am stärksten divergierenden Regionen in Bezug auf Mutationstoleranz gehören. Reste, die bei einem Virus den Rezeptor erfassen, sind in diesem Virus stark eingeschränkt, aber im anderen relativ permissiv — ein Ausdruck dafür, wie jedes Virus seine Andockplattform fein abgestimmt hat. Ähnliche Divergenz zeigte sich in einem kleinen membrangebundenen Protein namens 3A, das hilft, Zellmembranen umzubauen und Wirtsfaktoren für die Genomreplikation zu rekrutieren. Modellierungen deuteten darauf hin, dass die beiden Viren teilweise unterschiedliche Kontaktflächen auf 3A nutzen, um denselben Wirtsfaktor GBF1 zu binden, und dieses Protein möglicherweise in unterschiedlicher Tiefe in Membranen einfügen. Diese Unterschiede helfen zu erklären, warum eng verwandte Viren verschiedene Gewebe infizieren und unterschiedliche Krankheitsbilder hervorrufen können.
Was Labor‑Evolution verpasst — und was sie richtig abbildet
Um ihre Zellkultur‑Experimente in den realen Kontext einzuordnen, verglichen die Autorinnen und Autoren ihre Mutationskarten mit tausenden natürlichen Virussequenzen aus Proben von Patientinnen und Patienten. Insgesamt zeigten Stellen, die im Labor flexibel waren, auch in der Natur tendenziell Variation, besonders in breiteren vergleichenden Analysen auf Art‑Ebene. Untersuchte man jedoch, welche spezifischen Aminosäuren an jeder Stelle bevorzugt werden, stimmten natürliche Evolution und Laborauswahl am engsten innerhalb eines einzelnen Virustyps überein. Auffällig waren die größten Diskrepanzen an der äußeren Kapsidoberfläche und an wirtsinteragierenden Regionen der nicht-strukturellen Proteine 2A und 3A — genau dort, wo Immunantworten und komplexe Wirtsumgebungen am stärksten ins Gewicht fallen. Das deutet darauf hin, dass Deep Mutational Scanning die grundlegenden mechanischen Einschränkungen viraler Proteine erfasst, während reale Infektionen zusätzliche Selektionsdrücke durch Immunität und Gewebetropismus überlagern, die in vitro schwerer nachzubilden sind.
Eine gemeinsame Schwachstelle für zukünftige Medikamente finden
Schließlich fragten die Forschenden, ob diese Karten eine gemeinsame Achillesferse für die Wirkstoffentwicklung aufzeigen könnten. Mit computergestützten Werkzeugen suchten sie in beiden Viren nach Taschen auf Proteinoberflächen, die prinzipiell kleine Molekülwirkstoffe binden könnten. Anschließend überlagerten sie die Mutationsdaten, um zu erkennen, welche Taschen aus Resten bestehen, die das Virus nicht leicht verändern kann, ohne seine Fitness zu beeinträchtigen. Eine Tasche, gelegen an der 2C‑Helikase — einem ringförmigen Motor, der beim Aufwinden der viralen RNA hilft — stach hervor. Ihre Form und die konstituierenden Reste sind über vier wichtige humane Enterovirus‑Spezies hinweg hoch konserviert, sie liegt abseits bereits bekannter aktiver Zentren, und Veränderungen dort sind sowohl in natürlichen Sequenzen selten als auch in Labortests stark nachteilig. 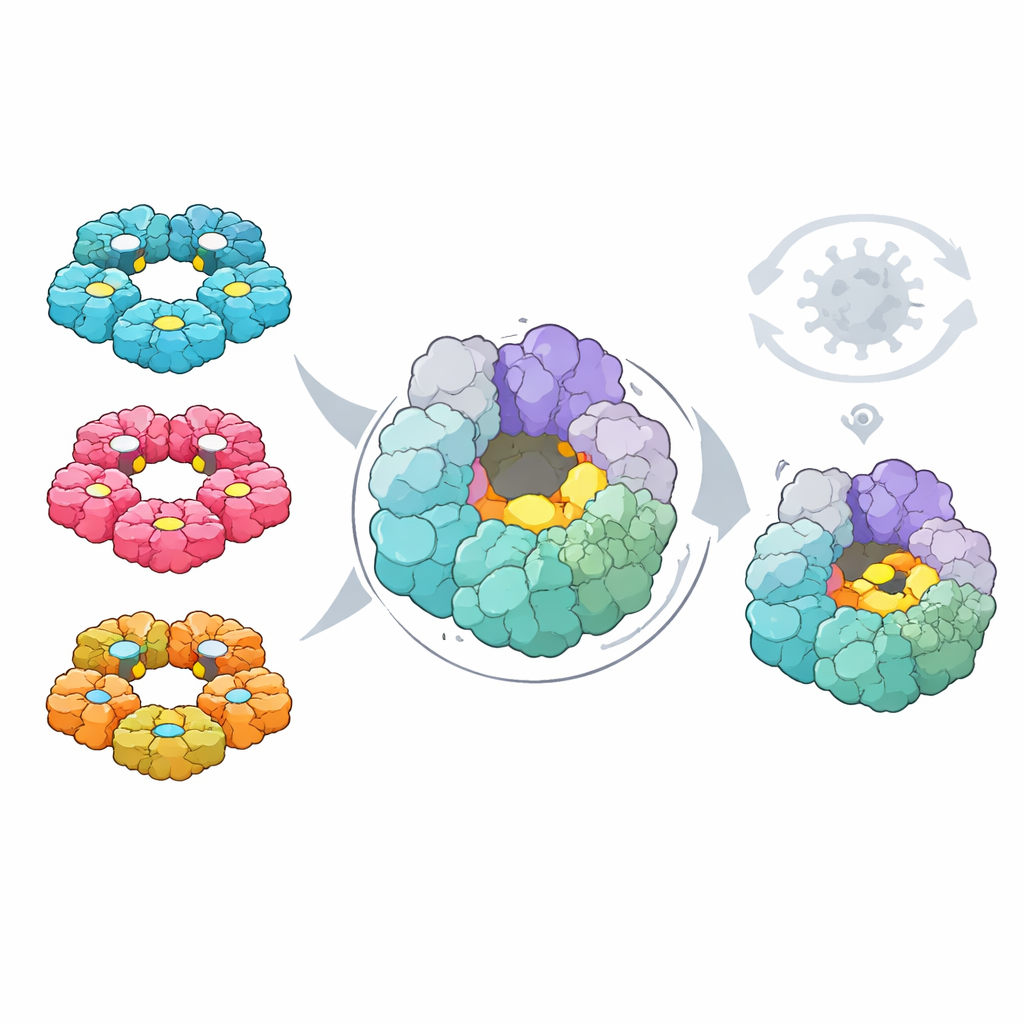
Was das für zukünftige Behandlungen bedeutet
Indem die Studie systematisch untersucht, wie jede mögliche Einzelbuchstabenänderung zwei wichtige Enteroviren beeinflusst, offenbart sie eine klare Trennung zwischen einem gemeinsamen, starren Kern der viralen Maschinerie und flexibleren, virus‑spezifischen Schnittstellen mit dem Wirt. Der konservierte Kern umfasst eine neu hervorgehobene Tasche an der 2C‑Helikase, die für das Virus offenbar nur schwer zu mutieren ist, ohne die Fitness zu opfern — damit ein attraktives Ziel für Breitband‑Antiviralia mit hoher Resistenzbarriere. Gleichzeitig erklären die anpassungsfähigeren äußeren Oberflächen und Wirtskontaktstellen, warum verwandte Viren sich im Körper so unterschiedlich verhalten, und zeigen, wo Impfstoffe und immunbasierte Therapien mit schneller Evolution rechnen müssen. Zusammen liefern diese Ergebnisse eine Landkarte für die Entwicklung von Behandlungen, die die evolutionären Grenzen des Virus gezielt ausnutzen.
Zitation: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Schlüsselwörter: Enteroviren, virale Evolution, Deep Mutational Scanning, antivirale Ziele, 2C-Helikase