Clear Sky Science · de
Native H2 pathways enable biocompatible hydrogenation of metabolic alkenes in bacteria
Bakterien zu winzigen grünen Fabriken machen
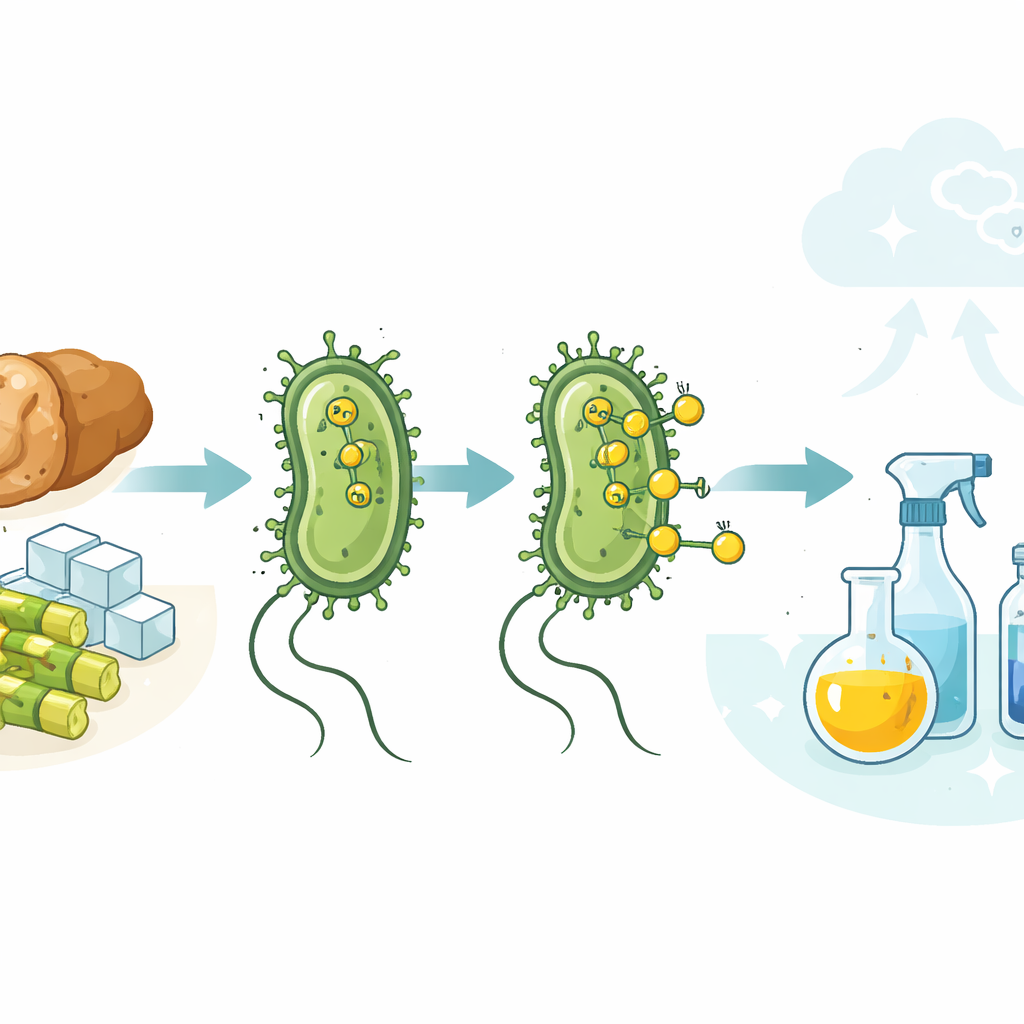
Stellen Sie sich vor, gewöhnliche Darmbakterien könnten helfen, fossile Brennstoffe bei der Herstellung alltäglicher Chemikalien zu ersetzen – von Konservierungsmitteln bis zu Kunststoffen – und dabei sogar Lebensmittelabfälle verwerten. Diese Studie zeigt, dass unauffällige Laborstämme von Escherichia coli genau das können: Sie erzeugen auf natürliche Weise Wasserstoffgas in ihren Zellen, und dieser Wasserstoff lässt sich an der Zelloberfläche nutzen, um chemische Reaktionen unter schonenden, wässrigen Bedingungen anzutreiben. Durch die Kombination lebender Mikroben mit einem festen Metallkatalysator beschreiben die Forschenden einen Weg zu saubereren, klimaschonenderen Produktionsprozessen.
Warum Wasserstoff für Alltagsprodukte wichtig ist
Wasserstoff steht im Zentrum moderner Chemie. Er wird eingesetzt, um flüssige Öle zu Streichfetten umzuwandeln, Rohöle zu veredeln und viele Inhaltsstoffe für Arzneimittel und Kunststoffe herzustellen. Heute stammt nahezu all dieser Wasserstoff aus fossilen Quellen, vor allem Erdgas und Kohle, was große Mengen Kohlendioxid freisetzt. Gleichzeitig geben viele Mikroben beim Abbau von Zucker unter Sauerstoffmangel natürlich Wasserstoff ab. Die Herausforderung, die die Autorinnen und Autoren angehen, besteht darin, diesen milden, biologischen Wasserstoffstrom so zu nutzen, dass er die gleichen Reaktionen antreibt, die die Industrie derzeit mit hohem Druck, organischen Lösungsmitteln und fossilem Gas durchführt.
Bakterien einen Metallkatalysator antreiben lassen
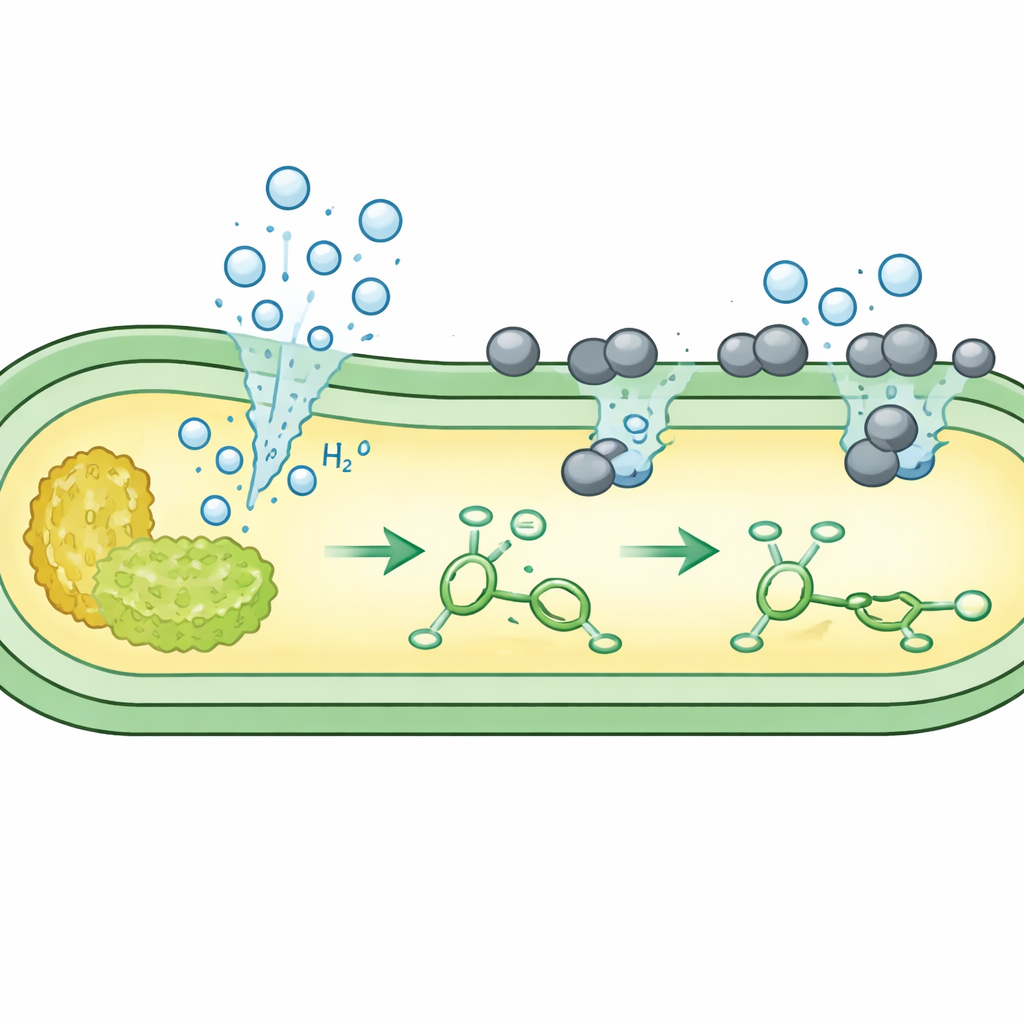
Das Team konzentrierte sich auf einfache Hydrierungsreaktionen, bei denen eine Doppelbindung in einem Molekül durch Wasserstoff „gesättigt“ wird. Sie kultivierten mehrere unveränderte E. coli‑Stämme in zuckerbasierten Medien und fügten dann einen fein verteilten Palladiumkatalysator hinzu, der zellverträglich ist. Unter sauerstofffreien Bedingungen wandelte der native Stoffwechsel der Bakterien Zucker in Formiat und dann an der inneren Membranseite in Wasserstoffgas um. Mikroskopische Aufnahmen zeigten, dass die positiv geladenen Katalysatorpartikel sich an der negativ geladenen Zelloberfläche anlagern, wo sie auf den entweichenden Wasserstoff treffen. Dort nutzt das Metall den mikrobiellen Wasserstoff, um ein Testmolekül, Kaffeesäure, zu seinem gesättigten Produkt zu reduzieren – mit sehr hohen Ausbeuten, die oft besser waren als bei einem zuvor stark gentechnisch veränderten Stamm.
Erweiterung der Produkt- und Rohstoffpalette
Sobald die Grundreaktion funktionierte, testeten die Forschenden eine breite Palette von Molekülen mit Kohlenstoff‑Kohlenstoff‑Doppelbindungen, darunter pflanzenbasierte Säuren und langkettige Fettsäureverbindungen. Viele wurden glatt in ihre gesättigten Formen überführt, einige nahezu in quantitativen Ausbeuten. Außerdem konstruierten sie E. coli‑Stämme, die durch Umlenkung von mehr Stoffwechselfluss in den nativen wasserstoffbildenden Pfad zusätzlichen Wasserstoff produzieren. Diese verstärkten Stämme ermöglichten ähnliche Umsetzungen mit weniger Metallkatalysator. In einer bemerkenswerten Wendung ersetzten die Forschenden reinen Zucker durch verflüssigtes Altbrot als Nahrungsquelle. Enzyme bauten das alte Brot zu Glukose ab, die die Bakterien ebenso effektiv vergoren – so wurde ein gewöhnlicher Lebensmittelabfall in biologischen Wasserstoff und wertvolle Chemikalien verwandelt.
Sowohl Ausgangsstoff als auch Treibstoff in einer Zelle herstellen
Als Nächstes fragten die Autorinnen und Autoren, ob eine einzelne Bakterienzelle nicht nur das Wasserstoff‑„Reagenz“, sondern auch das ungesättigte „Substrat“ herstellen könnte, das verändert werden soll. Sie konstruierten E. coli so, dass Zucker zuerst in Wege fließt, die aromatische Bausteine wie Zimtsäure und Kumarsäure produzieren, sowie in einen separaten Pfad, der Wasserstoff erzeugt. Nachdem die Kultur diese internen Metaboliten aufgebaut hatte, fügten sie den Palladiumkatalysator hinzu. An der Zelloberfläche nutzte der Katalysator den in situ erzeugten Wasserstoff, um die neu gebildeten doppelt gebundenen Metaboliten in vollständig gesättigte Produkte zu überführen, etwa Hydrocinnaminsäure, Desaminotyrosin und Adipinsäure, einen wichtigen Vorläufer für Nylon. In einigen Varianten erreichte dieses Kometabolisieren beinahe vollständige Umsetzungen, alles innerhalb derselben lebenden Kultur.
Den Klimaeffekt messen
Um zu prüfen, ob diese clevere Biochemie tatsächlich dem Klima nützt, führten die Forschenden eine Lebenszyklusanalyse durch und verglichen ihren hybriden „chemo‑mikrobiellen“ Ansatz mit herkömmlichen Hydrierungswegen, die durch fossilen oder elektrolytisch erzeugten Wasserstoff angetrieben werden. Wenn biologischer Wasserstoff und die in‑zell Produktion der Substrate in einem einzigen, wärmeeffizienten Prozess kombiniert wurden, sanken die Gesamtemissionen von Treibhausgasen deutlich. Die Verwendung von Altbrot als Rohstoff steigerte den Effekt: Durch das Vermeiden von Deponie oder Verbrennung und die Umwandlung weggeworfener Lebensmittel in Chemikalien wurden einige Szenarien insgesamt kohlenstoffnegativ, das heißt sie entziehen mehr Treibhausgase aus der Atmosphäre, als sie ausstoßen.
Was das für die zukünftige Produktion bedeutet
Einfach ausgedrückt zeigt die Studie, dass alltägliche Bakterien dazu gebracht werden können, zugleich Energiequelle und Produktionsfabrik für wichtige chemische Reaktionen zu sein, während ein festes Metall an ihrer Oberfläche die Aufgabe vollendet. Da alles in Wasser, bei nahe Körpertemperatur und mit erneuerbaren oder Abfallzuckern stattfindet, könnte dieser Ansatz eines Tages sauberere Alternativen zu traditionellen petrochemischen Anlagen bieten. Mit weiterer Optimierung der mikrobiellen Stoffwechselwege und Katalysatoren könnte diese lebende Zellplattform eine neue Generation nachhaltiger Prozesse ermöglichen, die erneuerbaren Kohlenstoff und weggeworfene Lebensmittel in nützliche Produkte mit deutlich kleinerer Klimabilanz verwandeln.
Zitation: White, M.F.M., Trotter, C.L., Steele, J.F.C. et al. Native H2 pathways enable biocompatible hydrogenation of metabolic alkenes in bacteria. Nat. Chem. 18, 535–543 (2026). https://doi.org/10.1038/s41557-025-02052-y
Schlüsselwörter: mikrobieller Wasserstoff, grüne Chemie, Biokatalyse, Abfall-zu-Chemikalien, nachhaltige Produktion