Clear Sky Science · de
Monovalente pseudo-natürliche Wirkstoffe verstärken den Abbau von IDO1 durch das native E3 KLHDC3
Ein krebsförderndes Enzym ausschalten
Unser Immunsystem patrouilliert ständig nach Krebszellen, doch Tumoren wehren sich oft, indem sie die Chemie des Körpers zu ihren Gunsten nutzen. Ein Schlüsselfaktor in diesem Tauziehen ist das Enzym IDO1, das Tumoren hilft, Immunzellen zu neutralisieren. Diese Studie beschreibt eine neue Klasse kleinmolekularer Verbindungen, die mehr leisten als nur die Aktivität von IDO1 zu blockieren — sie veranlassen die Zellen, das Enzym vollständig zu entsorgen. Indem sie die natürliche Müllentsorgungsmaschinerie der Zelle nutzen, könnten diese Verbindungen Immunangriffe auf Tumoren wiederbeleben, auf eine Weise, die älteren Wirkstoffen verwehrt blieb.
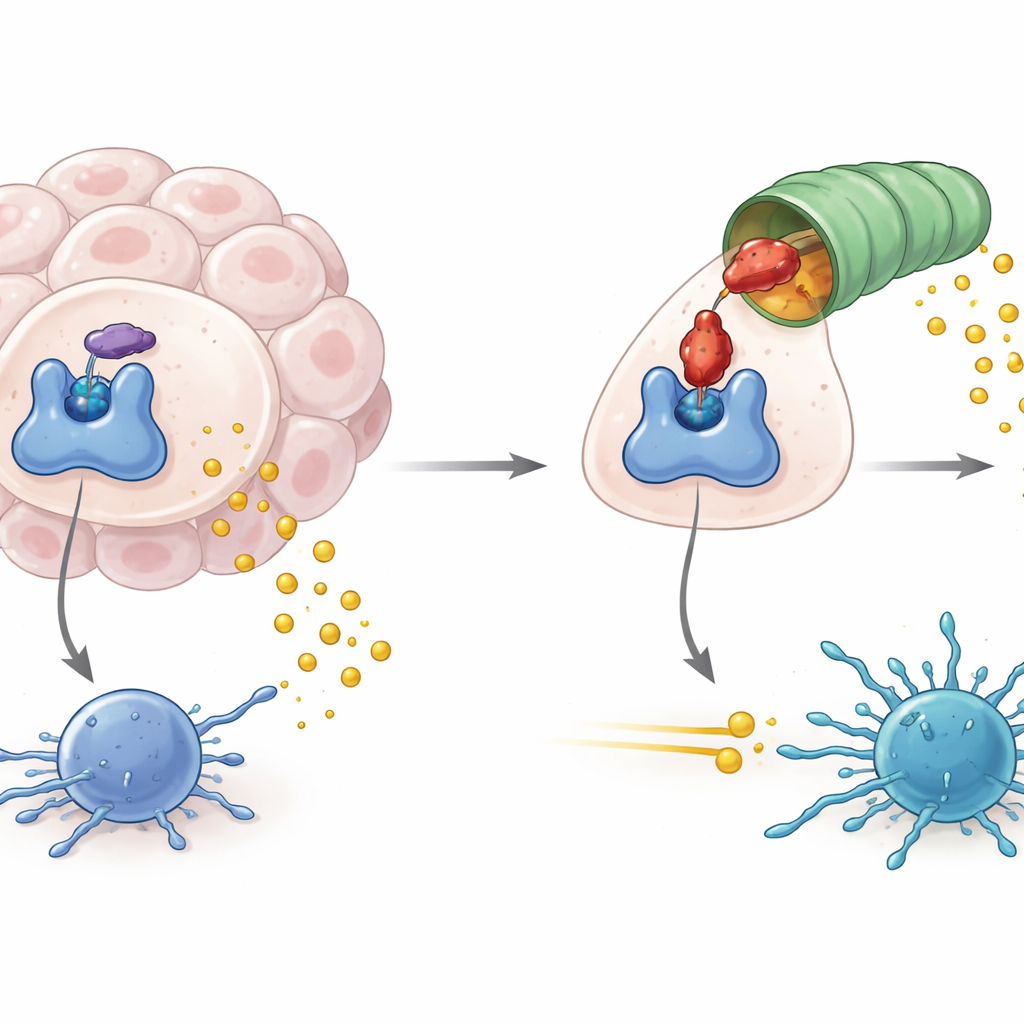
Wie Tumoren einen metabolischen Wächter ausnutzen
IDO1 sitzt am Eingang einer Stoffwechselbahn, die die Aminosäure Tryptophan in ein Produkt namens Kynurenin umwandelt. Wenn IDO1 reichlich vorhanden und aktiv ist, sinkt der Tryptophanspiegel und Kynurenin steigt an, wodurch ein chemisches Milieu entsteht, das die Aktivität von Immunzellen, einschließlich tumorbekämpfender T‑Zellen, dämpft. Hohe IDO1‑Aktivität wurde nicht nur mit schwächerer Anti‑Tumor‑Immunität, sondern auch mit virusbedingten Lymphomen und einigen Formen der Neurodegeneration in Verbindung gebracht. Arzneimittelentwickler haben sich daher darauf konzentriert, die Enzymaktivität von IDO1 zu blockieren, in der Hoffnung, dieses immunsuppressive Signal abzuschneiden und bestehende Krebsimmuntherapien wirksamer zu machen.
Warum einfache Enzymhemmer versagt haben
Trotz vielversprechender Ergebnisse in Tiermodellen waren klinische Studien mit traditionellen IDO1‑Inhibitoren enttäuschend. Eine mögliche Erklärung ist, dass IDO1 mehr ist als ein einfacher Katalysator. Selbst wenn seine chemische Aktivität blockiert ist, kann das Protein selbst als Signalknoten fungieren, der weiterhin Tumorwachstum und -ausbreitung fördert. Manche Inhibitoren stabilisieren IDO1 sogar und erhöhen so die Menge des Proteins in Zellen. Mit anderen Worten: Das bloße Abschalten der katalytischen Funktion lässt seine pro‑tumoralen, nicht‑enzymatischen Rollen unangetastet — oder stärkt sie im schlimmsten Fall sogar.
Verbindungen entwerfen, die Selbstzerstörung auslösen
Die Autoren durchsuchten eine große Bibliothek „pseudo‑natürlicher“ Moleküle — synthetische Verbindungen, aufgebaut aus Fragmenten, die von Naturstoffen inspiriert, aber neu kombiniert sind. Sie identifizierten eine Molekülfamilie, genannt iDegs, abgeleitet von einem pflanzenähnlichen Baustein namens (−)-Myrtanol. Diese Verbindungen binden in die übliche Bindetasche von IDO1 für seinen eisenhaltigen Kofaktor Häm. Indem sie Häm verdrängen, schwächen iDegs sowohl die Fähigkeit von IDO1, Kynurenin zu produzieren, als auch — entscheidend — sie verändern einen Teil der C‑terminalen Helix des Proteins. Hochaufgelöste Kristallstrukturen zeigen, dass iDegs im Häm‑Bindungsort eine Lockerung und partielle Entordnung einer C‑terminalen Helix bewirken, die normalerweise in einer kompakten, geschützten Konformation gehalten wird.
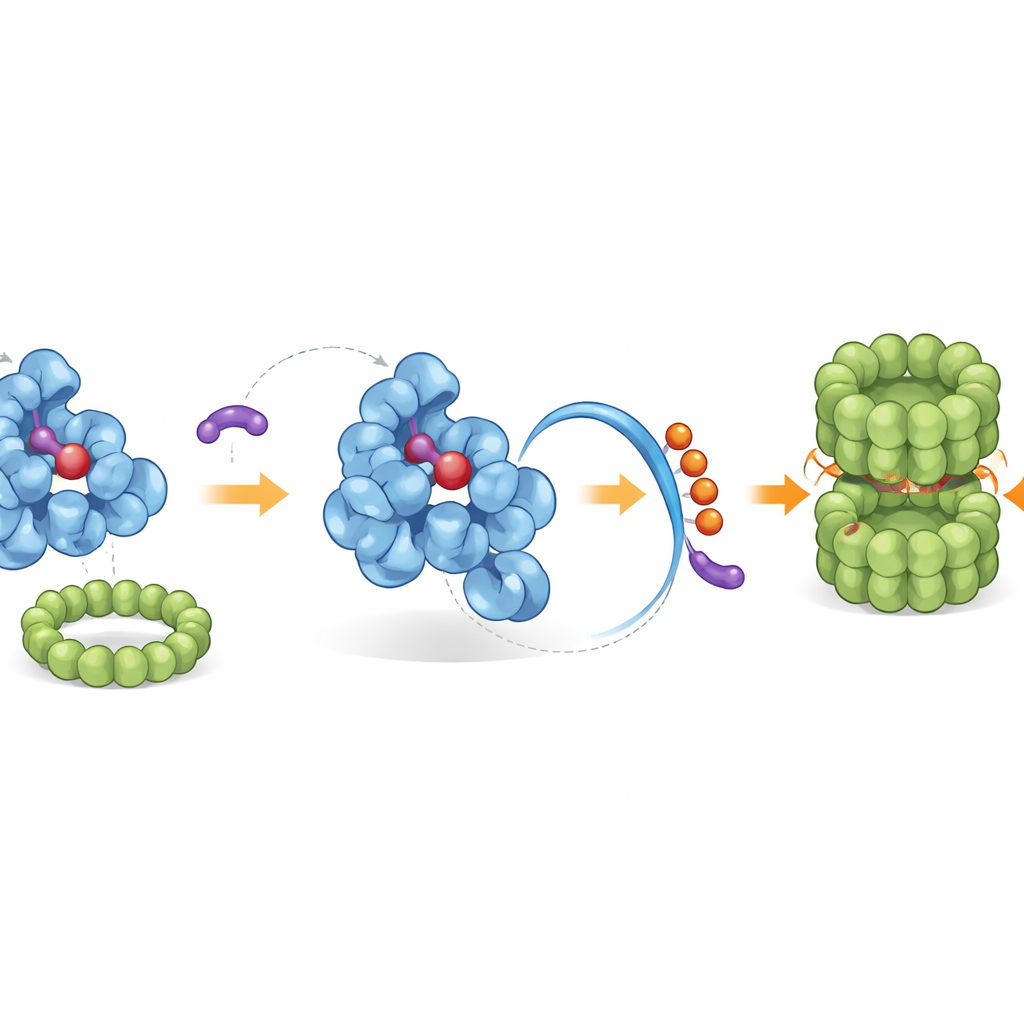
Die native Aufräumcrew der Zelle rekrutieren
Der umgestaltete Schwanz legt ein eingebautes „Endetikett“ frei, das die Müllentsorgungsmaschinerie der Zelle erkennt. Mithilfe genetischer Screens und biochemischer Rekonstruktion identifizierten die Forscher einen spezifischen Ligasekomplex, genannt CRL2–KLHDC3, der natürlicherweise kleine Ubiquitin‑„Marken“ an den freigelegten Schwanz von IDO1 anheftet und es so für den Proteasom‑vermittelten Abbau kennzeichnet — den molekularen Shredder der Zelle. Unter normalen Bedingungen wird nur die hämfreie Form von IDO1 effizient auf diese Weise markiert, während die hämgebundene Form geschützt ist. iDegs verschieben dieses Gleichgewicht, indem sie ausschließlich an die hämfreie Form binden und den natürlichen Abbauweg verstärken. Potente Vertreter der Serie blockieren nicht nur die Kynureninproduktion, sondern erhöhen auch die Ubiquitin‑Markierung von IDO1 und reduzieren dessen Proteinspiegel in mehreren Krebszelltypen deutlich.
Das Schicksal von IDO1 — und die Immunantworten — ändern
Dieses Doppelwirkungsprinzip hat wichtige funktionelle Folgen. In Migrationsassays mit Ovarialkarzinomzellen beschleunigte ein klinisch untersuchter IDO1‑Inhibitor, der das Enzym stabilisiert, tatsächlich die Zellbewegung, was zu IDO1s nicht‑enzymatischer, pro‑tumoraler Rolle passt. Im Gegensatz dazu verlangsamte ein iDeg‑Verbindung die Migration, was sowohl mit enzymatischer Hemmung als auch mit Verlust des Proteins vereinbar ist. Die Studie eröffnet somit einen neuen Weg, IDO1 zu beeinflussen: nicht durch das gewaltsame Heranziehen zu einer fremden Ligase mit einem sperrigen Designer‑Molekül, sondern durch das „Aufladen“ eines bereits in Zellen vorhandenen nativen Abbauwegs.
Was das für zukünftige Krebstherapien bedeuten könnte
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass die Qualität — nicht nur die Quantität — der Enzymhemmung zählt. Diese neuen kleinmolekularen Wirkstoffe wirken wie präzise Schalter: Sie sperren IDO1 in eine verwundbare Form, die die Zelle bereits zum Abbau vorgesehen hat, und unterbinden damit sowohl dessen metabolische als auch seine signalgebenden Beiträge zum Tumorüberleben. Da iDegs kompakt, arzneimittelähnlich und auf die körpereigene Ligase für die Entfernung von IDO1 angewiesen sind, könnten sie einen subtileren und weiter anwendbaren Ansatz bieten als frühere „Protein‑Degrader“-Medikamente. Wenn ähnliche Strategien auf andere problematische Proteine anwendbar sind, deutet diese Arbeit auf eine neue Generation von Therapien hin, die kranke Zellen dazu bringen, ihre eigenen molekularen Waffen zu demontieren.
Zitation: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Schlüsselwörter: IDO1, Krebsimmuntherapie, gerichteter Proteinabbau, Ubiquitin-Ligase, kleinmolekulare Degrader