Clear Sky Science · de
Biokompatible Liganden‑Balance in Übergangsmetall‑Koordination ermöglicht harmlose in‑zell Protein‑Arylierung
Metalle als schonende Werkzeuge für Zellen
Viele leistungsfähige chemische Reaktionen beruhen auf Metallen, doch bringt man dieselben Metalle in die Nähe lebender Zellen, entstehen meist Probleme: Schäden, Stress und Zelltod. Diese Studie zeigt, dass es mit dem richtigen molekularen "Griff" um ein Nickelatom möglich ist, eine anspruchsvolle Reaktion innerhalb lebender Zellen durchzuführen, ohne sie zu schädigen. Dieser Durchbruch erlaubt es Forschern, tausende spezifische Stellen in Proteinen zu markieren und sogar das Auftauchen schwer nachzuverfolgender Erreger zu verfolgen — und eröffnet damit neue Wege, abzubilden, was in Zellen bei Gesundheit und Krankheit wirklich vor sich geht.
Warum Metalle sowohl Helfer als auch Gefahr sind
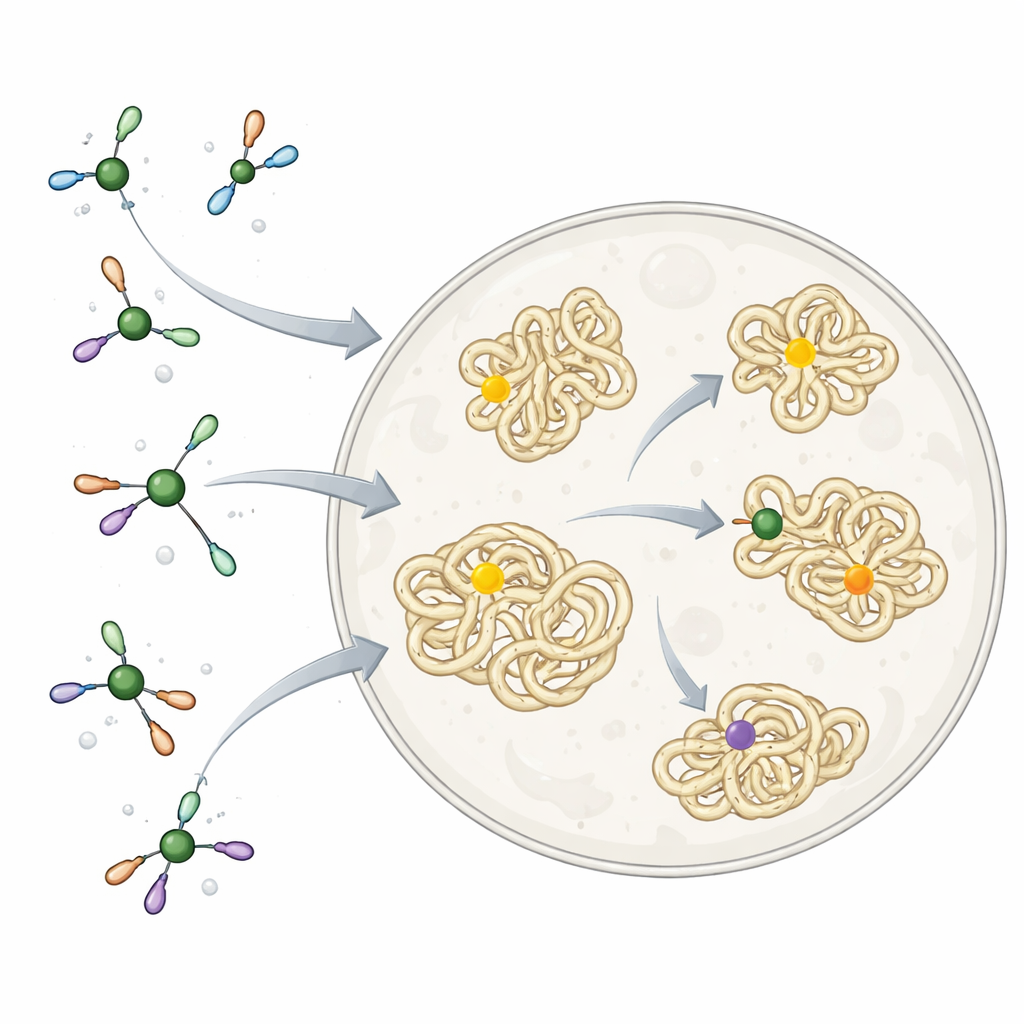
Nickel und andere Metalle arbeiten bereits unauffällig in unserem Körper als Bestandteile natürlicher Enzyme, können aber auch toxisch werden, wenn sie an der falschen Stelle binden. Die Natur löst das, indem sie Metalle mit sorgfältig ausgewählten kleinen Molekülen und Proteinen umgibt, die sie zu den richtigen Zielen lenken und unerwünschte Reaktionen blockieren. Chemiker hingegen verwenden oft Metallreagenzien, die extrem reaktiv und nicht auf das Leben abgestimmt sind. Diese waren ausgezeichnete Werkzeuge zum Aufbau komplexer Moleküle in einem Kolben, sind jedoch viel zu hart, um sie frei in Zellen einzusetzen — insbesondere wenn das Ziel darin besteht, ein kleines "Etikett" an eine spezifische Aminosäure in einem Protein zu koppeln, ohne den Rest der Zelle zu stören.
Entwicklung eines schonenderen Nickel‑Reagenzes
Die Forscher ließen sich davon inspirieren, wie Zellen selbst Nickel handhaben. Sie bauten eine Reihe von Nickelkomplexen, die von einem einfachen, biokompatiblen Liganden namens TMEDA umhüllt sind. Dieses kleine Molekül wirkt wie eine weiche Klammer: fest genug, um zu verhindern, dass Nickel an falsche zelluläre Komponenten bindet, aber locker genug, um eine Schlüsselreaktion zuzulassen. Die Reaktion verbindet ein „Aryl“-Fragment — eine flache, ringförmige Gruppe, die häufig in Arzneistoffen vorkommt — mit dem Schwefelatom der Aminosäure Cystein in Proteinen. An gereinigten Proteinen in Lösung hefteten diese Nickelkomplexe sehr schnell und selektiv Arylgruppen an einzelne Cysteinstellen an und funktionierten bei vielen unterschiedlichen Proteinformen und Positionen, was zeigte, dass die Chemie allgemein mit realen biologischen Molekülen kompatibel ist.
Proteine innerhalb lebender Zellen editieren
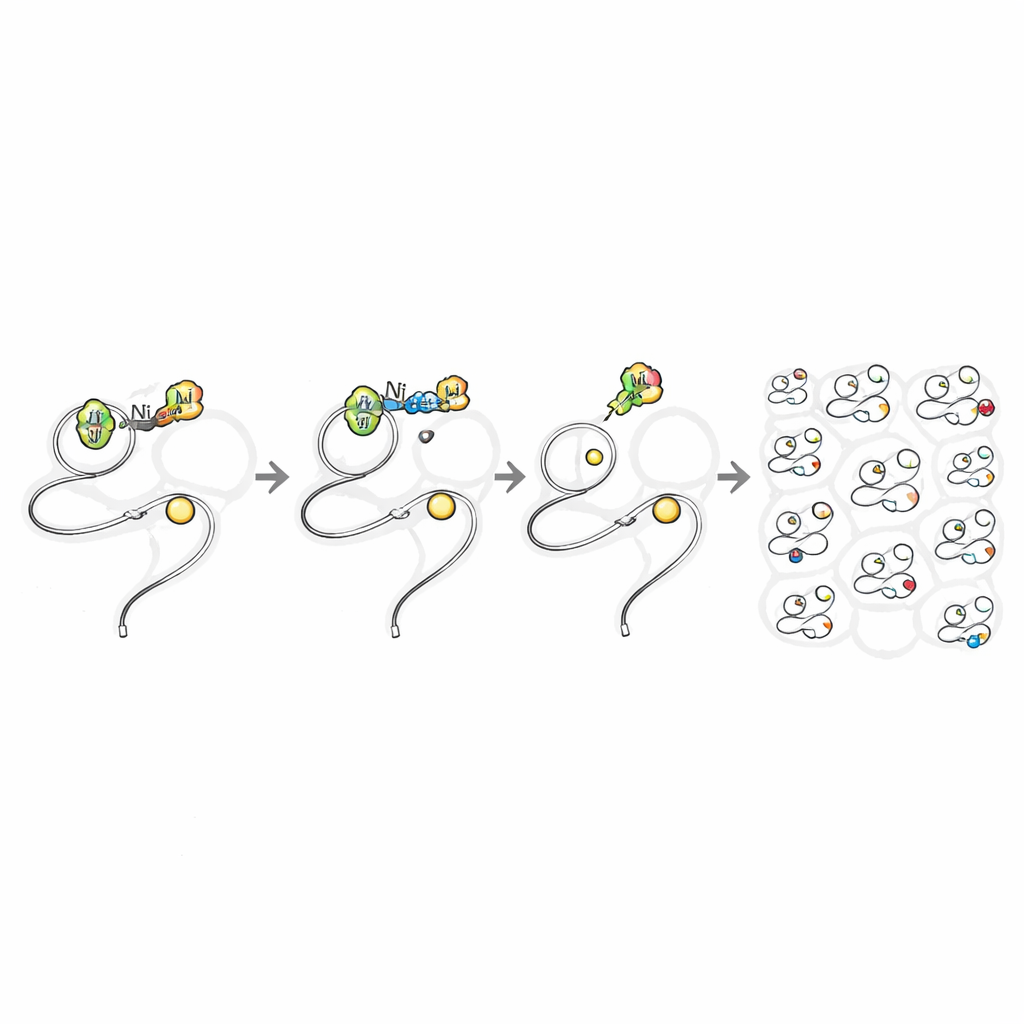
Als Nächstes prüfte das Team, ob dieselben Reagenzien in lebenden Zellen funktionieren können, ohne giftig zu sein. Sie verglichen einfache Nickelsalze, die bekanntermaßen schädlich sind, mit den TMEDA‑gebundenen Nickelkomplexen. In Säugerzellen führten die einfachen Nickelquellen bereits bei relativ niedrigen Dosen zu erheblichem Zelltod, während die ligand‑ausbalancierten Komplexe selbst bei millimolarer Konzentration gut verträglich blieben. Dieses Sicherheitsfenster erlaubte es den Forschern, bakterielle und Säugerzellen lange genug in den Nickelreagenzien zu baden, damit diese in die Zellen eindringen und Proteine modifizieren konnten. Durch Einbau eines Azid‑"Griffs" in eine Version der Arylgruppe konnten sie nach der Reaktion Fluoreszenzfarbstoffe oder Biotin‑Etiketten ankoppeln und so eine klare, dosisabhängige Färbung von Proteinen im gesamten Zytoplasma und Zellkern lebender Zellen sichtbar machen.
Reaktive Proteinstellen im Proteom kartieren
Mit einer sicheren und schnellen In‑Cell‑Reaktion verwandelten die Autoren diese Methode in ein Entdeckungswerkzeug. Sie behandelten lebende menschliche Zellen mit dem azidtragenden Nickelreagenz und verwendeten dann ein photolysierbares Biotin‑Tag sowie fortgeschrittene Massenspektrometrie, um genau zu sehen, welche Cysteine modifiziert worden waren. In einem einzigen Experiment detektierten sie nahezu 11.000 Cysteinstellen in fast 5.000 Proteinen — etwa doppelt so viele Proteine wie in allen bisherigen Live‑Cell‑Cystein‑Profiling‑Studien zusammen. Die Markierung war hochselektiv für Cystein und zeigte wenig Verzerrung gegenüber bestimmten Proteintypen, Lokalisationen oder bekannten aktiven Stellen. Bemerkenswerterweise gehörten viele der anvisierten Proteine nach aktuellen Standards der Wirkstoffforschung zu den als „nicht‑ligandierbar“ angesehenen, einschließlich niedrig abundanter Signalmoleküle und redox‑sensitiver Schalter, die sich allein durch genetische Methoden nur schwer untersuchen lassen.
Versteckte Pathogene in Echtzeit verfolgen
Die gleiche Chemie erwies sich auch als empfindlich genug, um fremde Proteine während einer Infektion zu erfassen. In menschlichen Zellen mit latenten viralen Sequenzen detektierte die Methode virale Transkriptionsfaktoren, die in extrem niedriger Menge vorhanden waren, einschließlich alternativer Spleißvarianten. Das Team infizierte anschließend Zellen mit zwei sehr unterschiedlichen Erregern: dem intrazellulären Bakterium Chlamydia trachomatis und dem Sindbis‑Virus, einem RNA‑Virus, das mit dem Chikungunya‑Virus verwandt ist. Durch pulsartige Behandlung infizierter Zellen mit dem Nickelreagenz zu verschiedenen Zeitpunkten konnten sie Cysteinstellen an wichtigen bakteriellen ribosomalen und regulatorischen Proteinen einfangen, während das Bakterium zwischen Lebenszyklusphasen wechselte, sowie an kritischen viralen nicht‑strukturellen Proteinen, die die RNA‑Replikation antreiben. Diese markierten Stellen heben sich nun als potenzielle Schwachstellen für zukünftige antivirale oder antibakterielle Strategien hervor.
Was das für die zukünftige Zellchemie bedeutet
Indem die Ligandenhülle um Nickel sorgfältig ausbalanciert wird, zeigt diese Arbeit, dass ein traditionell riskantes Metall eine präzise, kovalente Protein‑Editierreaktion tief in lebenden Zellen mit minimalem Schaden ausführen kann. Das macht es möglich, eine detaillierte, funktionelle Karte reaktiver Cysteinstellen im gesamten Proteom zu zeichnen, einschließlich Proteinen, die selten, transient oder schwer zu adressieren sind. Es bietet außerdem einen Weg, Pathogene innerhalb ihrer Wirtszellen auf der Ebene einzelner Aminosäuren zu verfolgen und zu untersuchen. Allgemeiner legt die Studie nahe, dass viele andere „verbotene“ Metallchemien auf ähnliche Weise gezähmt werden könnten und damit eine neue Ära eröffnet wird, in der die mächtigen Werkzeuge der synthetischen Chemie sicher innerhalb lebender Systeme eingesetzt werden können.
Zitation: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Schlüsselwörter: Cystein‑Profiling, Nickel‑Biokonjugation, Lebend‑Zell Proteinmarkierung, Chemoproteomik, Pathogen‑Proteomkartierung