Clear Sky Science · de
RNA-spezifische lokale Translation wird durch Kondensate für das Wachstum multinukleärer Zellen räumlich angeordnet
Wie große Zellen entfernte Aufgaben synchron halten
Zellen in unserem Körper sind üblicherweise winzige, abgeschlossene Einheiten mit einem einzigen Zellkern. Manche Organismen, darunter bestimmte Pilze und Muskelzellen, bilden jedoch riesige Kompartimente mit vielen Kernen, die sich das gleiche Zytoplasma teilen. In diesen Riesen können Signale und Moleküle lange brauchen, um sich durch Diffusion fortzubewegen, was die Frage aufwirft: Wie koordinieren sie Wachstum und Teilung über so große Entfernungen, ohne die Kontrolle zu verlieren? Diese Studie geht dieses Problem in einem multinukleären Pilz an und zeigt, wie winzige Tröpfchen innerhalb der Zelle die Proteinsynthese lokal dort feinsteuern, wo sie gebraucht wird.
Winzige Tröpfchen, die eine Riesen‑Zelle organisieren
Im fadenförmigen Pilz Ashbya gossypii enthalten lange röhrenartige Zellen, sogenannte Hyphen, viele Kerne, die asynchron teilen, während das Wachstum vor allem an den Spitzen stattfindet. Frühere Arbeiten zeigten, dass ein Protein namens Whi3 mikroskopische Tröpfchen oder Kondensate mit spezifischen messenger-RNAs (mRNAs) bildet, die für zentrale Regulatoren des Zellzyklus und des Spitzenwachstums codieren. Hier untersuchten die Autoren, welche Funktion diese Kondensate tatsächlich haben. Mit schneller dreidimensionaler Bildgebung fanden sie, dass Whi3-Kondensate in Größe und Anzahl variieren, je nachdem, wo sie sich in der Zelle befinden und wie lokal der Wachstums‑ und Teilungszustand ist. Große Kondensate gruppieren sich in der Nähe langsam wachsender Hyphenspitzen, während kleinere, variablere Kondensate Kerne in bestimmten Phasen des Zellzyklus umgeben. Mutante Pilze, die keine normalen Kondensate bilden können, wachsen an den Spitzen schneller und zeigen stärker synchronisierte Kernteilungen, was nahelegt, dass die Eigenschaften der Kondensate diese Prozesse koordinieren.
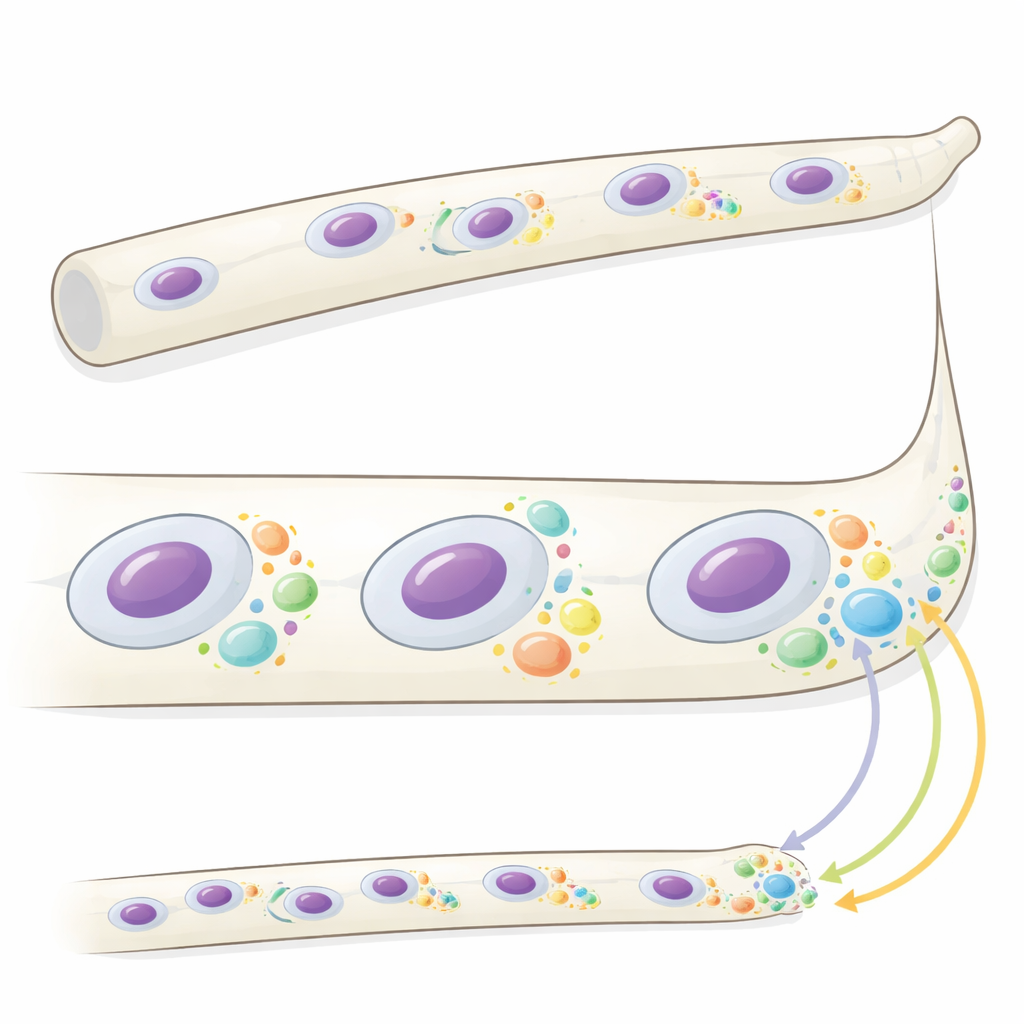
Lokale Proteinsynthese, räumlich und zeitlich geschrieben
Um zu prüfen, ob Whi3-Kondensate steuern, wo Proteine hergestellt werden, maßen die Forschenden die Translation — den Prozess, in dem mRNA in Protein übersetzt wird — für zwei wichtige Whi3-gebundene Botschaften. CLN3 codiert einen Cyclin, der die Zellteilung vorantreibt; BNI1 codiert einen Faktor, der das Wachstum an der Hyphenspitze gestaltet. Mithilfe einer empfindlichen Fluoreszenz-Methode, die aktive Ribosomen auf einzelnen endogenen mRNA-Molekülen detektiert, zeigten die Forschenden, dass CLN3 vor allem in der Nähe bestimmter Kerne und nur während spezifischer Phasen ihres Zyklus übersetzt wird, insbesondere rund um mitotische Kerne. BNI1-mRNA sammelt sich an Hyphenspitzen, ihre Translation dort ist jedoch meist spärlich und variabel. Wenn Whi3 durch eine Phospho-mimetische Mutation verändert wird, reichert sich BNI1-Translation stark an den Spitzen an und das Spitzenwachstum beschleunigt sich, was zeigt, dass Whi3 je nach Zustand und Standort Translation entweder hemmen oder erlauben kann.
Minimale Bausteine, viele Ausgänge
Um zu testen, ob diese Feinabstimmung eine intrinsische Eigenschaft der Kondensatbestandteile ist, rekonstruierten die Autor:innen das System in zellfreien Extrakten. Sie koppelten einen Luciferase-Reporter an die regulatorischen Regionen der CLN3‑ oder BNI1-mRNAs und mischten diese RNAs mit gereinigtem Whi3 in unterschiedlichen Konzentrationen. Bei niedrigen Konzentrationen, bei denen keine Tröpfchen entstehen, änderte sich die Translation kaum. Bei höheren Konzentrationen, die Kondensatbildung fördern, wurde die CLN3-gekoppelte Translation stark reprimiert, je mehr Whi3 und je größer die Kondensate wurden. BNI1 verhielt sich anders: moderate Kondensatniveaus erhöhten seine Translation, während bei höheren Mengen oder größeren Kondensaten das System in Repression umschlug. Mutante Whi3‑Versionen, die kleinere oder weniger Tröpfchen bildeten, oder RNAs mit weniger Whi3-Bindungsstellen verschoben diese Reaktionen, oft durch Aufhebung der Repression und Steigerung der Translation. Diese Experimente zeigen, dass dieselben Grundzutaten — Whi3, seine Ziel‑RNAs und deren Kondensate — ein Kontinuum von Translationalzuständen erzeugen können, allein durch Änderung von Konzentration, Wechselwirkungsstärke oder Tropfengröße.
Wo Translation stattfindet: am Rand des Tropfens
Bulk-Assays mitteln über viele Moleküle hinweg und können nicht zeigen, wo genau Translation innerhalb oder um Kondensate herum stattfindet. Um dies direkt sichtbar zu machen, verwendete das Team einen „MoonTag“-Reporter, der aufleuchtet, wenn neue Proteinketten aus Ribosomen hervortreten. In vitro sahen sie MoonTag‑Signale, die sich auf und innerhalb von Whi3–RNA‑Tröpfchen ansammelten, was beweist, dass diese Kondensate tatsächlich aktive Translationsorte sein können und keine bloßen Speicher. Auffällig war, dass sowohl Ribosomen als auch Signale naszierender Proteine am stärksten an der Tropfenoberfläche waren und einen hellen Ring um jedes Kondensat bildeten. Kleinere Kondensate, die im Verhältnis mehr Oberfläche zur Volumen haben, unterstützten mehr Translation pro RNA als größere Tropfen, die insgesamt repressiver waren. Änderungen der RNA‑Valenz oder des Ladungszustands von Whi3 verschoben, ob diese translationsfreundliche Zone an der Oberfläche lag oder tiefer im Inneren, was darauf hindeutet, dass subtile molekulare Eigenschaften des Kondensats steuern, wie leicht die Translationsmaschinerie auf die darin befindlichen RNAs zugreifen kann.
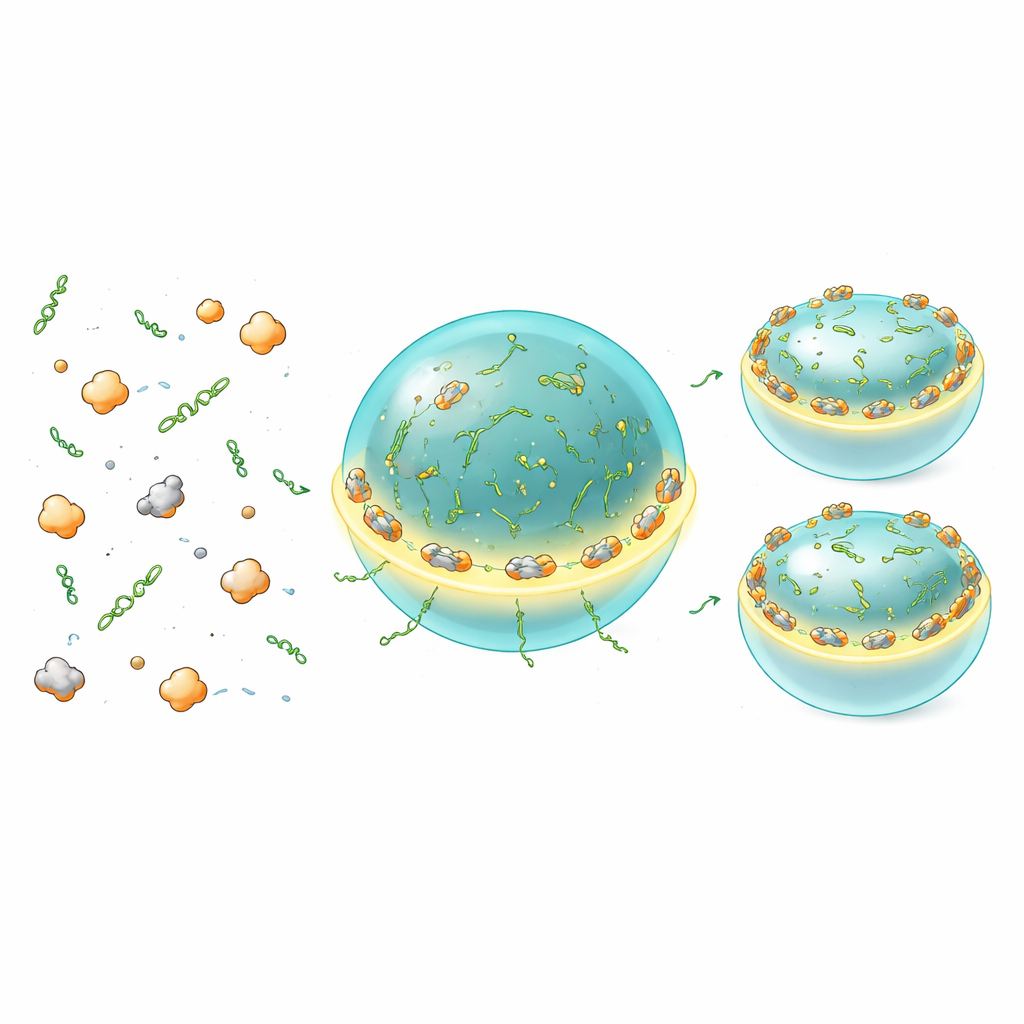
Fein abgestimmte Dosierung für ausgewogenes Wachstum
Insgesamt zeichnen die Ergebnisse Whi3–RNA‑Kondensate als verstellbare Ventile, die lokal produzierte Proteine dosieren, statt als einfache Ein‑/Aus‑Schalter. Im Pilz bedeutet das, dass der CLN3‑Cyclin in Pulsen um ausgewählte Kerne herum produziert werden kann, um deren Teilungszyklen phasenverschoben zu halten, während BNI1 in intermittierenden Schüben an Hyphenspitzen hergestellt wird, um Wachstum zu stützen, aber eine unkontrollierte Ausdehnung an einem einzelnen Ort zu verhindern. Wenn die Kondensatbildung oder deren Eigenschaften gestört sind, geht diese feine Kontrolle verloren: Die Proteinproduktion wird räumlich und zeitlich einheitlicher, Kerne teilen sich synchroner, Verzweigungsmuster ändern sich und die Gesamtmorphologie gerät aus dem Gleichgewicht. Für ein breites Publikum lautet die Kernbotschaft: Zellen können winzige, phasentrennende Tröpfchen als räumlich und zeitlich einstellbare Reaktoren nutzen, sodass riesige, multinukleäre Zellen Wachstum und Teilung über große Distanzen koordinieren, indem sie lokal bestimmen, wann und wo Proteine entstehen.
Zitation: Geisterfer, Z.M., Jalihal, A.P., Cole, S.J. et al. RNA-specific local translation is patterned by condensates for multinucleate cell growth. Nat Cell Biol 28, 507–519 (2026). https://doi.org/10.1038/s41556-026-01887-y
Schlüsselwörter: biomolekulare Kondensate, lokale Translation, Kontrolle des Zellzyklus, Pilzhyphen, Phasentrennung