Clear Sky Science · de
Lysin-11-Ubiquitinierung treibt Typ-I/III-Interferon-Induktion durch cGAS–STING und die Toll-ähnlichen Rezeptoren 3 und 4
Wie unsere Zellen Alarm schlagen
Wenn Viren oder gefährliche Moleküle in den Körper eindringen, müssen unsere Zellen innerhalb von Minuten entscheiden, ob sie kraftvolle antivirale Alarmsignale namens Interferone auslösen. Diese Signale können uns vor schweren Infektionen bewahren – doch bei Fehlzündungen treiben sie auch schädliche Autoimmunerkrankungen voran. Diese Studie enthüllt ein bislang verborgenes molekulares „Schaltzentrum“ in Zellen, das mitentscheidet, wann Interferonantworten eingeschaltet und wann sie zurückgehalten werden. Das Verständnis dieses Schaltzentrums liefert Hinweise für bessere Impfstoffe, antivirale Therapien und Behandlungen interferongetriebener Erkrankungen.
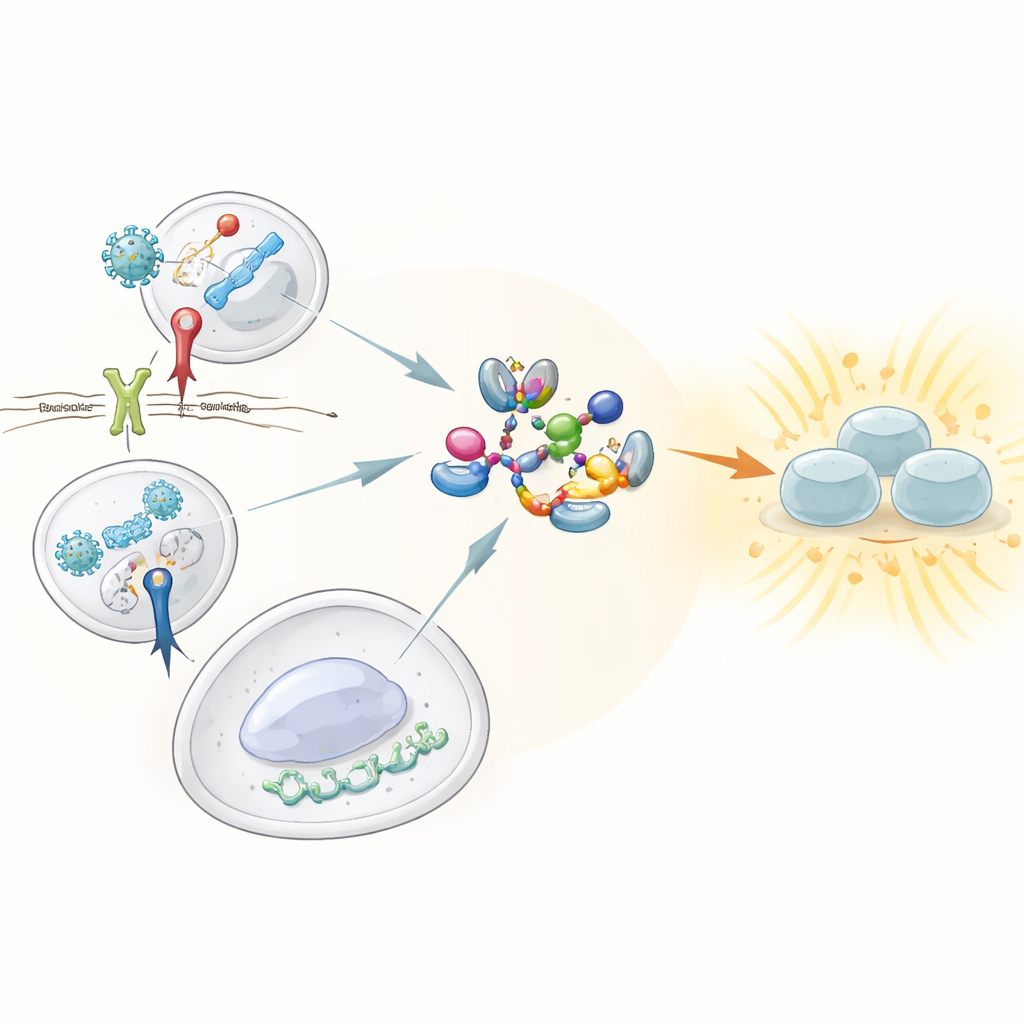
Wächter, die Gefahr erkennen
Unser angeborenes Immunsystem verlässt sich auf Wächter, sogenannte Mustererkennungsrezeptoren, die nach typischen Merkmalen von Viren und Bakterien fahnden. Drei davon stechen durch ihre Fähigkeit hervor, starke Interferonantworten auszulösen: Toll-like Rezeptor 3 (TLR3), der doppelsträngige virale RNA erkennt; Toll-like Rezeptor 4 (TLR4), der einen Bestandteil bakterieller Zellwände wahrnimmt; und der cGAS–STING-Weg, der fehlplatzierte DNA im Inneren von Zellen erkennt. Alle drei müssen ein zentrales Enzym namens TBK1 aktivieren, das wiederum den Transkriptionsfaktor IRF3 einschaltet, um die Produktion von Typ-I- und Typ-III-Interferonen zu steuern. Bislang war wenig bekannt darüber, wie diese Sensoren auf TBK1 zulaufen, um es in seinen aktiven Zustand zu versetzen.
Ein verborgenes molekulares Verbindungsstück
Die Forschenden entdeckten, dass ein Protein namens ANKIB1 als entscheidende Verbindung zwischen diesen Sensoren und TBK1 fungiert. ANKIB1 ist ein Enzym, das kleinen molekularen Anhängseln, den sogenannten Ubiquitinketten, an andere Proteine befestigt. Wichtig ist, dass es eine spezifische Kettenart aufbaut, basierend auf einer Verknüpfung namens „K11“, die vorher eher aus der Zellteilungsforschung als aus der Immunologie bekannt war. In menschlichen Zellen ohne ANKIB1 führte die Stimulation von TLR3 oder die Aktivierung von STING nicht mehr zu einer ordnungsgemäßen Aktivierung von TBK1 und IRF3, und Interferon-Gene wurden kaum hochreguliert. Die Wiederherstellung von ANKIB1 brachte die Antwort zurück, was zeigt, dass dieses einzelne Enzym notwendig und ausreichend ist, um diesen Ast des antiviralen Alarms anzutreiben.
Aufbau einer Andockplattform für Relaissignale
Genauere Untersuchungen zeigten, wie ANKIB1 seine Wirkung entfaltet. Wenn TLR3 oder STING Gefahr erkennen, bilden sie Mehrproteinplattformen, sogenannte Signalosome. ANKIB1 wird über eine Region, die Ubiquitin erkennt, an diese Plattformen rekrutiert. Dort versieht es mehrere Schlüsselkandidaten – darunter die Adapterproteine TRIF und STING selbst sowie weitere Signalmoleküle – mit K11-verknüpften Ubiquitinketten. Diese Ketten markieren Proteine nicht einfach zum Abbau; vielmehr wirken sie wie molekulares Klettband. Ein anderes Protein, Optineurin (OPTN), wird spezifisch an diese modifizierten Stellen gebunden. Als Relay-Adapter bringt OPTN dann TBK1 in den Komplex, damit es aktiviert werden und das Signal an IRF3 und Interferon-Gene weiterleiten kann. Wurde OPTN entfernt, brach die TBK1-Aktivierung zusammen – ein Hinweis darauf, dass die K11-gekoppelte Markierung durch ANKIB1 und die OPTN-Bindung eine einzige, essenzielle Achse bilden.
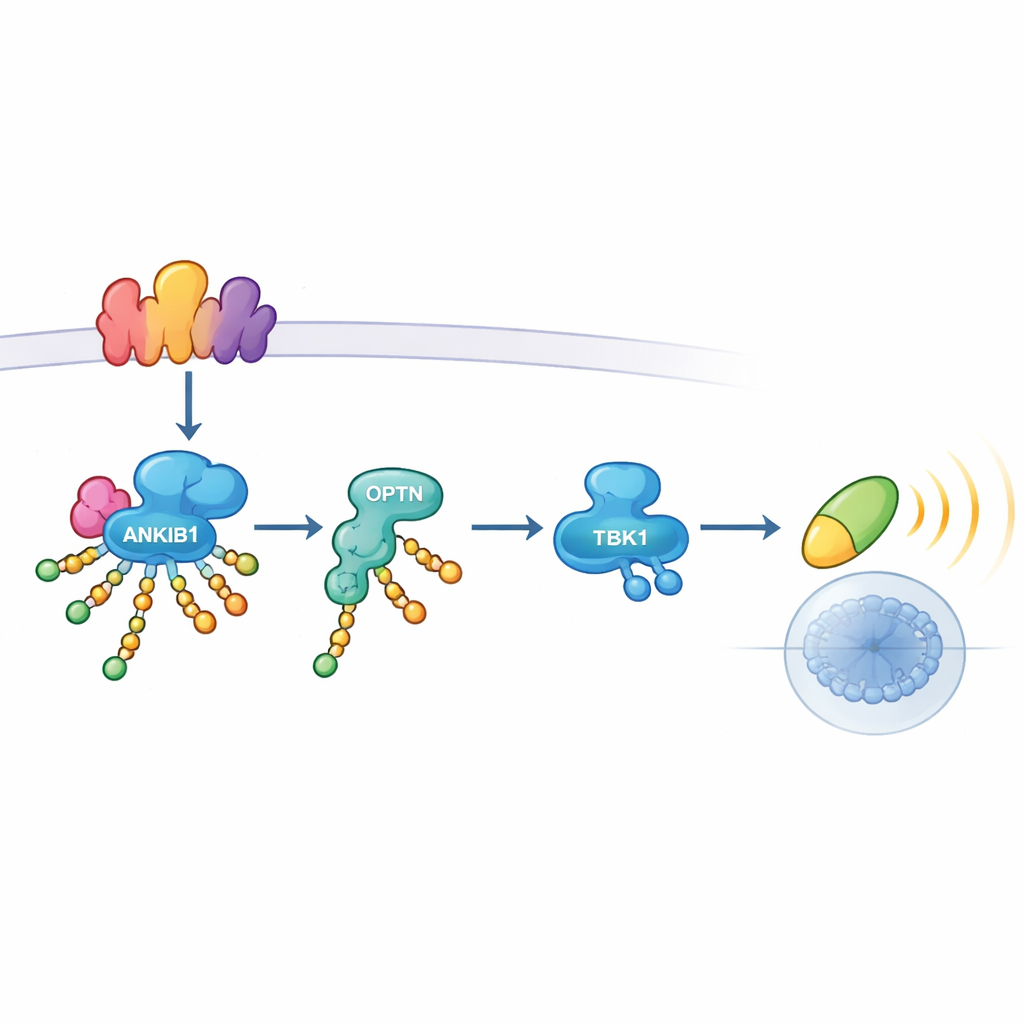
Wann dieser Weg wichtig ist – und wann nicht
Das Team fragte anschließend, ob dieser Mechanismus universell für alle antiviralen Sensoren gilt. Sie fanden heraus, dass ANKIB1 entscheidend für die Interferoninduktion durch TLR3, den TRIF-abhängigen Arm von TLR4 und den cGAS–STING-Weg ist, die alle OPTN als Hauptadapter zu TBK1 nutzen. Im Gegensatz dazu verlässt sich ein anderer Sensor, RIG-I, der virale RNA erkennt, auf ein anderes Set von Adapterproteinen und benötigt weder ANKIB1 noch OPTN zur Aktivierung von TBK1. Experimente an Mäusen spiegelten diese zellbasierten Befunde wider. Tiere ohne Ankib1 produzierten deutlich weniger Interferon nach Aktivierung von TLR3 oder STING, waren vor einem tödlichen, interferongetriebenen Entzündungssyndrom geschützt, wurden jedoch viel anfälliger für Infektionen mit Herpes-simplex-Virus 1, einem DNA-Virus, dessen Kontrolle stark von cGAS–STING-getriebener Interferonantwort abhängt. Die Reaktionen auf Influenzaviren, die hauptsächlich von RIG-I erkannt werden, blieben weitgehend erhalten.
Abwägung zwischen Schutz und Schaden
Zusammen zeigen diese Ergebnisse, dass von ANKIB1 erzeugte K11-verknüpfte Ubiquitinketten eine zentrale Rolle in einem wichtigen Zweig der angeborenen antiviralen Signalgebung spielen. Indem ANKIB1 Andockstellen für OPTN schafft, hilft es beim Zusammenbau des präzisen molekularen Relais, das von TLR3, TLR4 (über TRIF) und cGAS–STING erkannte Gefahr in eine robuste Interferonproduktion übersetzt. Diese Achse ist zweischneidig: Sie ist essentiell für die Abwehr bestimmter Viren, treibt jedoch auch interferongetriebene Entzündungserkrankungen an, wenn sie überaktiviert wird. Da die katalytische Aktivität und spezifische Domänen von ANKIB1 für diese Funktion erforderlich sind, bieten sie vielversprechende Ansatzpunkte für künftige Medikamente, die entweder schädliche Interferonantworten bei Autoimmunerkrankungen dämpfen oder die antivirale Immunität dort stärken, wo sie zu schwach ist.
Zitation: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Schlüsselwörter: angeborene Immunität, Interferon-Signalgebung, Ubiquitinierung, cGAS–STING-Signalweg, Virusinfektion