Clear Sky Science · de
Peritumorales Fettgewebe fördert Immunflucht beim kolorektalen Krebs durch adipose–mesenchymale Transformation
Warum das Bauchfett rund um Tumoren eine Rolle spielt
Kolorektales Karzinom wächst in der Darmwand, liegt aber direkt neben einem dicken Polster aus Bauchfett. Die meisten Menschen betrachten dieses Fett als passive Polsterung. Diese Studie zeigt etwas Überraschendes: Das Fett, das den Tumor umgibt, kann im Verborgenen krebsbekämpfende Immunzellen vom Tumor wegziehen und so dem Krebs helfen, sich dem Immunsystem zu entziehen. Das Verständnis dieses versteckten Tauziehens eröffnet neue Wege, vorherzusagen, wer auf Immuntherapie anspricht, und wie sich diese Behandlungen wirksamer machen lassen.
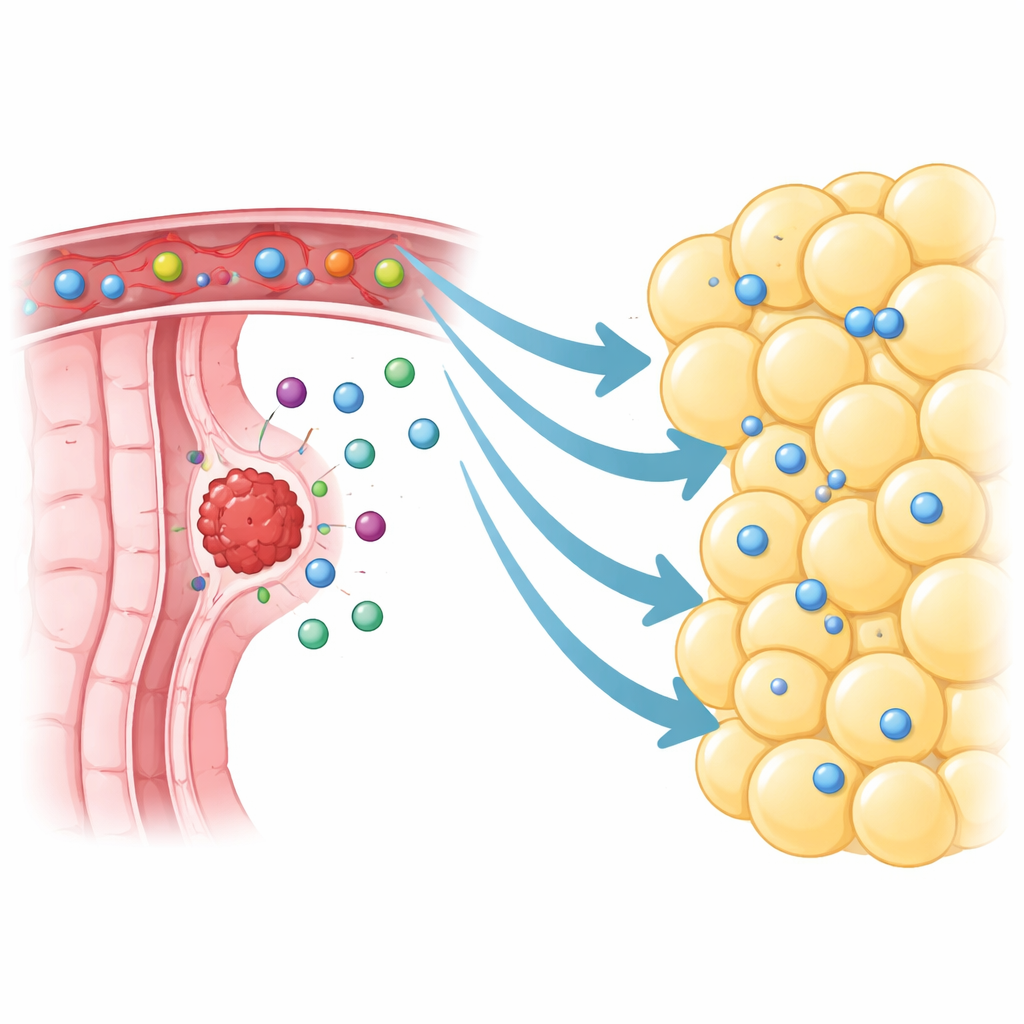
Eine geschäftige immunologische Nachbarschaft neben dem Tumor
Die Forscher konzentrierten sich auf das viszerale Fett, das den kolorektalen Tumoren unmittelbar anliegt, das sogenannte peritumorale viszerale Adiposegewebe. Mit Einzelzell-RNA-Sequenzierung kartierten sie mehr als 370.000 einzelne Zellen aus Tumoren, nahegelegenem Fett, entferntem Fett und normalem Gewebe. Anstatt ruhig und träge zu sein, wimmelte es im Fett neben den Tumoren vor Immunzellen, insbesondere T‑Zellen und B‑Zellen. Man fand sogar organisierte Cluster, die Mini-Lymphknoten ähneln — ein Hinweis darauf, dass dieses Gewebe aktive Immunreaktionen beherbergen kann. Im Vergleich zu weiter entfernt entnommenem Fett enthielt das peritumorale Fett deutlich mehr Lymphozyten, darunter Gedächtnis- und tumorspezifische Killer-T‑Zellen, die im Prinzip nach Krebs suchen sollten.
Wenn hilfreiche Immunzellen am falschen Ort landen
Um zu prüfen, ob dieses immunreiche Fett hilfreich oder schädlich war, verwendete das Team Mausmodelle, in denen Tumoren in der Nähe eines Fettpolsters implantiert wurden, das der menschlichen Situation ähnelt. Anschließend entfernten sie dieses nahegelegene Fett chirurgisch oder lösten es chemisch auf. Entgegen der Intuition verlangsamte das Entfernen des peritumoralen Fetts das Tumorwachstum. Tumoren von Mäusen, denen dieses Fett entzogen worden war, enthielten mehr CD4‑ und CD8‑T‑Zellen, einschließlich T‑Zellen, die Tumorantigene erkannten. Zusätzliche Experimente mit nachverfolgten Spender-Immunzellen zeigten, dass viele dieser Zellen bei vorhandenem Fettpolster im Fett akkumulierten statt im Tumor. Das Entfernen des Fetts leitete die Zellen in den Tumor um und stärkte die antitumorale Reaktion. Mit anderen Worten: Das Fett fungierte als konkurrenzreservoir, das Immunzellen aufsaugte und daran hinderte, ihr eigentliches Ziel zu erreichen.
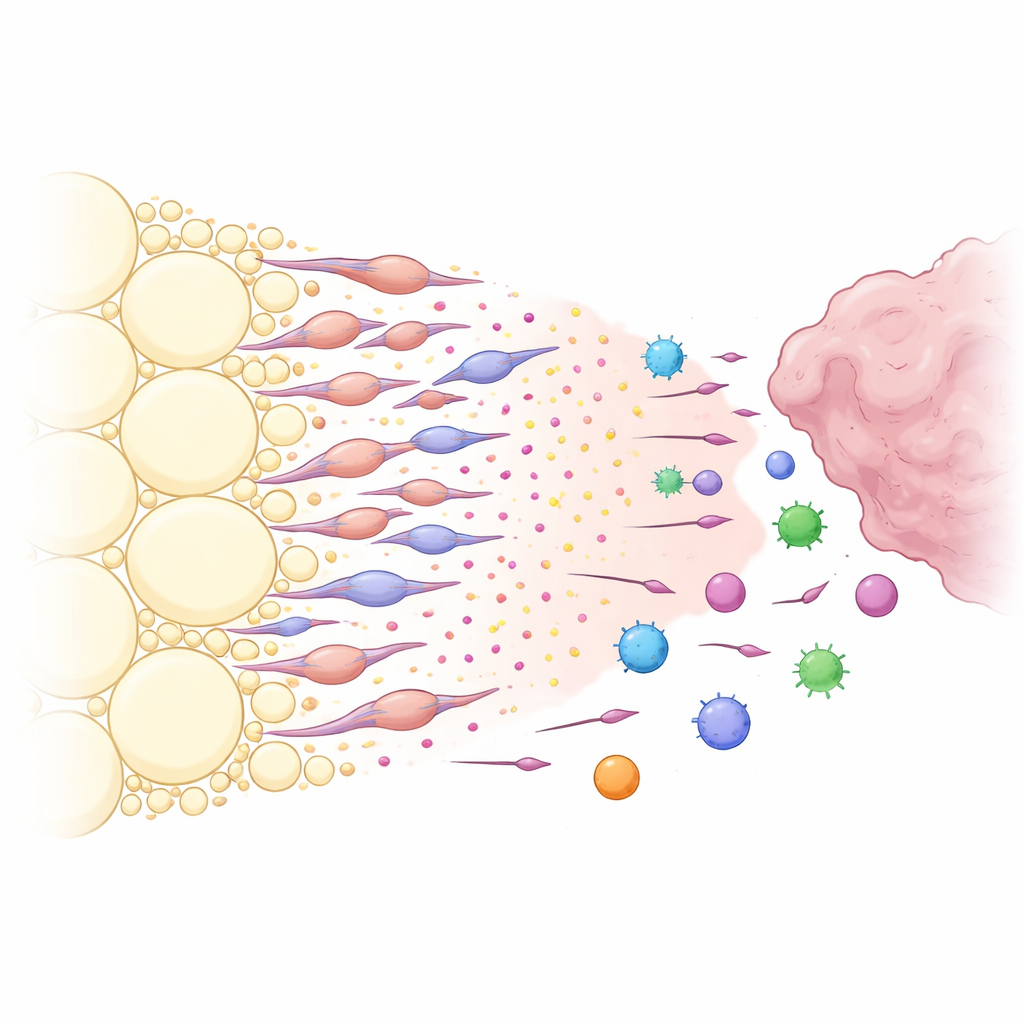
Ein chemischer Lockstoff, erzeugt von umgewandelten Fettzellen
Was machte das peritumorale Fett so effektiv beim Einfangen von Immunzellen? Durch die Analyse der Kommunikationssignale zwischen Zelltypen identifizierten die Forscher einen starken chemischen Signalweg um das Molekül CXCL12 und seinen Rezeptor CXCR4. Stromale Zellen im Fett nahe dem Tumor produzierten hohe Mengen an CXCL12, während viele Immunzellen CXCR4 exprimierten und daher auf dieses Signal reagierten. Das lokale Blockieren von CXCL12 im Fett oder dessen genetische Deletion im Fettstrom führte zu Tumorverkleinerung und ermöglichte mehr CXCR4‑positive Immunzellen, in den Tumor einzudringen statt abgelenkt zu werden. Das Team entdeckte dann, dass die Hauptproduzenten von CXCL12 keine gewöhnlichen Fettzellen waren, sondern eine spezielle Gruppe von fettabgeleiteten, fibroblastähnlichen Zellen, die sie adipose‑abgeleitete tumorumgebungsassoziierte Fibroblasten nannten. Vom Tumor freigesetzte Faktoren, insbesondere der Wachstumsfaktor TGF‑β1, trieben lokale adipöse Stromazellen dazu, sich in diese fibroblastähnlichen Zellen zu verwandeln, die wiederum große Mengen CXCL12 und andere wachstumsfördernde Signale ausschütteten.
Ein Schild in eine Schwachstelle verwandeln
Da diese transformierten Zellen Immunzellen vom Tumor weglenken, prüften die Forscher, ob das Zerlegen dieses „Immun-Sinks“ die Immuntherapie verbessern könnte. In Mäusen, bei denen die adipose‑abgeleiteten tumorumgebungsassoziierten Fibroblasten selektiv eliminiert werden konnten, wurde eine Behandlung mit einem PD‑1‑blockierenden Antikörper deutlich wirksamer: Die Tumoren wuchsen weniger, und mehr tumorspezifische sowie CXCR4‑positive T‑Zellen infiltrierten den Tumor. Ebenso wirkten Wirkstoffe oder Antikörper, die entweder CXCL12 oder seinen Rezeptor CXCR4 blockierten, synergistisch mit PD‑1‑Blockade in subkutanen und orthotopen Modellen des kolorektalen Karzinoms. Diese Kombinationen reduzierten nicht nur die Tumorgröße, sondern veränderten auch die immunologische Landschaft innerhalb des Tumors.
Hinweise aus Patientenaufnahmen und das Weitere
Das Team fragte dann, ob ihre Befunde bei echten Patienten relevant sind. In einer Gruppe von Personen mit lokal fortgeschrittenem kolorektalen Krebs, die eine kombinierte Chemotherapie, Strahlentherapie und PD‑1‑Immuntherapie erhielten, wiesen diejenigen mit einem kompletten Ansprechen vor der Behandlung tendenziell ein kleineres Volumen an peritumoralem viszeralem Fett im MRT auf. Quantitativ sagte die Fläche dieses Fetts das Therapieansprechen besser voraus als einige Standardgewebsmarker, und Patienten mit großen peritumoralen Fettvolumina hatten deutlich geringere Ansprechraten. Für Nicht‑Spezialisten ist die Erkenntnis eindrücklich: Nicht nur der Tumor selbst, sondern auch das unmittelbar ihn umgebende Fett kann bestimmen, wie gut Immuntherapie wirkt. Indem man sich auf dieses Fett konzentriert — sei es durch Messung zur Steuerung von Behandlungsentscheidungen oder durch gezielte Bekämpfung seiner transformierten Stromazellen und des CXCL12–CXCR4‑Signals — könnte man ein schützendes Schild des Tumors in eine therapeutische Schwachstelle verwandeln.
Zitation: Wang, JH., Zheng, YQ., Qian, ZY. et al. Peritumoural adipose tissue drives immune evasion in colorectal cancer via adipose–mesenchymal transformation. Nat Cell Biol 28, 581–595 (2026). https://doi.org/10.1038/s41556-026-01885-0
Schlüsselwörter: kolorektales Karzinom, Tumormikroumgebung, viszerales Fett, Immuntherapie, CXCL12 CXCR4