Clear Sky Science · de
Umgestaltung des ER ist ein Merkmal des Alterns und hängt von ER‑phagie ab
Warum die inneren Falten der Zelle mit dem Älterwerden wichtig sind
Die Zellen in unserem Körper sind von einem labyrinthartigen Membransystem durchzogen, dem endoplasmatischen Retikulum, kurz ER. Diese Struktur hilft beim Aufbau von Fetten und Proteinen, steuert Zucker- und Kalziumhaushalt und steht im ständigen Austausch mit anderen Zellkompartimenten. Da so viele lebenswichtige Aufgaben über dieses Netzwerk laufen, kann jede langfristige Umgestaltung des ER beeinflussen, wie unser Gewebe altert, wie widerstandsfähig es gegenüber Stress ist und letztlich, wie lange wir gesund bleiben. Diese Studie stellt eine auf den ersten Blick einfache Frage: Altert das ER selbst auf eine spezifische, organisierte Weise, und falls ja, ist diese Veränderung schädlicher Verschleiß oder eine eingebaute Schutzstrategie?
Ein verborgener Wandel an der zellulären Werkbank
Mit Hilfe fortgeschrittener Mikroskopie und fluoreszenter Marker in dem winzigen Wurm Caenorhabditis elegans verfolgten die Autorinnen und Autoren das ER in lebenden Tieren, als diese von der jungen Erwachsenenphase ins hohe Alter übergingen. In jugendlichen Zellen bildet das ER breite, geschichtete Membranschichten, die mit der Proteinbiosynthese bestückt sind und einem ordentlich eingerichteten Fabrikboden ähneln. Mit dem Altern schrumpfen diese Schichten an Volumen und weichen einem dünneren, eher tubulären Netz, das weniger Raum einnimmt. Messungen zeigten, dass der Gesamtgehalt an ER deutlich abnimmt, während sich seine Form ändert — ein Hinweis darauf, dass es sich nicht um zufällige Schäden, sondern um ein koordiniertes Schrumpfen und Umkonfigurieren des Organells handelt.
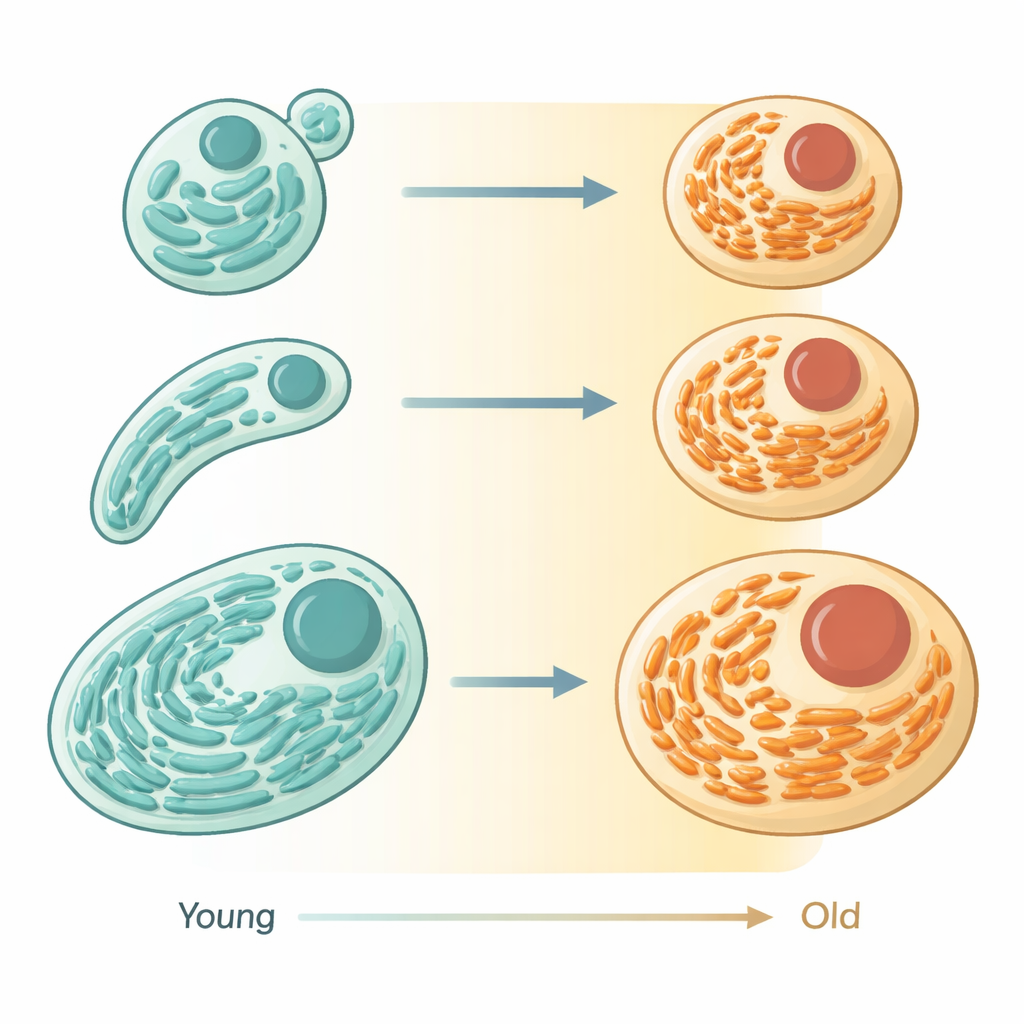
Vom Proteinaufbau zur Fettbewirtschaftung
Form in der Biologie signalisiert oft Funktion, und das traf auch hier zu. Die Forschenden verglichen, wie ER‑assoziierte Proteine im Laufe der Zeit in verschiedenen Wurmgeweben verändert werden. Proteine, die am Aufbau, Falten und Kontrollieren anderer Proteine beteiligt sind, sanken mit dem Alter in Einklang mit dem Verlust der schichtartigen ER‑Struktur. Im Gegensatz dazu blieben viele ER‑Proteine, die mit Fett‑ und Membranstoffwechsel zu tun haben, konstant oder nahmen sogar zu. Gemeinsam deuten diese Muster darauf hin, dass alternde Zellen die Massenproduktion von Proteinen drosseln und die Ressourcen des ER stärker auf das Management von Fetten und Membranen ausrichten. Auffällig ist, dass bei der Analyse großer Datensätze aus alternden Mäusen ein ähnliches Bild auftauchte: ER‑Proteine für Sekretion und Proteinverarbeitung gingen tendenziell zurück, während solche, die am Lipidstoffwechsel und an der Autophagie beteiligt sind, relativ erhalten blieben oder zunahmen.
Ein zellulärer Recyclingweg hinter der Umgestaltung
Was treibt diese groß angelegte Umgestaltung an? Das Team führte die Veränderungen auf ER‑phagie zurück, eine Form selektiver Selbstverzehrung, bei der die Zelle ER‑Stücke in Recyclingvesikel verpackt, damit sie in Lysosomen abgebaut werden. Das Blockieren zentraler Autophagie‑Gene in Würmern verhinderte den normalen altersbedingten Verlust an ER‑Masse und den Wechsel von Schichten zu Tubuli und zeigte damit, dass dieser Recyclingweg nicht nur Reste aufräumt, sondern das Organell aktiv formt. Unabhängige Experimente in Hefen bestätigten, dass ER‑Komponenten mit dem Alter zum Recyclingzentrum der Zelle umgeleitet werden — ebenfalls abhängig von Autophagie. Elektronenmikroskopie zeigte ER‑Fragmente in degradativen Kompartimenten und lieferte damit physische Belege dafür, dass Teile des Netzwerks gezielt entfernt werden.

Gewebespezifische Steuerung eines gemeinsamen Altersprogramms
Obwohl die ER‑Umgestaltung in vielen Wurmgeweben beobachtet wurde — Darm, hypodermales, hautähnliches Gewebe, Muskel und Nervenzellen — erwiesen sich die auslösenden Faktoren als gewebespezifisch. Im Hypodermis verband ein zuvor wenig bekanntes Membranprotein namens TMEM‑131 den ER‑Umsatz mit der Kollagenverarbeitung. Wird TMEM‑131 reduziert, wird der altersbedingte ER‑Verlust in diesem Gewebe größtenteils verhindert, was nahelegt, dass das ER verkleinert wird, wenn seine Kollagen‑„Kunden“ abnehmen. Im Darm hingegen war der entscheidende Regulator der IRE‑1–XBP‑1‑Arm der UPR (unfolded protein response), ein zentrales Stress‑Erkennungsnetzwerk. Das Stilllegen dieses Signalzweigs bewahrte das intestinale ER während des Alterns, was darauf hindeutet, dass in diesem Organ ER‑Stress‑Signalgebung mitentscheidet, wann Teile des ER geopfert werden sollten.
Das ER für ein längeres Leben umschalten
Die Studie verknüpft die ER‑Umgestaltung auch mit Lebensverlängerung. Bei Würmern lösten mehrere bekannte lebensverlängernde Interventionen — Abschwächung insulinähnlicher Signale, Reduktion der mTOR‑Nährstoffwahrnehmung, Entfernung der Keimbahn oder leicht verlangsamte Proteinsynthese — früh im Erwachsenenalter eine ER‑Verkleinerung und eine Zunahme tubulärer Netzwerke aus, statt erst im hohen Alter. Wichtig ist: Wenn ER‑phagie ausgeschaltet wurde, gingen die normalerweise durch mTOR‑Hemmung erzielten Lebensverlängerungen in Hefe und Würmern deutlich zurück oder fielen ganz weg. Das legt nahe, dass ein sorgfältig gesteuertes Beschneiden des ER nicht nur eine Begleiterscheinung des Alterns oder einer Behandlung ist, sondern ein Mechanismus, durch den Zellen einen widerstandsfähigeren Zustand erreichen.
Was das für gesundes Altern bedeutet
Für eine(n) Laien mag der Verlust eines beträchtlichen Teils einer Schlüsselstruktur der Zelle im Alter rein schädlich klingen. Die vorliegende Arbeit zeichnet ein nuancierteres Bild. Das ER scheint aktiv umgestaltet zu werden — durch selektiven Selbstverzehr und gewebespezifische Regulatoren — sodass alternde Zellen weniger neue Proteine produzieren, mehr in Lipid‑ und Membranmanagement investieren und möglicherweise das Risiko chronischen Stresses mindern. Diese Umgestaltung scheint von Hefen bis zu Säugetieren konserviert zu sein und ist für zumindest einige Formen der Lebensverlängerung erforderlich. Langfristig kann das Schrumpfen des ER jedoch mit Kompromissen verbunden sein und beeinflussen, wie gut Zellen andere Organellen reparieren und mit altersbedingtem Verfall umgehen. Indem ER‑phagie und ER‑Dynamik als Kernmerkmale normalen und verzögerten Alterns sichtbar gemacht werden, hebt diese Forschung eine neue Reihe potenzieller Hebel hervor, die eventuell einst verstellt werden könnten, um gesünderes, widerstandsfähigeres Gewebe zu fördern.
Zitation: Donahue, E.K.F., Hepowit, N.L., Ruark, E.M. et al. ER remodelling is a feature of ageing and depends on ER-phagy. Nat Cell Biol 28, 449–464 (2026). https://doi.org/10.1038/s41556-025-01860-1
Schlüsselwörter: endoplasmatisches Retikulum, Autophagie, zelluläres Altern, Protein‑Homöostase, Lipidstoffwechsel