Clear Sky Science · de
Zeitaufgelöste funktionelle Genomik mit Deep Learning zeigt globale hierarchische Kontrolle der Autophagie
Wie Zellen sich selbst recyceln — und wissen, wann sie aufhören müssen
Zellen überstehen kärgliche Zeiten, indem sie eigene Bestandteile durch einen Prozess namens Autophagie recyceln — wörtlich „Selbstessen“. Zu wenig Recycling lässt beschädigte Komponenten ansammeln; zu viel führt dazu, dass die Zelle sich selbst auffrisst. Diese Studie stellt eine auf den ersten Blick einfache Frage mit weitreichenden Folgen für Altern und Krankheit: Wie schaltet eine lebende Zelle Autophagie in den richtigen Momenten ein und aus, wenn Nährstoffe schwanken?
Tausende Zellen durch einen Wechsel von Überfluss zu Mangel verfolgen
Um dies zu untersuchen, nutzten die Forschenden die Bäckerhefe als Modell und verfolgten nahezu sechstausend verschiedene Mutantenstämme während Hungern und Erholung. Jeder Hefestamm trug fluoreszierende Marker für Strukturen, die an der Autophagie beteiligt sind, sodass ein leistungsfähiges Mikroskop stündlich Bilder aufnehmen konnte, während Nährstoffe entzogen und dann wiedergegeben wurden. Statt diese Bilder manuell zu sortieren, trainierte das Team Deep‑Learning‑Algorithmen darauf, allein anhand von Bildmerkmalen zu erkennen, wann eine Zelle sich in einem autophagischen Zustand befindet, unabhängig von menschlicher Beurteilung. So entstanden präzise zeitliche Verläufe der Autophagieaktivität für nahezu das gesamte Hefagenom, die zeigten, wie schnell und wie stark jeder Mutant auf Nährstoffänderungen reagierte. 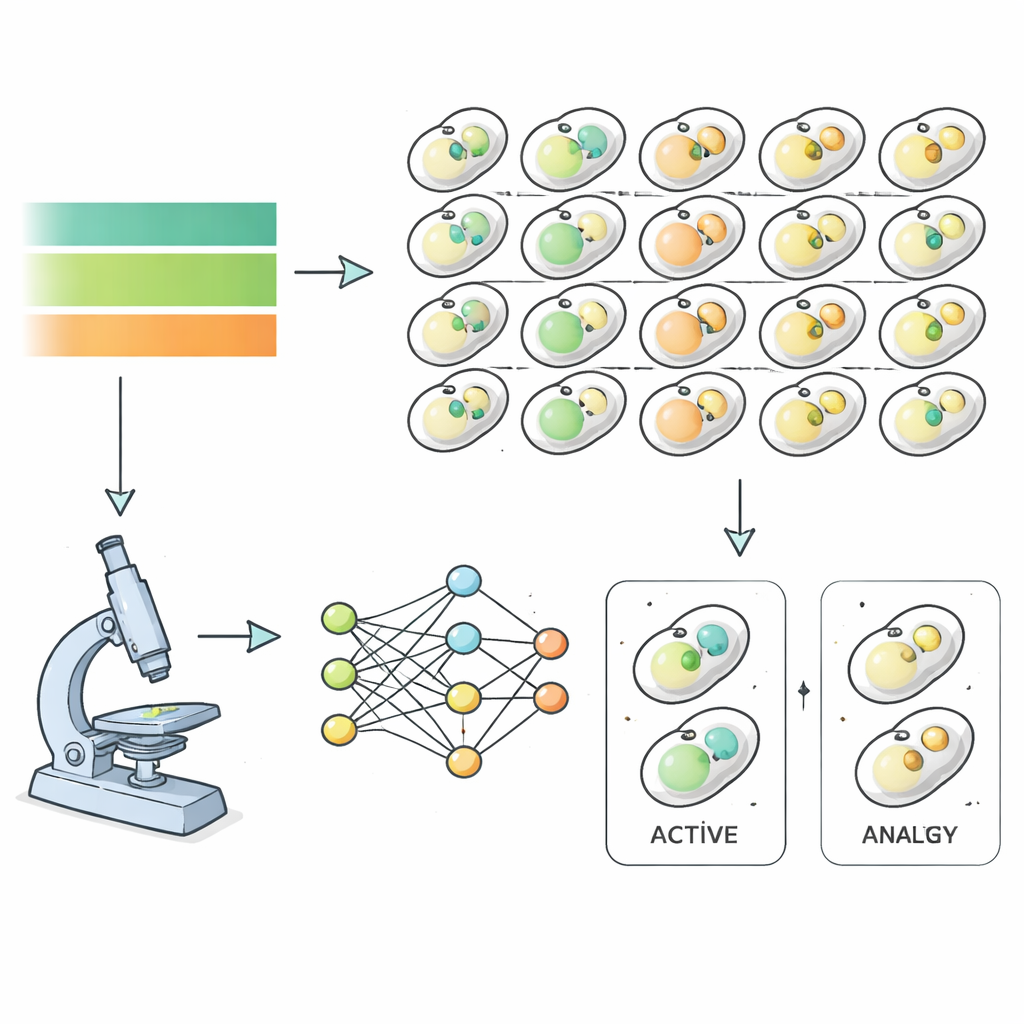
Sechs verschiedene Arten, wie Zellen Recycling fehlsteuern
Durch mathematisches Anpassen dieser Zeitverläufe gewannen die Autoren detaillierte „kinetische Fingerabdrücke“ für jeden Mutanten — wie schnell Autophagie anspringt, wie lange sie auf einem hohen Niveau bleibt und wie scharf sie abgeschaltet wird. Die Gruppierung dieser Signaturen deckte sechs breite Verhaltensklassen auf. Einige Mutanten waren „ultrasensitiv“ und reagierten sehr schnell auf Hunger und Nährstoffrückkehr. Andere zeigten „Hyposensitivität“ und reagierten träge. Eine „hyperaktive“ Gruppe wies ungewöhnlich hohen Basalrecycling auf, während mehrere Gruppen unterschiedliche Grade des Versagens zeigten, überhaupt eine adäquate Antwort zu erzeugen. Wichtig ist, dass bekannte Kern‑Autophagie‑Gene in die schwerwiegendsten Klassen fielen, was bestätigt, dass die Methode echte biologische Signale und nicht Messrauschen erfasst.
Eine Hierarchie der Kontrolle über Autophagie kartieren
Autophagie geschieht nicht isoliert; sie ist in die breiteren regulatorischen Netzwerke der Zelle eingebettet. Das Team überlagerte seine dynamischen Profile mit großen Karten genetischer und Protein‑Interaktionen in Hefe. Gene, deren Verlust starke Autophagiedefekte verursachte, lagen in diesen Netzwerken tendenziell nah an der bekannten „Kernmaschinerie“ der Autophagie, während subtilere Mutanten weiter entfernt waren — konsistent mit indirekterer Kontrolle. Durch die Untersuchung, welche zellulären Prozesse in jeder Verhaltensklasse angereichert waren, fanden sie, dass die Aktivierung durch Hunger stark von Wegwegen geprägt ist, die RNA, Proteinsynthese und Energiestoffwechsel steuern, während das Abschalten der Autophagie nach Nährstoffrückkehr stärker von Membranverkehr und Fusionsschritten abhängt, die Recyclingvesikel beseitigen.
Ins Detail gehen: Wie Vesikel entstehen und geräumt werden
Autophagie verläuft in zwei Hauptschritten: dem Aufbau von mit Fracht gefüllten Vesikeln und deren Fusion mit dem Recycling‑Kompartiment der Zelle zur Zersetzung. Um diese Phasen zu zerlegen, durchsuchten die Forschenden den „latenten Raum“ innerhalb ihres neuronalen Netzes — die komprimierte Repräsentation, die das Netz zur Unterscheidung von Bildern nutzt. Durch Projektion dieser internen Repräsentation auf eine zweidimensionale Karte konnten sie beobachten, wie Zellpopulationen von einer Region ohne Vesikel über eine mit vielen freien Vesikeln bis in eine Region wanderten, in der Vesikel bereits geräumt waren. Mit statistischen Vergleichen gegenüber Referenzmutanten, die in verschiedenen Stadien feststecken, quantifizierten sie für jedes Gen, ob es hauptsächlich die Vesikelbildung, die Vesikelräumung oder beides beeinflusst. Diese Analyse zeigte, dass die Kontrolle der Vesikelbildung zeitlich hochsensitiv gegenüber Stickstoffverfügbarkeit ist, während die Räumungsmaschinerie beständiger reagiert und oft die Hauptbegrenzung für den gesamten Recyclingfluss darstellt. 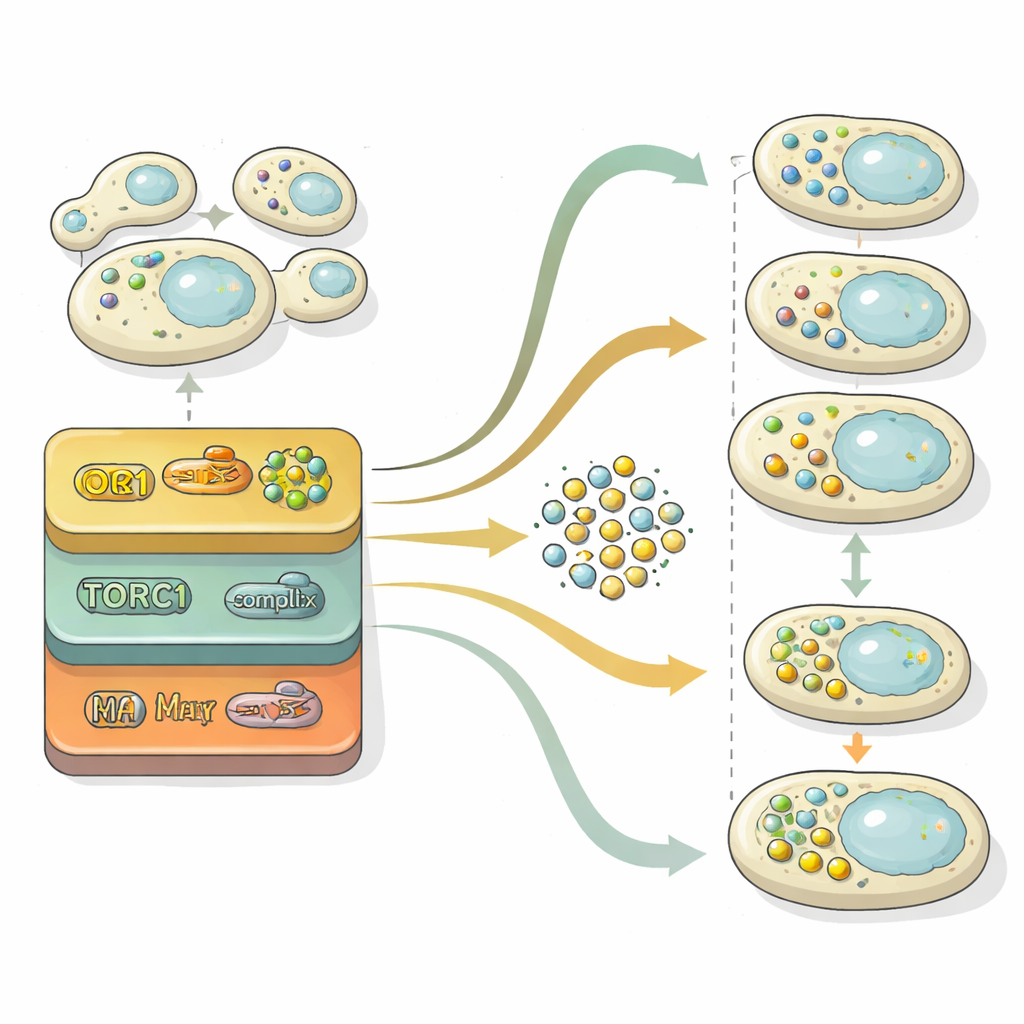
Eine versteckte Bremse des Recyclings: der retrograde Weg
Einer der eindrücklichsten Befunde betraf den sogenannten retrograden (RTG) Weg, der Signale von den Mitochondrien zum Zellkern übermittelt. Hefezellen, denen RTG‑Komponenten fehlten, produzierten selbst bei reichlich Nährstoffen zu viele Autophagosomen und hatten Schwierigkeiten, diese nach Nährstoffrückkehr zu räumen. Detaillierte Anschlussuntersuchungen zeigten, dass dieser Weg die Expression wichtiger Autophagie‑Gene steuert, insbesondere des Masterinitiators ATG1, weitgehend unabhängig vom bekannten TORC1‑Nährstoffsensor, der Ziel von Wirkstoffen wie Rapamycin ist. Effektiv wirkt RTG‑Signalisierung als zeitlich veränderliche Bremse, die unkontrollierte Autophagie unter nahrhaften Bedingungen verhindert und hilft, die Antwort zu beenden, wenn sich die Bedingungen verbessern.
Warum das für Gesundheit und Therapie wichtig ist
In der Summe liefert diese Arbeit eine genomweite, zeitaufgelöste Karte, wie Zellen Autophagie über wechselnde Nährstoffbedingungen feinabstimmen. Sie zeigt, dass Aktivierung und Abschalten keine Spiegelbilder sind: Viel mehr Gene beeinflussen, wie Recycling beginnt, als wie es endet, und das langfristige Gleichgewicht hängt stark von Vesikelräumung und Transkriptionsbremsen wie dem RTG‑Weg ab. Für die allgemein interessierte Leserschaft lautet die wesentliche Erkenntnis, dass zelluläres Selbstkannibalismus unter geschichteten, hierarchischen Kontrollen steht und dass wir diese Ebenen jetzt mit hoher Präzision kartieren können. Solche systemweiten Einsichten könnten schließlich zu nuancierteren Therapien führen, die Autophagie in bestimmten Phasen anpassen — das nützliche Recycling stärken, ohne die schädlichen Auswirkungen chronisch unkontrollierter Selbstverdauung auszulösen.
Zitation: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
Schlüsselwörter: Autophagie, Deep Learning, Hefegenetik, Nährstoffwahrnehmung, zelluläres Recycling