Clear Sky Science · de
Verfeinerte Phänotypisierung von Impfantworten enthüllt transkriptomische Determinanten der Heterogenität neutralisierender Antikörper
Warum manche Impfstoffe bei bestimmten Personen besser wirken
Wenn wir uns eine COVID-19-Impfung geben lassen, gehen wir womöglich davon aus, dass das Immunsystem aller Menschen gleich reagiert. Tatsächlich unterscheiden sich Menschen stark darin, wie schnell und wie stark sie schützende Antikörper aufbauen. In dieser Studie wurden Erwachsene nachverfolgt, die inaktivierte SARS-CoV-2-Impfstoffe erhielten, und es zeigte sich, dass Impfantworten sich in unterschiedliche Muster einordnen lassen, die jeweils von verschiedenen frühen Immunhinweisen bestimmt werden, die in Genen und Blutzellen ablesbar sind. Das Verständnis dieser Muster könnte eines Tages dabei helfen, Impfpläne so anzupassen, dass jeder den Schutz erhält, den er benötigt.
Drei Wege zum Schutz nach derselben Impfung
Die Forschenden verfolgten 73 gesunde Erwachsene, die zwei Dosen eines inaktivierten COVID-19-Impfstoffs erhielten. Sie maßen neutralisierende Antikörper — jene, die das Virus blockieren können — vor der Impfung, eine Woche nach der zweiten Dosis und etwa einen Monat später. Statt die Teilnehmenden einfach in „hohe“ und „niedrige“ Responder zu unterteilen, nutzten sie datengetriebene Methoden, um Personen nach dem Verlauf ihrer Antikörperspiegel zu gruppieren. Drei klare Muster traten hervor: eine „low-delayed“-Gruppe mit einem langsamen, mäßigen Anstieg der Antikörper; eine „rapid-stabilizing“-Gruppe, deren Antikörper schnell anstiegen und dann ein Plateau erreichten; und eine „continuous-increase“-Gruppe, deren Antikörperspiegel kontinuierlich weiter zunahmen und die höchsten Werte erreichten. Diese Muster ließen sich nicht durch Alter, Geschlecht oder Körpergewicht erklären und nur teilweise durch die Marke des erhaltenen inaktivierten Impfstoffs.
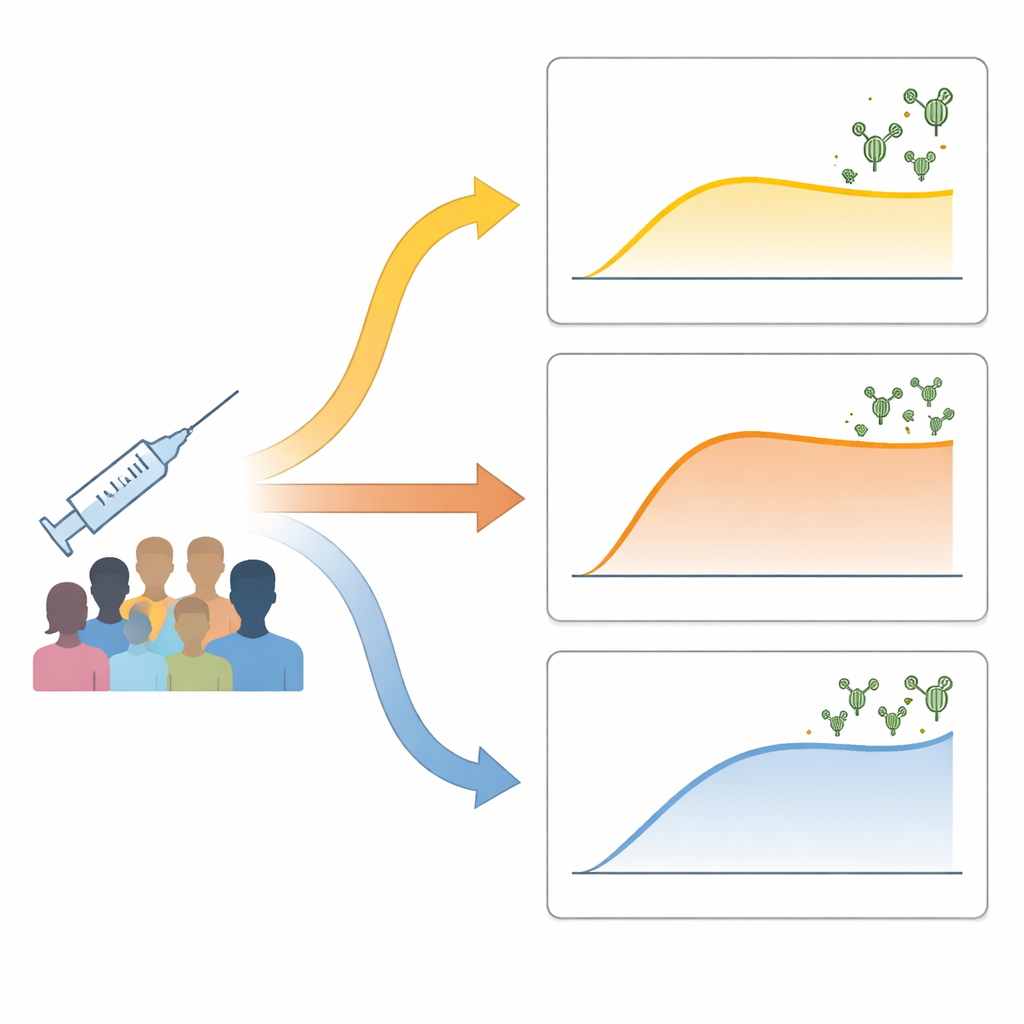
Wie frühe Immunaktivität das Ergebnis formt
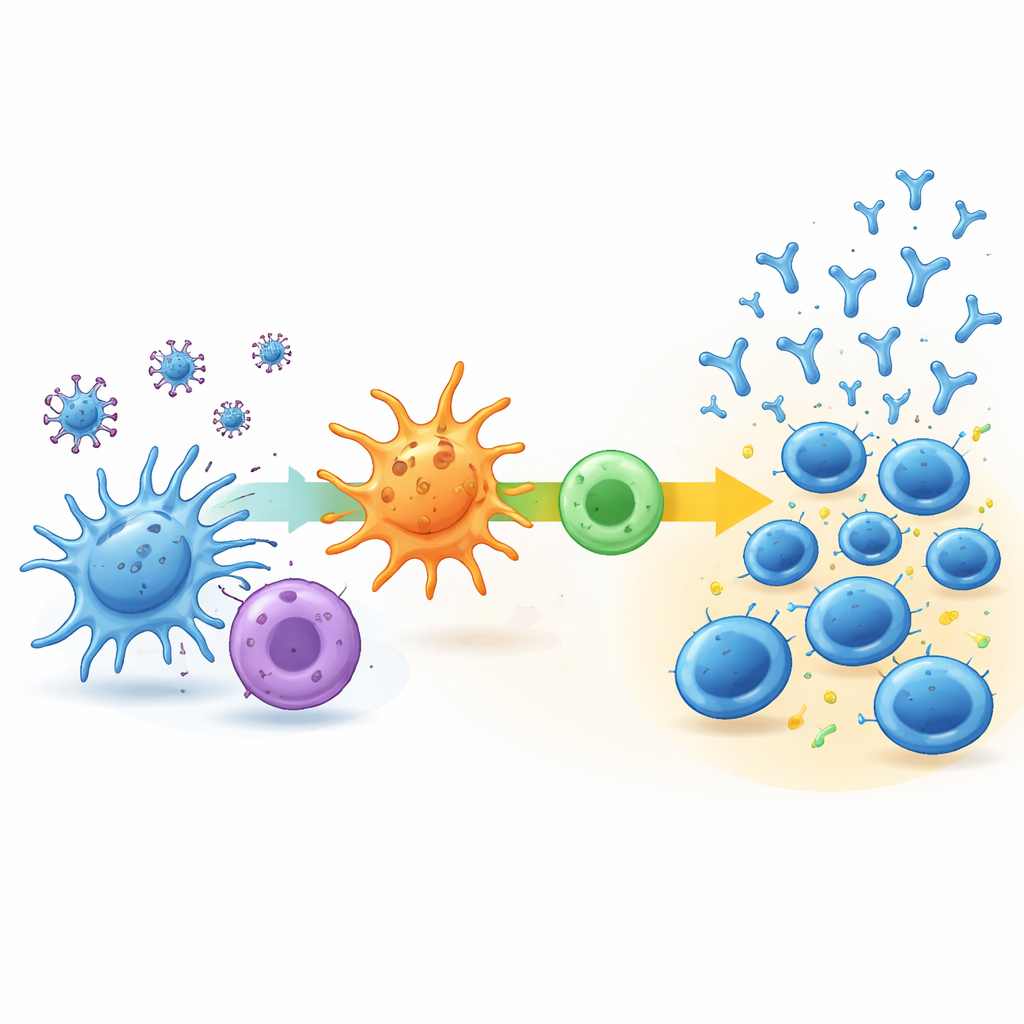
Um zu untersuchen, was diese unterschiedlichen Wege antreibt, analysierte das Team die genetische Aktivität von Immunzellen im Blut zu Beginn und eine Woche nach der zweiten Impfung. In der low-delayed-Gruppe änderte sich sehr wenig: Wichtige Immunwege schalteten kaum ein, und die Zusammensetzung der Immunzelltypen im Blut blieb größtenteils unverändert. Im Gegensatz dazu zeigten die rapid-stabilizing- und continuous-increase-Gruppen deutliche Anzeichen früher Immunaktivierung. Bei den stärksten Respondern gab es koordinierte Aktivität in Wegen, die virale Fragmente verarbeiten, sie anderen Immunzellen präsentieren und eine Form der Helfer-T‑Zell-Antwort unterstützen, die bekanntermaßen die Antikörperproduktion fördert. Diese Personen hatten zudem tendenziell mehr naive B‑Zellen und Helfer-T‑Zellen, die zum Reagieren bereitstanden, und zeigten später etwas stärkere virus-spezifische T‑Zell-Aktivität.
Verborgene Steuerungsebenen in RNA und B‑Zellen
Über einfache Genein‑/aus‑Änderungen hinaus untersuchten die Wissenschaftler feinere Regulationsebenen in der RNA, den Zwischenmolekülen zwischen DNA und Protein. In der Gruppe mit der besten Antwort zeigten Immungene, die an der Präsentation viraler Fragmente beteiligt sind, andere „Spleiß“-Muster und kürzere Schwanzregionen am Ende ihrer RNA. Diese Merkmale gelten als förderlich dafür, dass Zellen bestimmte Proteine leichter produzieren und starke Signalübertragungen aufrechterhalten können. Das Team rekonstruierte außerdem das Repertoire der B‑Zell‑Rezeptoren — die einzigartigen Antennen auf antikörperproduzierenden Zellen — aus denselben Blutproben. Während die Gesamtdiversität in den Gruppen ähnlich war, nutzte jedes Antwortmuster leicht unterschiedliche Kombinationen und Formen dieser Rezeptoren, und die stärksten Respondern favorisierten Rezeptortypen, die zuvor mit besonders wirksamen Antikörpern gegen das Coronavirus-Spike-Protein in Verbindung gebracht worden waren.
Wahrscheinliche Low‑Responder vor der Impfung erkennen
Da Personen der low-delayed‑Gruppe nach einem Standardimpfregime möglicherweise weniger geschützt sind, fragten die Forschenden, ob man sie im Voraus identifizieren könnte. Sie konzentrierten sich auf eine kleine Anzahl von Genen, die sich vor der Impfung schwach zwischen den schwächsten und stärksten Respondern unterschieden. Mit Hilfe maschineller Lernverfahren bauten sie ein Modell auf Basis der Aktivität von nur acht Genen, gemessen vor der Impfung. Dieses Modell konnte in ihrem Datensatz low-delayed‑Responder mit hoher Genauigkeit unterscheiden, wobei zwei Gene, die an grundlegender Zell‑Signalübertragung und Entzündungsprozessen beteiligt sind, den größten Beitrag zur Vorhersage leisteten. Obwohl diese Ergebnisse in größeren und vielfältigeren Kohorten validiert werden müssen, deutet das darauf hin, dass ein einfacher Bluttest eines Tages individuellere Impfpläne ermöglichen könnte.
Was das für zukünftige Impfstoffe bedeutet
Insgesamt zeigt diese Studie, dass Menschen nicht einfach „starke“ oder „schwache“ Antikörperantworten entwickeln; sie folgen unterschiedlichen zeitlichen Verläufen, die durch frühe, schwer sichtbare Immunereignisse geprägt werden. Die am besten Geschützten aktivieren koordinierte Netzwerke von Genen und Zellen, die ihnen helfen, den Impfstoff schnell zu erkennen und langlebige Antikörper aufzubauen, während Low‑Responder eine gedämpfte frühe Reaktion zeigen. Indem diese internen Unterschiede kartiert und Werkzeuge zur Vorhersage schlechterer Antworten entwickelt werden, legt die Arbeit das Fundament für personalisierte Impfstrategien — etwa frühere Auffrischungen oder alternative Formulierungen für Risikogruppen — damit der Nutzen von Impfungen gerechter verteilt wird.
Zitation: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
Schlüsselwörter: Impfantworten, neutralisierende Antikörper, COVID-19-Impfung, Immunheterogenität, personalisierte Impfstoffe