Clear Sky Science · de
Immunogenität und Schutz von oktavalenten Influenza‑Impfstoffkandidaten mit adjuvantierten Proteinen oder mRNA‑LNPs in naiven Mäusen
Warum ein besserer Grippeimpfstoff wichtig ist
Saisonale Grippeimpfstoffe retten viele Leben, ihre Schutzwirkung schwankt jedoch von Jahr zu Jahr stark. Ein Grund ist, dass gegenwärtige Impfstoffe hauptsächlich das Immunsystem darauf trainieren, ein einzelnes Virusprotein zu erkennen, sodass andere nützliche Zielstrukturen weniger genutzt werden. Diese Studie an Mäusen untersucht nächst‑Generation‑Grippeimpfstoffe, die das Immunsystem gleichzeitig auf zwei Schlüsselformationen des Virus sensibilisieren, und vergleicht einen traditionellen proteinbasierten Ansatz mit einer neueren mRNA‑Technologie, ähnlich der in den jüngsten COVID‑19‑Impfstoffen.
Zwei Ziele statt eines
Die heutigen Grippeimpfstoffe konzentrieren sich hauptsächlich auf das Hämagglutinin (HA), ein Protein, das dem Virus hilft, an unsere Zellen anzudocken. Die Forschenden fügten ein zweites Virusprotein hinzu, die Neuraminidase (NA), die dem Virus hilft, sich aus infizierten Zellen zu befreien und sich zu verbreiten. Durch die Kombination von vier HA‑Varianten und vier NA‑Varianten aus den Saisonstrainen 2018–2019 entwickelten sie einen „oktavalenten“ Impfstoff, der zwei Typen von Influenza A und zwei Linien von Influenza B abdecken soll. Diese acht Komponenten verpackten sie auf zwei verschiedene Weisen: als gereinigte Proteine gemischt mit einem immunverstärkenden Wirkstoff und als mRNA, eingehüllt in winzige Lipidblasen (mRNA‑LNPs), die die körpereigenen Zellen anregen, die Virusproteine herzustellen.
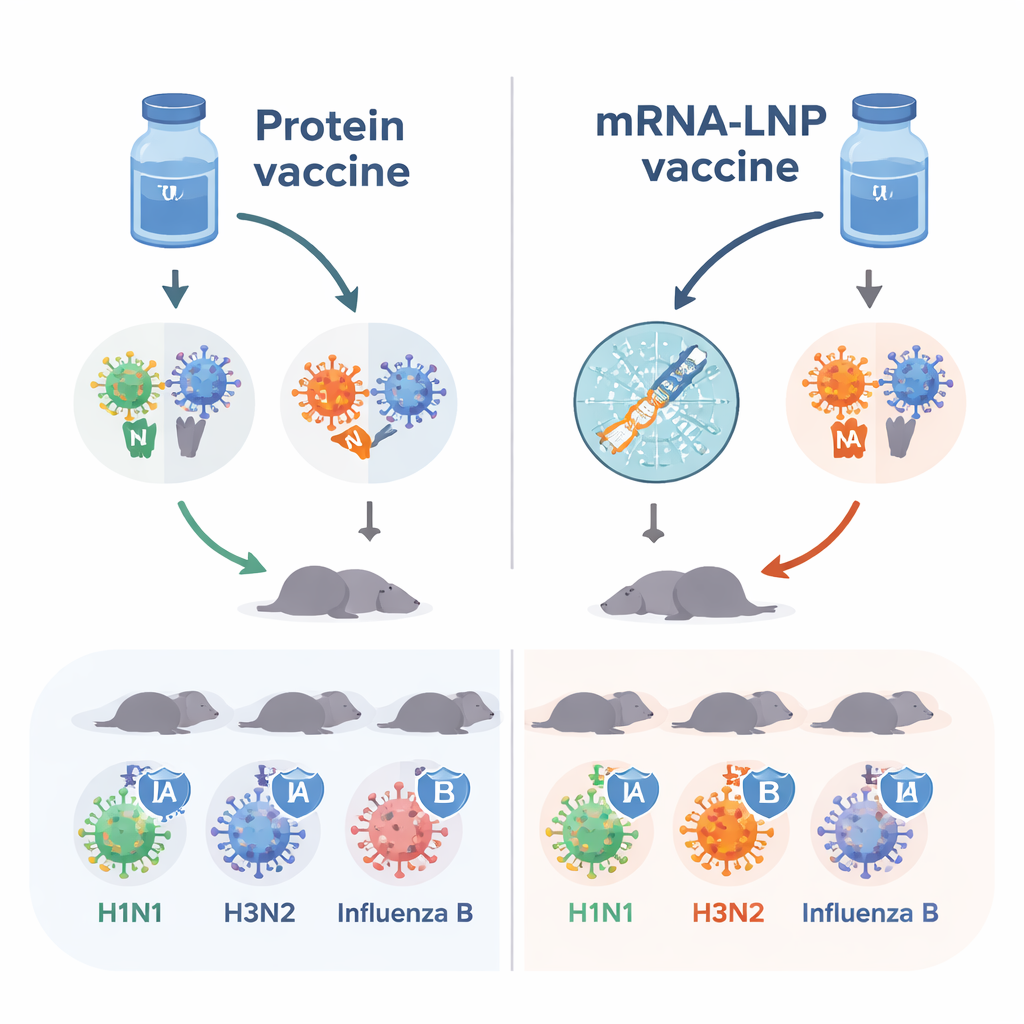
Stärkere Antikörperantworten mit mRNA
Naive Mäuse – Tiere, die noch nie mit Grippeviren oder Impfungen in Kontakt gewesen waren – erhielten zwei Dosen entweder des Proteinimpfstoffs oder der mRNA‑LNP‑Variante. Das Team maß Antikörper im Blut, die HA und NA erkennen. Beide Impfstoffe erzeugten nützliche Antworten, doch die mRNA‑LNP‑Injektionen produzierten durchweg höhere Antikörperspiegel gegen die meisten HA‑ und NA‑Komponenten. Insbesondere Antikörper, die die Aktivität der NA blockieren und bekanntermaßen unabhängig zum Schutz beitragen, waren nach mRNA‑LNP‑Impfung allgemein stärker. Diese Befunde deuten darauf hin, dass im Tiermodell die mRNA‑Plattform die gleichen Virusziele für das Immunsystem sichtbarer macht.
Schutz gegen passende und aktuelle Stämme
Der eigentliche Prüfstein war, ob diese Impfstoffe Mäuse vor schwerer Krankheit bewahren können. In dosisangepasster Form, die einer menschlichen Grippeimpfung entspricht, schützten beide Impfstoffformate die Tiere vollständig vor tödlicher Infektion mit H1N1‑ und Influenza‑B‑Viren, die eng mit den Impfkomponenten übereinstimmten, sowie vor gentechnisch hergestellten H3N2‑ähnlichen Viren, die verwendet wurden, wenn gängige menschliche Stämme Mäuse nicht krank machen. Geimpfte Mäuse hielten ihr Körpergewicht und überlebten, während ungeimpfte Tiere Gewicht verloren und oft verstarben. Für diese eng verwandten Stämme schnitten die traditionellen Proteinimpfstoffe und die mRNA‑LNP‑Impfstoffe hinsichtlich Überleben ähnlich ab, obwohl sich die Antikörperprofile unterschieden.
Vorteil gegenüber älteren, nicht passenden Grippeviren
Wo die mRNA‑LNP‑Strategie hervortrat, war in härteren „Mismatch“-Tests. Die Forschenden setzten geimpfte Mäuse historischen H3N2‑Stämmen aus den Jahren 1968, 1975 und 1982 aus – Viren, die sich von den modernen Stämmen unterscheiden, die der Impfstoff nachbilden sollte. Alle ungeimpften Mäuse und die meisten Tiere, die Proteinimpfstoffe erhielten, starben, doch jede Maus, die den oktavalenten mRNA‑LNP‑Impfstoff erhalten hatte, überlebte, obwohl sie weiterhin Krankheitszeichen zeigte. Dieser Überlebensvorteil hielt fast ein Jahr nach der Impfung an und deutet auf langanhaltenden Schutz hin. Als das Team Serum aus geimpften Tieren in ungeimpfte Mäuse übertrug, schützte nur Serum mit Antikörpern, die durch mRNA‑LNP‑Impfstoffe gegen HA ausgelöst wurden, vor dem Tod durch ein nicht passendes Virus, was auf querspezifische HA‑Antikörper als Schlüsselfaktor hinweist.
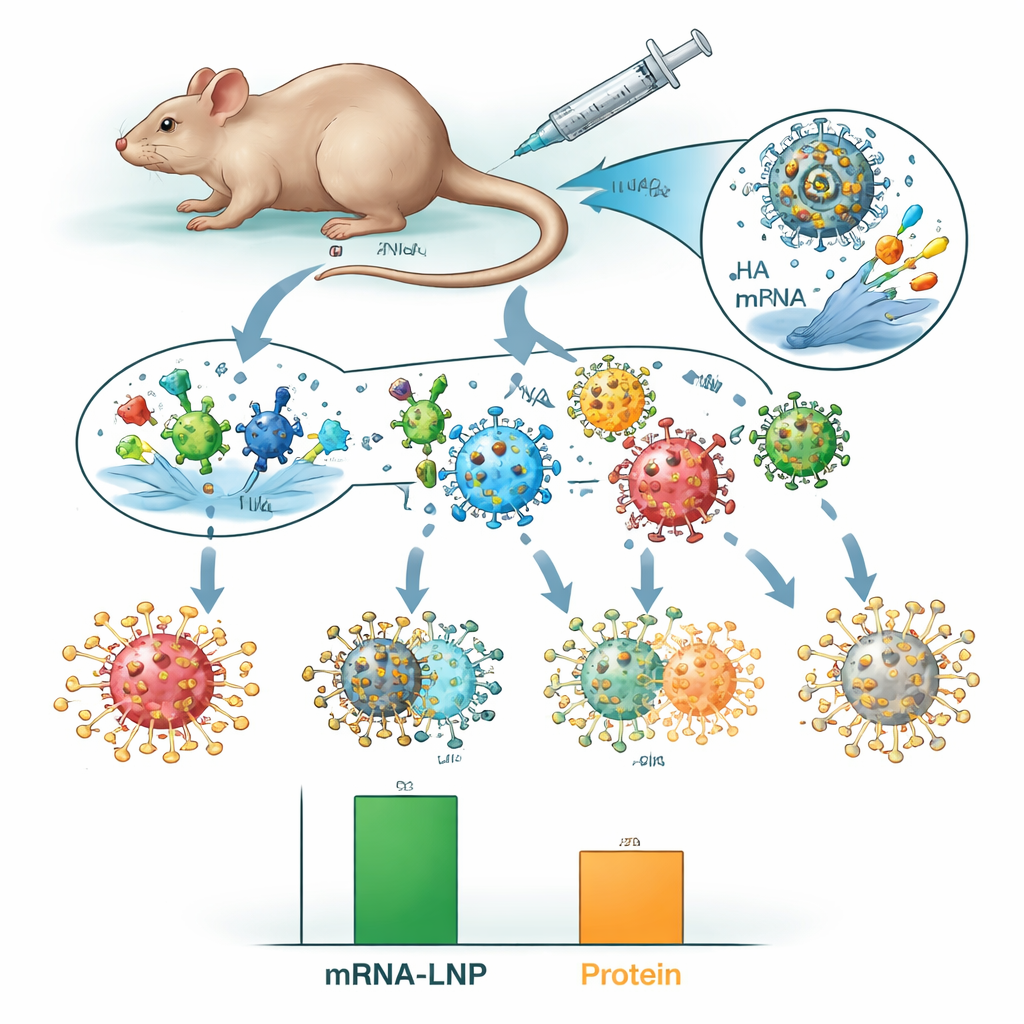
Was das für künftige Grippeimpfungen bedeutet
Laienfähig zusammengefasst heißt das: Beide Impfstofftypen schützten Mäuse vor den Grippestämmen, auf die sie ausgelegt waren, doch die mRNA‑LNP‑Variante bot zudem breiteren und länger anhaltenden Schutz gegen ältere, nicht mehr aktuelle Viren. Durch die Kombination beider wichtigen Oberflächenproteine des Grippevirus und die Präsentation als mRNA könnte diese Strategie helfen, die Unterschiede zwischen guten und schlechten Grippesaisons zu verringern. Während Ergebnisse aus Mausstudien keinen Erfolg beim Menschen garantieren und stärkere Adjuvantien Proteinimpfstoffe vielleicht weiter verbessern könnten, stützt die Arbeit die Idee, dass multikomponentige mRNA‑Grippeimpfstoffe eines Tages einen zuverlässigeren Schutz gegen ein breiteres Spektrum zirkulierender und neu auftretender Influenzastämme bieten könnten.
Zitation: Catani, J.P.P., Smet, A., Ysenbaert, T. et al. Immunogenicity and protection of octavalent influenza vaccine candidates using adjuvanted proteins or mRNA-LNPs in naïve mice. npj Vaccines 11, 57 (2026). https://doi.org/10.1038/s41541-026-01378-z
Schlüsselwörter: Influenza‑Impfstoff, mRNA‑LNP, Hämagglutinin, Neuraminidase, Querschutz