Clear Sky Science · de
Antigen‑Kreuzpräsentation verstärkendes Krebsimpfstoff‑Adjuvans für T‑Zell‑Expansion und Synergie mit Anti‑PD‑1
Das Immunsystem in einen präzisen Tumorkämpfer verwandeln
Krebsimpfstoffe werden oft als Mittel beschrieben, das Immunsystem zu lehren, Tumore zu erkennen und zu zerstören, doch in der Praxis haben sie dieses Versprechen selten vollständig eingelöst. Diese Studie untersucht einen neuen Weg, solche Impfstoffe zu „verstärken“, damit sie stärkere, langlebigere zytotoxische T‑Zellen erzeugen und besser mit beliebten Immuntherapeutika wie Anti‑PD‑1 zusammenwirken. Für Leser, die sich dafür interessieren, wie zukünftige Krebsbehandlungen Biologika, Impfstoffe und Immunengineering kombinieren könnten, bietet diese Arbeit einen Einblick, wie die nächste Generation hochspezifischer Immuntherapien aussehen könnte.
Warum Krebsimpfstoffe bessere Unterstützung brauchen
Therapeutische Krebsimpfstoffe zielen nicht auf Prävention, sondern darauf, Menschen mit bestehenden Tumoren zu behandeln, indem sie starke, tumorspezifische Immunantworten hervorrufen. Die Schlüsselfiguren sind CD8‑„Killer“‑T‑Zellen, die Krebszellen erkennen und zerstören können, wenn diese charakteristische Antigene präsentieren. Leider sind Tumorantigene schwach stimulierend, weil sie meist wie veränderte Versionen körpereigener Proteine aussehen. Eine anhaltende Exposition während der Tumorentwicklung kann T‑Zellen zudem erschöpfen oder tolerisieren und so die Wirkung von Impfstoffen abschwächen. Um das zu überwinden, müssen Impfstoffe mit Adjuvantien kombiniert werden – Hilfsbestandteilen, die das angeborene Immunsystem wecken, die Antigenpräsentation verbessern und einen großen, widerstandsfähigen Pool tumorspezifischer T‑Zellen aufbauen.
Ein hybrider Immunverstärker aus zwei starken Signalen
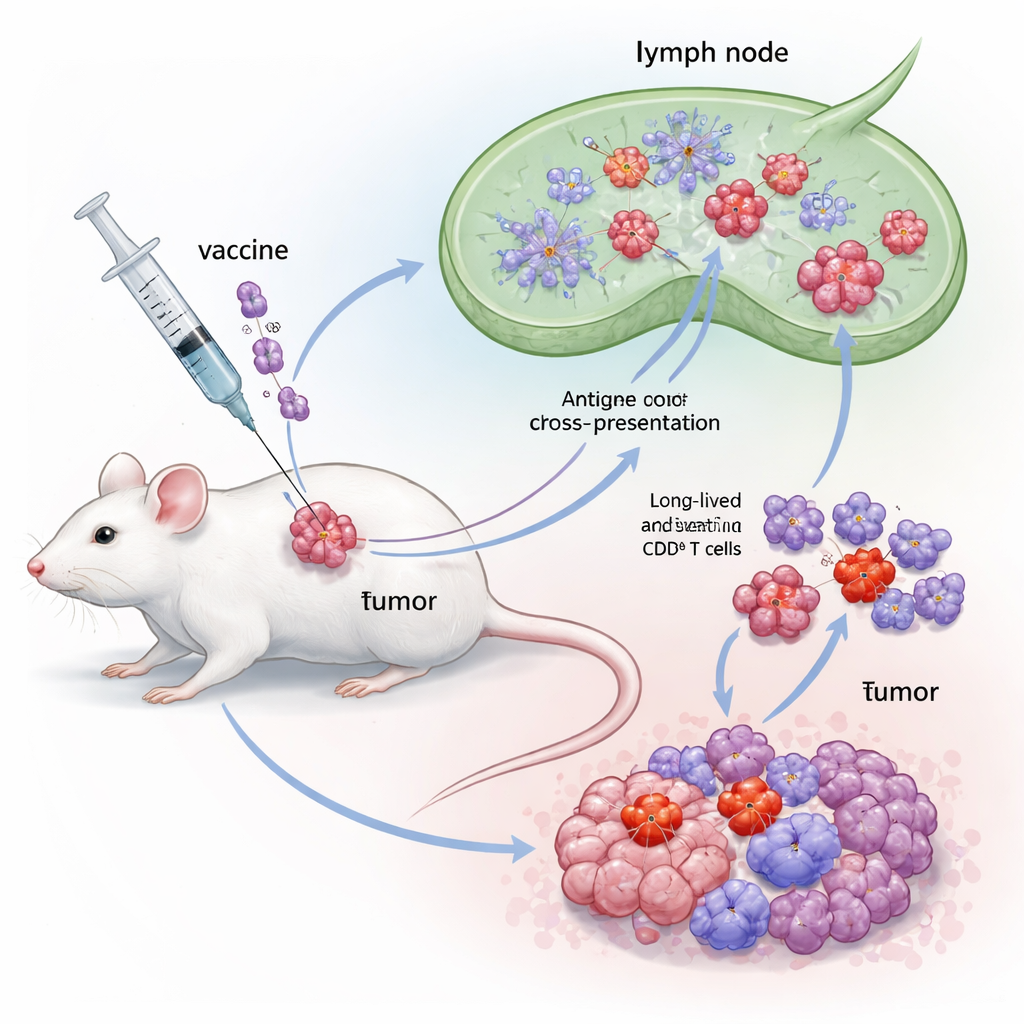
Die Forschenden entwickelten ein hybrides Adjuvans namens Flt3L‑FlaB, kurz FB, indem sie zwei immunstimulierende Moleküle zu einem einzigen Protein verbanden. Die eine Hälfte, Flt3L, ist ein natürlicher Wachstumsfaktor, der eine spezialisierte Gruppe von dendritischen Zellen, die als cDC1 bekannt sind, vermehrt. Diese Zellen sind besonders gut in der „Kreuzpräsentation“ – sie nehmen Tumorfragmenten auf und präsentieren sie CD8‑T‑Zellen auf eine Weise, die starke Antworten auslöst. Die andere Hälfte, FlaB, ist ein bakterielles Flagellin‑Fragment, das einen angeborenen Sensor namens TLR5 aktiviert und als potentes Gefahrensignal fungiert. Durch die Verbindung beider Komponenten wollten die Autoren sowohl cDC1 vermehren als auch in einen hochaktiven Zustand versetzen, wodurch die Präsentation von Tumorantigenen an T‑Zellen verbessert und die Dauer dieser Stimulation verlängert wird.
Erprobung des neuen Adjuvans in Tumormodellen
Um FB zu testen, verwendete das Team ein etabliertes Maus‑Tumormodell, das auf Zellen basiert, welche mit krebsauslösenden Proteinen des humanen Papillomvirus (HPV) ausgestattet wurden. Die Mäuse erhielten zunächst ein kleines Tumorimplantat und anschließend einen therapeutischen Impfstoff mit einem HPV‑E7‑Antigen, kombiniert entweder mit Flt3L allein, FlaB allein oder der neuen FB‑Fusion. Alle Impfungen wurden in Tumornähe verabreicht. Während jedes einzelne Adjuvans das Tumorwachstum etwas verlangsamte, stach der FB‑basierte Impfstoff hervor: Er verzögerte das Tumorwachstum deutlich stärker, verlängerte das Überleben signifikant und ließ einen bemerkenswerten Anteil der Mäuse vollständig tumorfrei zurück. Immunanalysen zeigten, dass die FB‑Impfung ungewöhnlich starke E7‑spezifische CD8‑Antworten im Blut, in Lymphknoten und Milz erzeugte, mit hohen Interferon‑Gamma‑Spiegeln und robuster T‑Zell‑Proliferation – ein Beleg dafür, dass die Fusion mehr bewirkte als nur die addierten Effekte ihrer beiden Teile.
Aufbau dauerhafter immunologischer Erinnerung und ein besserer Partner für Anti‑PD‑1
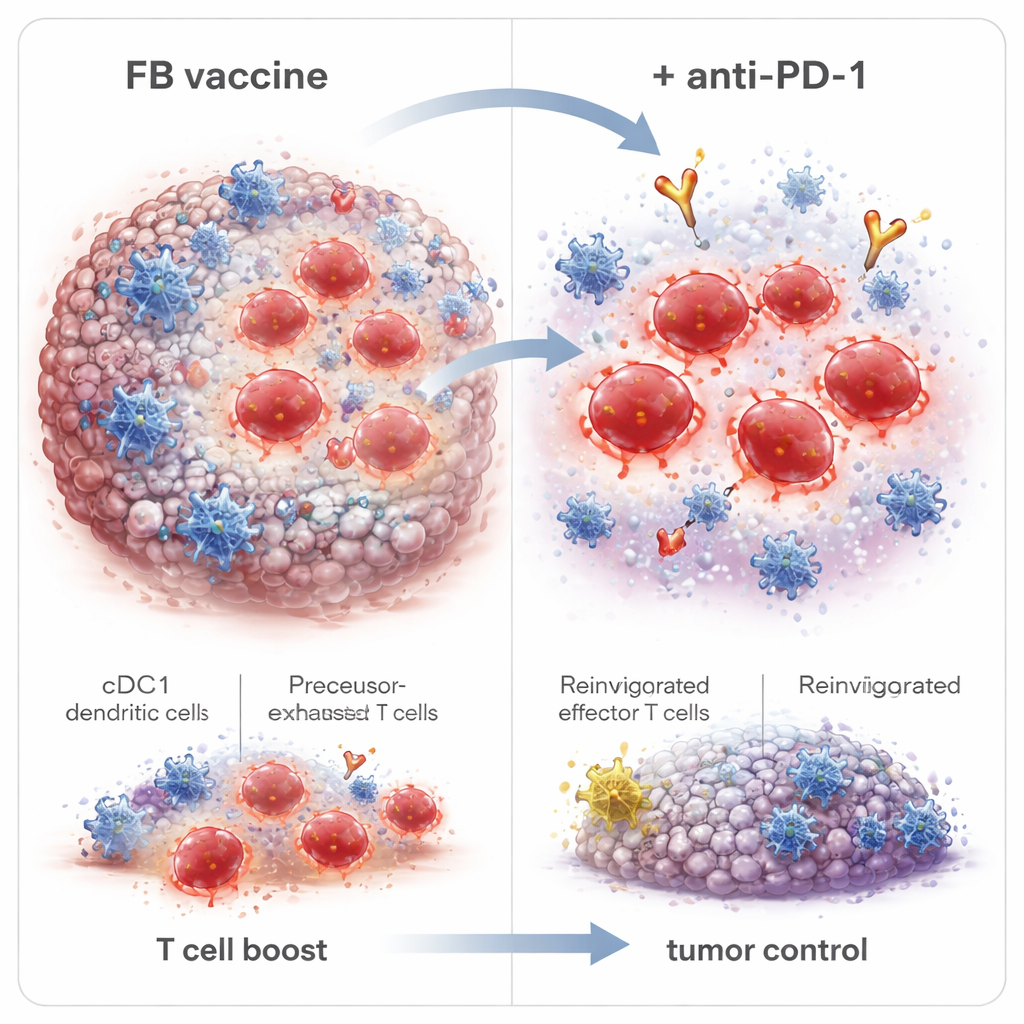
Bei genauerer Betrachtung fanden die Wissenschaftler, dass FB nicht nur die Anzahl der CD8‑T‑Zellen veränderte, sondern auch deren Qualitäten. Es förderte kurzlebige Effektorzellen, die Tumore sofort angreifen, ebenso wie Gedächtnisvorläufer und stamm‑ähnliche Gedächtniszellen, die bestehen bleiben und später erneut reagieren können. Wichtig ist, dass FB auch eine Gruppe innerhalb der Tumore erweiterte, die als prä‑erschöpfte T‑Zellen (Tpex) bezeichnet wird – Zellen, die an der Grenze zwischen Erschöpfung und voller Funktionalität stehen und besonders empfindlich auf Anti‑PD‑1‑Medikamente reagieren. Wenn nachträglich tumorfreie Überlebende lange nach der Impfung mit höheren Dosen von Tumorzellen herausgefordert wurden, verhinderten die meisten ein Nachwachsen und zeigten damit eine langlebige Immunerinnerung. Das Blockieren des Austritts von Immunzellen aus den Lymphknoten beseitigte FBs Vorteile, was darauf hindeutet, dass tumorvernichtende T‑Zellen in diesen Knoten von cDC1 antrainiert und anschließend in den Tumor migriert wurden.
Stärker zusammen: Impfstoffe plus Checkpoint‑Blockade
Da Anti‑PD‑1‑Therapie am besten wirkt, wenn bereits ein Pool an reaktionsfähigen T‑Zellen vorhanden ist, kombinierten die Forschenden die FB‑adjuvantierte Impfung mit einem Anti‑PD‑1‑Antikörper. Im HPV‑Tumormodell verlangsamte die zusätzliche Anti‑PD‑1‑Behandlung das Tumorwachstum weiter, erhöhte die Zahl der Mäuse, die ihren Krebs vollständig beseitigten, und bot vollständigen Schutz gegen eine sehr hohe Dosis bei Tumornachherausforderung. Die zeitliche Abstimmung war wichtig: Das Beginnen der Anti‑PD‑1‑Behandlung nach der zweiten statt der ersten Impfdosis verbesserte die vollständige Tumorbeseitigung leicht, was mit dem Warten übereinstimmt, bis sich Tpex‑Zellen ausreichend vermehrt hatten. Das FB‑Adjuvans verbesserte außerdem die Reaktionen auf peptidbasierte Impfstoffe, einschließlich tumorspezifischer Neoantigene in einem Dickdarmkrebsmodell, was darauf hindeutet, dass diese Strategie über HPV‑verwandte Erkrankungen hinaus breit anwendbar sein könnte.
Was das für die zukünftige Krebsversorgung bedeuten könnte
Für Nicht‑Fachleute ist die Kernbotschaft, dass diese Arbeit verfeinert, wie man das Immunsystem „lehrt“, Krebs zu bekämpfen. Durch die Kombination eines dendritischen Zell‑Wachstumsfaktors mit einem starken Gefahrensignal in einem einzigen, stabilen Protein schafft das FB‑Adjuvans mehr der richtigen antigenpräsentierenden Zellen, hilft ihnen, Tumorantigene wirksamer zu präsentieren, und formt eine Population von Killer‑T‑Zellen, die sowohl jetzt kraftvoll sind als auch bereit sind, auf spätere Checkpoint‑Therapien zu reagieren. Obwohl diese Ergebnisse an Mäusen gewonnen wurden und noch viele Schritte bis zur Anwendung beim Menschen nötig sind, skizziert die Studie eine klare Roadmap: Schlaue Adjuvantien, die Kreuzpräsentation und T‑Zell‑Stammigkeit orchestrieren, könnten therapeutische Krebsimpfstoffe zu deutlich stärkeren Partnern für Medikamente wie Anti‑PD‑1 machen und so zu tieferer, länger anhaltender Tumorkontrolle bei Patienten führen.
Zitation: Dang, G.C., Loeurng, V., Pa, P. et al. Antigen cross-presentation potentiating cancer vaccine adjuvant for T cell expansion and synergy with anti-PD-1. npj Vaccines 11, 56 (2026). https://doi.org/10.1038/s41541-026-01376-1
Schlüsselwörter: Krebsimpfstoffe, Immuntherapie, Dendritische Zellen, PD‑1‑Blockade, HPV‑verwandte Tumore