Clear Sky Science · de
Universelles Breitband-Schleimhautvakzin-Design für humane Coronaviren inspiriert von künstlichen Antikörpern
Warum ein besserer Coronavirus-Impfstoff weiterhin wichtig ist
Auch wenn COVID-19 sich zunehmend zu einer saisonalen Infektion entwickelt, tauchen weiterhin Wellen neuer Varianten auf, und mehrere andere humane Coronaviren verursachen noch immer schwere Erkrankungen. Aktuelle Impfstoffe verhindern in der Regel schwere Verläufe gut, sind aber weniger effektiv darin, Infektion und Transmission zu blockieren — besonders in Nase und Rachen, wo diese Viren zuerst Fuß fassen. Diese Studie beschreibt eine neue Art von intranasalem Impfstoff, inspiriert von konstruierten Antikörpern, der darauf abzielt, einen langanhaltenden, breiten Schutz gegen viele Coronaviren an der mukosalen Frontlinie des Körpers zu bieten.
Aufbau eines intelligenteren Impfstoffgerüsts
Die Forschenden begannen mit einem bekannten Molekül: humanem IgG1, dem wichtigsten Antikörpertyp, der in vielen zugelassenen Antikörpermedikamenten verwendet wird. Sie entwarfen die schwere Kette so um, dass sie als flexibles "Gerüst" zur Präsentation von Rezeptorbindungsdomänen (RBDs) des Coronavirus-Spike-Proteins dienen kann — den Teilen, mit denen das Virus an unsere Zellen andockt. Durch das Entfernen der üblichen leichten Kette und das Einbringen spezifischer Mutationen verringerten sie die Bindung an Immunrezeptoren, die mit Nebenwirkungen wie Zytokinstürmen verbunden sind, und verstärkten gleichzeitig die Bindung an den neonatalen Fc-Rezeptor (FcRn). FcRn ist auf mukosalen Oberflächen reichlich vorhanden und hilft, Antikörper über die Barriere zu transportieren und ihre Verweildauer zu erhöhen. Auf diesem optimierten Rückgrat befestigte das Team ein, zwei, drei oder vier verschiedene RBDs aus SARS, MERS, saisonalen Coronaviren und mehreren SARS‑CoV‑2-Varianten, einschließlich Omicron-Linien, und schuf so mono-, bi-, tri- und tetravalente Impfstoffkandidaten.
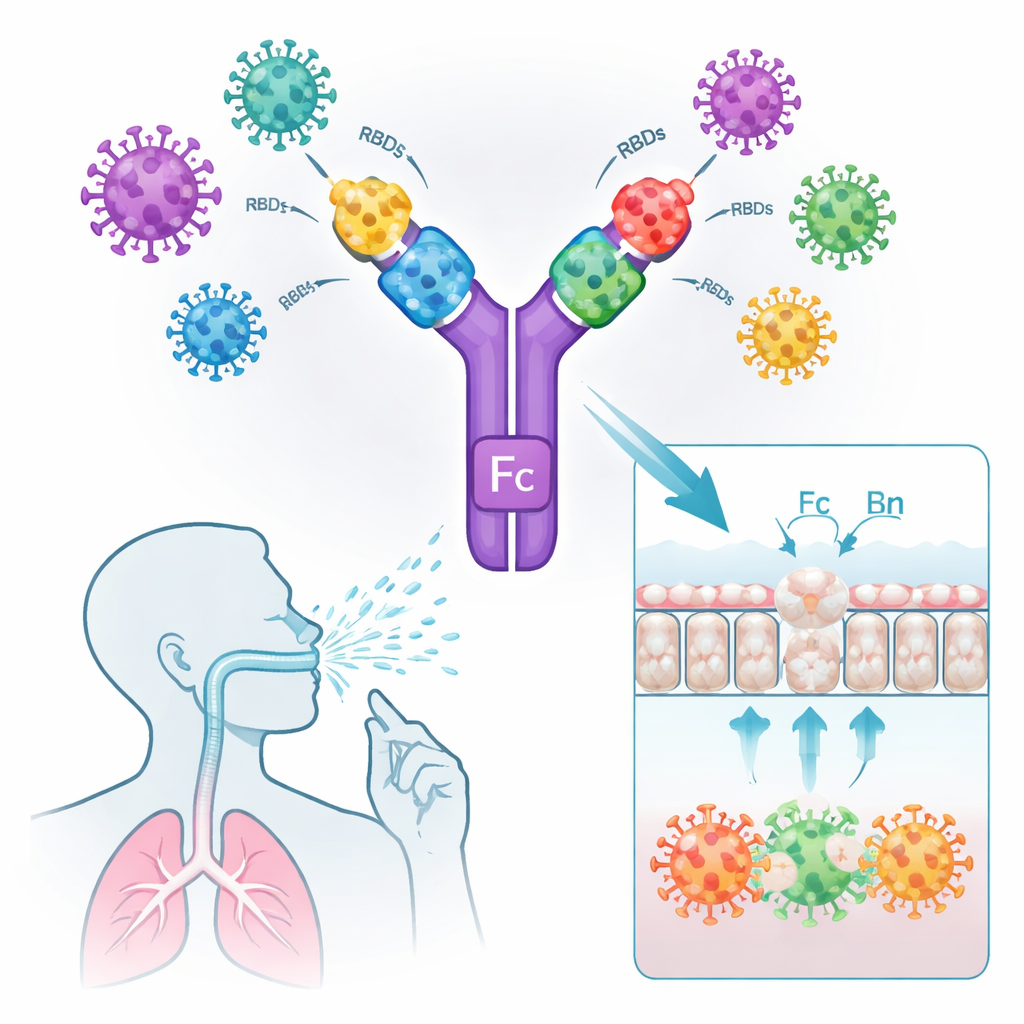
Überquerung der Schleimhautbarriere und Aktivierung lokaler Abwehr
Damit ein Nasenspray wirkt, müssen die Impfstoffantigene das Atemwegs-Epithel erreichen, dort verweilen und effizient von Immunzellen erkannt werden. In Zellkultursystemen banden die Fc-tragenden Konstrukte sowohl stark an ACE2 (den Eintrittsrezeptor von SARS‑CoV‑2) als auch an humanes oder murines FcRn und wurden aktiv durch eine Schicht mukosaler Zellen transportiert. Ein ähnliches RBD-Dimer ohne Fc‑Teil scheiterte an diesem Transport. Als fluoreszenzmarkierte Versionen der Impfstoffe in die Nasen von Mäusen verabreicht wurden, blieben die Fc‑enthaltenden Antigene stundenlang in der Lungenmukosa, während das nackte RBD-Dimer schnell verschwand. Die Mikroskopie zeigte, dass die Fc-modifizierten Impfstoffe antigenpräsentierende Zellen direkt unter der Schleimhaut anzogen und aktivierten, erkennbar an höheren Werten des Immunmarkers CD80 und der Kokolokalisation mit FcRn.
Stärkung von Antikörpern und T-Zellen dort, wo sie gebraucht werden
Das Team verglich anschließend die Immunantworten nach intramuskulärer Injektion mit denen nach intranasaler Verabreichung in Mäusen. Über mehrere Formulierungen hinweg lösten die Fc-basierten Impfstoffe sehr hohe Spiegel von IgG-Antikörpern im Blut gegen sowohl den ursprünglichen SARS‑CoV‑2-Stamm als auch gegen Omicron XBB.1.5 aus. Intranasale Gabe stach vor allem in Kombination mit einem modernen STING-Agonisten-Adjuvans (CF501) hervor, weil sie starke IgA-Antworten nicht nur im Blut, sondern auch in Nasensekreten und Lungenlavaten erzeugte — genau dort, wo mukosaler Schutz am wichtigsten ist. Die Fc-enthaltenden Konstrukte förderten außerdem stärkere zelluläre Reaktionen als nackte RBD-Dimere und erweiterten Helfer-T-Zellen, Killer-T-Zellen und langlebige gewebeansässige Gedächtnis-T-Zellen in der Lunge. Diese Zelltypen gelten als entscheidend für die Beseitigung respiratorischer Viren und die Verhinderung der Ausbreitung auf empfindliche Organe wie das Gehirn.
Breiter Schutz gegen viele Varianten und Spezies
Ein zentraler Test war, ob ein bivalenter Impfstoff, der RBDs des Prototyp-Virus und von Omicron XBB.1.5 kombiniert (genannt XBB.1.5 + PT‑Fc), Tiere gegen mehrere virale Herausforderungen schützen kann. In Mäusen, die humanes ACE2 exprimieren und zwei niedrige intranasale Dosen erhielten, induzierte dieser Kandidat starke neutralisierende Antikörper und schützte Tiere vollständig vor tödlicher Infektion mit sowohl dem ursprünglichen Virus als auch XBB.1.16: Geimpfte Mäuse hielten ihr Gewicht, überlebten und wiesen kein nachweisbares Virus im Gehirn, in der Lunge oder in nasalen Geweben auf, während Kontrolltiere erkrankten und starben. Derselbe Impfstoff verhinderte Krankheit und Tod auch bei Herausforderungen mit anderen wichtigen Varianten einschließlich Beta, Delta und mehreren Omicron-Unterlinien. In Hamstern, die sich gut für Transmissionsstudien eignen, hatten geimpfte Tiere nach direkter Herausforderung deutlich niedrigere Viruslasten und waren in Ko-Gehege-Experimenten weitgehend vor luftgetragener Übertragung geschützt. Antikörperspiegel und Gedächtnis-T‑Zellen blieben sowohl in Mäusen als auch in Hamstern mindestens 48 Wochen hoch, und Tiere waren fast ein Jahr nach der Impfung noch vollständig vor tödlichen Herausforderungen geschützt.
Auf dem Weg zu einem universellen Coronavirus-Nasenspray
Schließlich trieben die Forschenden die Plattform in Richtung eines wirklich universellen Designs voran. Sie mischten mehrere bivalente Konstrukte, die SARS‑CoV‑2, SARS, MERS und mehrere saisonale Coronaviren abdeckten, und bauten zudem tetravalente Moleküle, die vier verschiedene RBDs oder Spikefragmente auf einem einzigen Gerüst trugen. Diese Kombinationen erzeugten Antikörper, die ein breites Panel humaner Coronaviren erkannten und in Mäuse-Herausforderungsexperimenten die Viruslasten für mehrere Vertreter, einschließlich eines endemischen Virus (NL63), senkten. Obwohl weitergehende Tests in Modellen, die dem Menschen näher sind, und schließlich klinische Studien erforderlich sind, zeigt die Arbeit, dass ein konstruiertes Antikörper-Rückgrat diverse Coronavirus-Antigene sicher über die Nasenschleimhaut transportieren, starke lokale und systemische Immunität stimulieren und breiten, langlebigen Schutz bieten kann. Für Nichtfachleute lautet die Botschaft, dass zukünftige „universelle“ Coronavirus-Booster möglicherweise keine Injektionen mehr sind, sondern sanfte Nasensprays, die auf denselben Antikörpergerüsten basieren, die bereits in vielen Arzneimitteln als sicher erwiesen sind.
Zitation: Wu, Y., Lu, J., Fang, L. et al. Universal broad-spectrum mucosal vaccine design for human coronaviruses inspired by artificial antibodies. npj Vaccines 11, 55 (2026). https://doi.org/10.1038/s41541-026-01375-2
Schlüsselwörter: intranasaler Impfstoff, breitbandiger Coronavirus, schleimhautimmunität, künstliches Antikörpergerüst, SARS-CoV-2-Varianten