Clear Sky Science · de
Deep-Learning-Modelle identifizieren Hirnveränderungen während des Fortschreitens der Alzheimer-Krankheit
Warum es wichtig ist, Hirnveränderungen über die Zeit zu verfolgen
Die Alzheimer-Krankheit raubt Menschen schrittweise Erinnerungen und Denkvermögen, doch die Schädigung im Gehirn baut sich bereits Jahre vor dem Auftreten alltäglicher Symptome auf. Ärztinnen und Ärzte verlassen sich oft auf eine einzelne Hirnaufnahme oder einen einzelnen Testwert, um zu beurteilen, ob jemand Alzheimer hat, obwohl sich die Krankheit über die Zeit entfaltet. Diese Studie stellt eine einfache Frage mit großen Konsequenzen: Wenn wir die Hirnscans von Personen über mehrere Jahre verfolgen und ein fortgeschrittenes Computermodell aus diesen Veränderungen lernen lassen, können wir dann nicht nur Alzheimer genauer erkennen, sondern auch sehen, welche Hirnareale zuerst und am stärksten betroffen sind?
Der Verlauf des Gehirns, nicht nur ein Schnappschuss
Die Forschenden verwendeten strukturelle MRT-Aufnahmen, die die detaillierte Gehirnanatomie zeigen, von mehr als 280 älteren Erwachsenen, darunter Menschen mit Alzheimer und kognitiv normalen Vergleichspersonen. Entscheidend ist, dass jede Person drei Aufnahmen im Abstand von etwa einem Jahr hatte, so dass das Team verfolgen konnte, wie sich Hirngewebe über zwei Jahre veränderte. Statt jede Aufnahme als separates Bild zu behandeln, bauten sie ein Deep-Learning-Modell, das alle Zeitpunkte zusammen verarbeitet. Das Modell war so konzipiert, dass es auf graue Substanz — das Hirngewebe mit den Nervenzellkörpern — sowie auf weiße Substanz und Liquor achtet und lernt, wie sich Muster in diesen Geweben verändern, während die Krankheit voranschreitet.
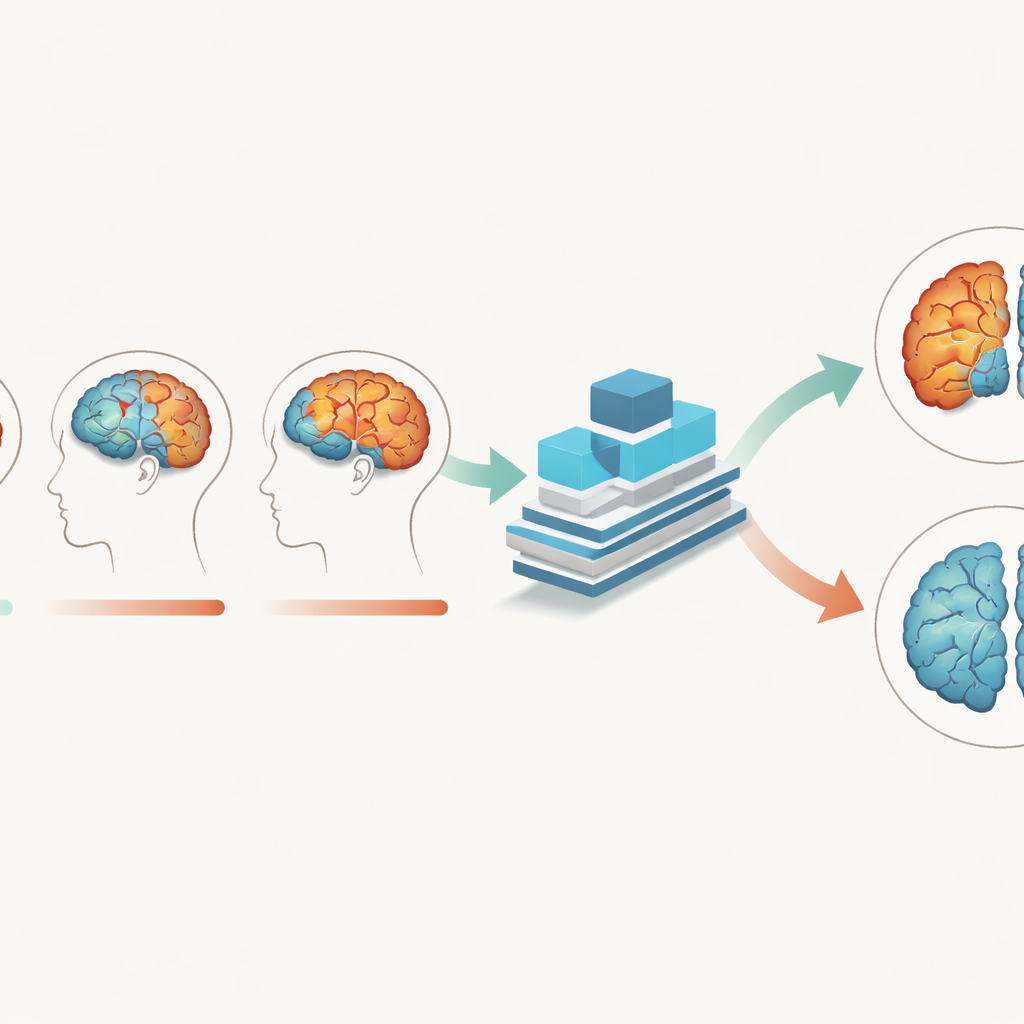
Ein Deep-Learning-Modell auf die Rhythmen des Gehirns abgestimmt
Um diese subtilen Verschiebungen zu erfassen, entwickelte das Team ein Multi-Branch Fusion Channel Attention Network, ein 3D-konvolutionales neuronales Netzwerk, das MRT-Volumina statt flacher Bilder verarbeitet. Separate Zweige behandeln unterschiedliche Gewebearten oder Zeitpunkte und verschmelzen dann ihre Informationen, während ein "Attention"-Mechanismus dem Modell hilft, sich auf die informativsten Bereiche im dreidimensionalen Raum zu konzentrieren. Hauptsächlich auf graue Substanz trainiert, lernte das Netzwerk, Alzheimer-Gehirne von normal alternen Gehirnen mit etwa 93 % Genauigkeit zu unterscheiden und erzielte in einem Datensatz perfekte Spezifität, womit es mehrere existierende KI-Methoden übertraf. Es generalisierte zudem gut auf einen unabhängigen australischen Datensatz, was darauf hindeutet, dass es sich nicht nur die Eigenheiten einer Studie merkt, sondern breitere Krankheitszeichen erfasst.
Erkennen, welche Hirnregionen das Gewicht ausmachen
Hohe Genauigkeit allein reicht in der Medizin nicht aus; Klinikerinnen und Kliniker müssen verstehen, was die Entscheidungen eines Modells antreibt. Die Forschenden verwendeten deshalb eine Interpretierbarkeitsmethode namens SHAP, die jedem winzigen dreidimensionalen Pixel — einem Voxel — im MRT eine Wichtigkeitsbewertung zuweist. Das Gruppieren dieser Voxel in anatomische Regionen enthüllte ein dynamisches Bild der Krankheit. Früh trat die Amygdala, eine Region, die an Emotion und Gedächtnis beteiligt ist, als besonders wichtig hervor, um Patientinnen und Patienten von gesunden Vergleichspersonen zu unterscheiden. Im Laufe der Zeit gewannen der Hippocampus, der parahippocampale Gyrus und besonders die posterioren Anteile des Temporallappens an Einfluss, während die relative Rolle der Amygdala abnahm. Nach zwei Jahren waren die Unterschiede zwischen Patientengruppe und Kontrollgruppe deutlich schärfer und stärker gebündelt, insbesondere auf der linken Gehirnhälfte.
Muster, die mit Symptomen und klinischen Scores übereinstimmen
Um zu prüfen, ob der Fokus des Modells mit biologischen Befunden übereinstimmt, führte das Team traditionelle Analysen des Hirnvolumens und statistische Tests durch. Sie fanden heraus, dass die graue Substanz in den hervorgehobenen Regionen bei Menschen mit Alzheimer schneller schrumpfte als bei normal alternden Erwachsenen und dass geringere Volumina in diesen Bereichen eng mit schlechteren Werten in standardisierten kognitiven Tests wie dem Mini-Mental-State-Examination und dem Clinical Dementia Rating korrelierten. Der Pfad der Schädigung — von inneren temporalen Strukturen nach außen zu posterioren Sprach- und Assoziationsarealen — spiegelte klassische pathologische Stadieneinteilungen der Alzheimer-Krankheit wider. Es zeigte sich außerdem eine Linksdomäne, was mit der Dominanz des Gehirns für Sprache und bestimmte Gedächtnisfunktionen auf dieser Seite übereinstimmt. Voxel-basierte Morphometrie zeigte, dass frühe Veränderungen verstreut und klein waren, dann aber mit dem Fortschreiten der Krankheit größer und konzentrierter in posterioren temporalen und frontalen Regionen wurden.
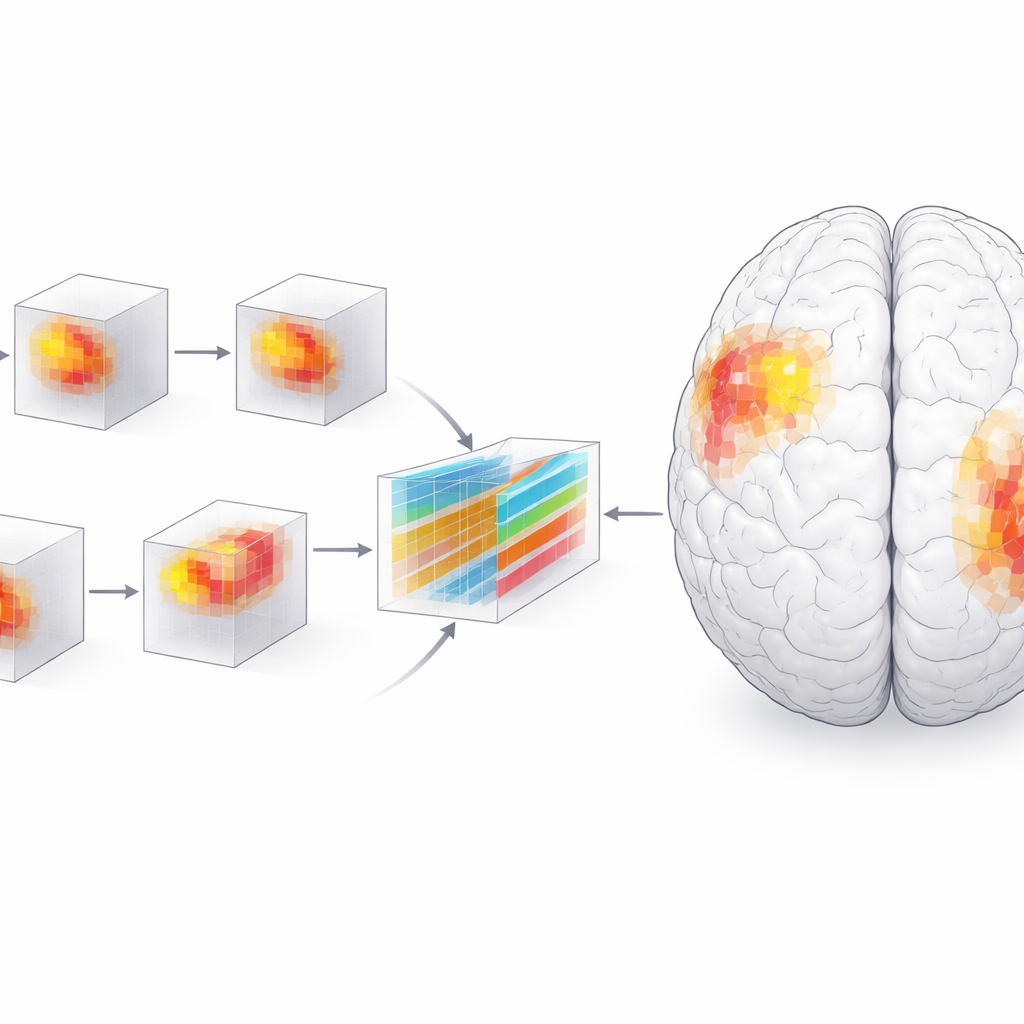
Was das für Patienten und Ärztinnen bedeutet
Für Nicht-Spezialisten ist die Kernbotschaft, dass Alzheimer nicht wie ein einfacher Ein-/Ausschalter im Gehirn wirkt; die Krankheit folgt einem geordneten, aber beschleunigten Verlauf und hinterlässt im Zeitverlauf deutliche Spuren. Indem man ein Deep-Learning-Modell darauf trainiert, nicht nur zu erkennen, wo das Gehirn anders aussieht, sondern wie sich diese Unterschiede über mehrere Jahre entwickeln, bietet diese Studie einen Weg, Alzheimer genauer und früher zu erkennen. Sie benennt außerdem eine kleine Gruppe von Hirnregionen — darunter Amygdala, Hippocampus, parahippocampaler Gyrus und posteriorer Temporalkortex — deren sich verändernde Größe und Struktur eng mit kognitivem Abbau verknüpft ist. Zwar ist weitere Arbeit nötig, insbesondere mit zusätzlichen Bildgebungsverfahren und größeren Datensätzen, doch bringt uns dieser Ansatz näher an die Nutzung zeitaufgelöster Hirnscans und interpretierbarer KI als praxisnahe Werkzeuge für Früherkennung, Monitoring und letztlich zur Steuerung von Interventionen gegen die Alzheimer-Krankheit.
Zitation: Sun, J., Han, JD.J. & Chen, W. Deep learning models identify brain changes during the progression of Alzheimer’s disease. npj Syst Biol Appl 12, 42 (2026). https://doi.org/10.1038/s41540-026-00666-7
Schlüsselwörter: Alzheimer-Krankheit, Hirn-MRT, Deep Learning, longitudinale Bildgebung, Neurodegeneration