Clear Sky Science · de
Entwicklung eines schweren Ratten-Modells des Refeeding-Syndroms und mathematische Modellierung der damit verbundenen Hypophosphatämie
Warum Essen wieder gefährlich sein kann
Wenn Menschen, die stark unterernährt sind, endlich Nahrung oder intravenöse Ernährung erhalten, müssen Ärzte vorsichtig vorgehen. Ein plötzlicher Kalorienzufluss kann ein „Refeeding-Syndrom“ auslösen, eine Komplikation, die das Elektrolytgleichgewicht stört und Herz, Muskeln sowie Lunge schädigen kann. Ein Schlüsselspieler ist Phosphor, ein Mineral, das in jeder Zelle für Energie benötigt wird. In dieser Studie nutzten Forscher Ratten und Computermodelle, um zu erklären, warum der Phosphor im Blut während des Refeedings so dramatisch abstürzen kann und wie man diesen gefährlichen Abfall besser verhindern könnte.
Ein genauerer Blick auf Probleme beim Refeeding
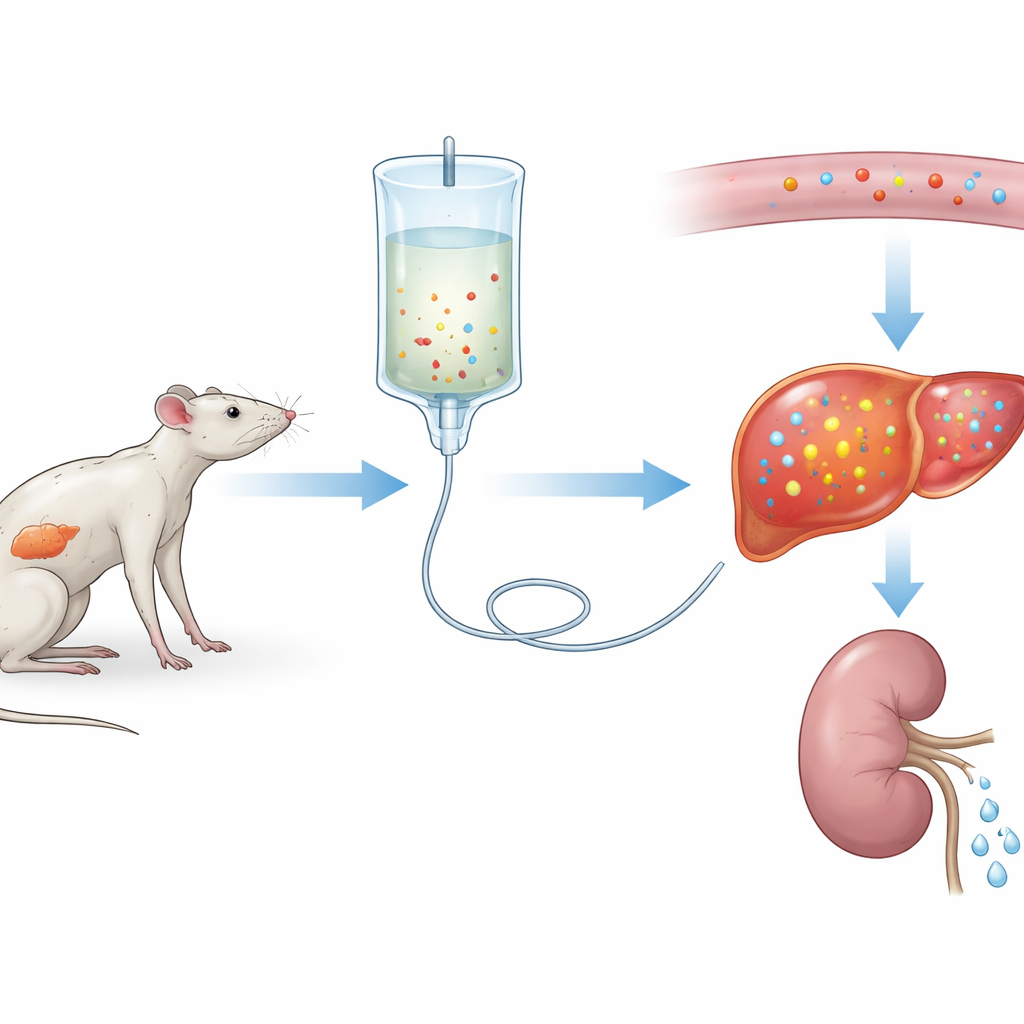
Die Forscher erzeugten zunächst eine schwere Form des Refeeding-Syndroms bei Ratten. Drei Wochen lang erhielt eine Gruppe eine normale Nahrung, während eine andere sehr wenig Protein bekam, um langanhaltende Unterernährung zu simulieren. Beide Gruppen bekamen danach drei Tage lang dieselbe intravenöse Ernährung. Die Ratten mit proteinarmer Diät zeigten einen starken Abfall des Blutphosphors—etwa 75 % Rückgang—zusammen mit Verschiebungen anderer Elektrolyte und Hinweisen auf Organverletzungen, besonders in Leber und Muskulatur. Diese Veränderungen ähnelten einem schweren Refeeding-Syndrom beim Menschen, was darauf hindeutet, dass das Team ein realistisches experimentelles Modell geschaffen hatte.
Was mit Phosphor beim Refeeding passiert
Um zu verstehen, wie sich Phosphor im Körper im Zeitverlauf bewegt, entnahmen die Wissenschaftler wiederholt Blut- und Harnproben derselben Ratten. Sie stellten fest, dass die Blutphosphorwerte sowohl bei normal ernährten als auch bei proteinunterversorgten Tieren nach Beginn der Ernährung sanken, wobei der Abfall in der unterernährten Gruppe deutlich tiefer und langanhaltender war. Überraschenderweise reduzierten die Nieren unmittelbar nach dem Refeeding den Phosphorverlust im Urin, sodass das Mineral nicht einfach ausgeschieden wurde. Stattdessen wurde Phosphor aus dem Blut in Gewebe gezogen, insbesondere in die Leber, deren Vorräte durch die wochenlange Mangelernährung erschöpft waren. Rechnerische Analysen bestätigten, dass die unterernährten Ratten mit deutlich geringerem intrazellulärem Phosphor starteten und diesen dann nach Nährstoffzufuhr aggressiv aufnahmen.
Insulin erklärt nicht alles
Da Refeeding Blutzucker und das Hormon Insulin erhöht, machten Ärzte lange Insulin für die Verlagerung von Phosphor in Zellen verantwortlich. Das Team testete diese Idee, indem es die Insulinfreisetzung mit dem Hormon Somatostatin dämpfte. Wie erwartet stieg der Blutzucker, doch der Absturz des Blutphosphors verbesserte sich kaum. Gleichzeitig stiegen die Spiegel freier Aminosäuren—der Bausteine von Proteinen—an. In einem separaten Experiment entfernten die Wissenschaftler Aminosäuren aus der Infusion. Nun blieben die Phosphorspiegel deutlich stabiler, und der schwere Abfall wurde verhindert, obwohl die Insulinspiegel ähnlich waren. Diese Ergebnisse deuten auf einen kombinierten Effekt hin: Sowohl Insulin als auch Aminosäuren, nicht Insulin allein, treiben die Zellen dazu, beim Refeeding zusätzlich Phosphor aufzunehmen.
Ein verborgenes Kontrollnetz in Leber und Niere
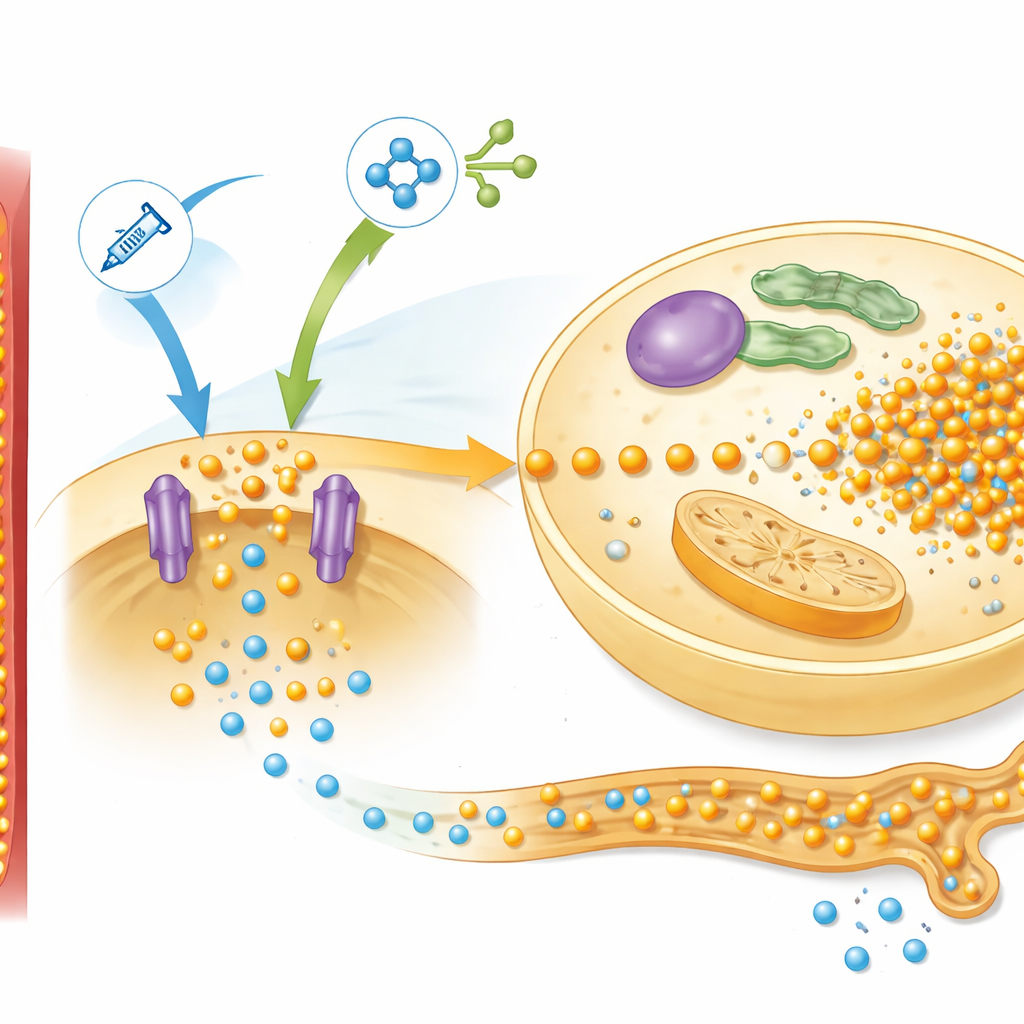
Bei genauerer Untersuchung analysierten die Forscher Leberproteine, die an der Nährstoffwahrnehmung beteiligt sind, mit Fokus auf einen Signalweg namens mTOR, der auf Insulin und Aminosäuren reagiert. Bei den proteinarmen Ratten aktivierte das Refeeding diesen Weg stark und erhöhte die Konzentration eines Phosphattransports namens Pit2, der Leberzellen beim Aufnehmen von Phosphor hilft. Das Muster entsprach dem Verhalten, das ihr mathematisches Modell vorhersagte, in dem dieses Netzwerk zu einem einzelnen Steuerungssignal zusammengefasst wurde, das sie „simTOR“ nannten. Für die Erklärung, wie die Nieren den Phosphorverlust im Urin anpassen, benötigte das Modell außerdem einen separaten Rückkopplungsfaktor. Messungen eines von Knochen stammenden Hormons, FGF-23, passten gut zu dieser Rolle: Seine Spiegel fielen mit Beginn der Ernährung stark ab und begrenzten die Phosphatausscheidung, dann divergierten sie zwischen normal ernährten und unterernährten Ratten in einer Weise, die dem simulierten Rückkopplungssignal entsprach.
Mit Mathematik Präventionsstrategien testen
Indem sie verschiedene Parameter in ihrem Computermodell veränderten, konnten die Autoren „Was-wäre-wenn“-Fragen stellen, die sich am Menschen schwer oder riskant direkt testen ließen. Die Analyse hob drei Haupteinflüsse auf Tiefe und Erholung des Phosphorabfalls hervor: den anfänglichen intrazellulären Phosphor, die Stärke des mTOR-gesteuerten Aufnahmesystems und die Zufuhrrate von Phosphor über die Ernährung. Simulationen deuteten darauf hin, dass das einfache Gleichzeitige Verabreichen großer Phosphatmengen zum Zeitpunkt des Refeedings schwer sicher auszubalancieren wäre. Hingegen könnte die Gabe von zusätzlichem Phosphor vor dem Refeeding—so dass Organe ihre intrazellulären Vorräte allmählich wiederaufbauen—den späteren Absturz im Blut abschwächen. Die Verringerung der Aminosäurenlast, insbesondere jener, die mTOR und Insulin stark aktivieren, erwies sich in den Tierversuchen ebenfalls als schützend.
Was das für Patienten bedeutet
Für Menschen mit Risiko für ein Refeeding-Syndrom—etwa solche mit lang andauernden Essstörungen oder schwerer Gebrechlichkeit—legt diese Arbeit nahe, dass die Gefahr nicht nur von einem Anstieg des Blutzuckers ausgeht. Ausgehungerte Organe starten das Refeeding mit leeren Phosphorspeichern, und unter dem kombinierten Antrieb von Insulin und Aminosäuren nehmen sie das Mineral rasch aus dem Blut auf, während die Nieren vorübergehend die Ausscheidung zurückhalten. Das Ergebnis ist ein scharfer, vorübergehender Mangel im Kreislauf, der lebenswichtige Gewebe schädigen kann. Das hier entwickelte Rattenmodell und die mathematische Grundlage deuten auf gezieltere Präventionsmaßnahmen hin: vorsichtige frühe Gabe von Phosphorpräparaten, sorgfältige Kontrolle proteinreicher Aminosäuregaben und Beachtung von Hormonen, die die renale Ausscheidung steuern. Zusammen könnten diese Ansätze Klinikern helfen, gefährdete Patienten sicherer zu ernähren.
Zitation: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
Schlüsselwörter: Refedingsyndrom, Hypophosphatämie, Phosphorstoffwechsel, mTOR-Signalgebung, parenterale Ernährung