Clear Sky Science · de
Räumliche FBA zeigt heterogene Warburg-Nischen in Nierentumoren und Laktatverbrauch im kolorektalen Krebs
Warum Tumorstoffwechsel im Raum wichtig ist
Krebszellen verhalten sich nicht alle gleich, selbst innerhalb eines einzelnen Tumors. Einige leben nahe Blutgefäßen, andere tief in schlecht versorgten Regionen, und diese Lagen prägen, wie sie Energie beschaffen und nutzen. Diese Studie stellt eine neue Methode vor, um diese verborgene „metabolische Karte“ aus modernen räumlichen Genexpressionsdaten zu entschlüsseln. Dadurch entdecken die Autoren überraschende Muster darin, wie verschiedene Tumoren mit einem Schlüsselstoff, dem Laktat, umgehen, und stellen damit die klassische Sicht in Frage, dass Krebszellen Laktat nur als Abfallstoff ausscheiden.
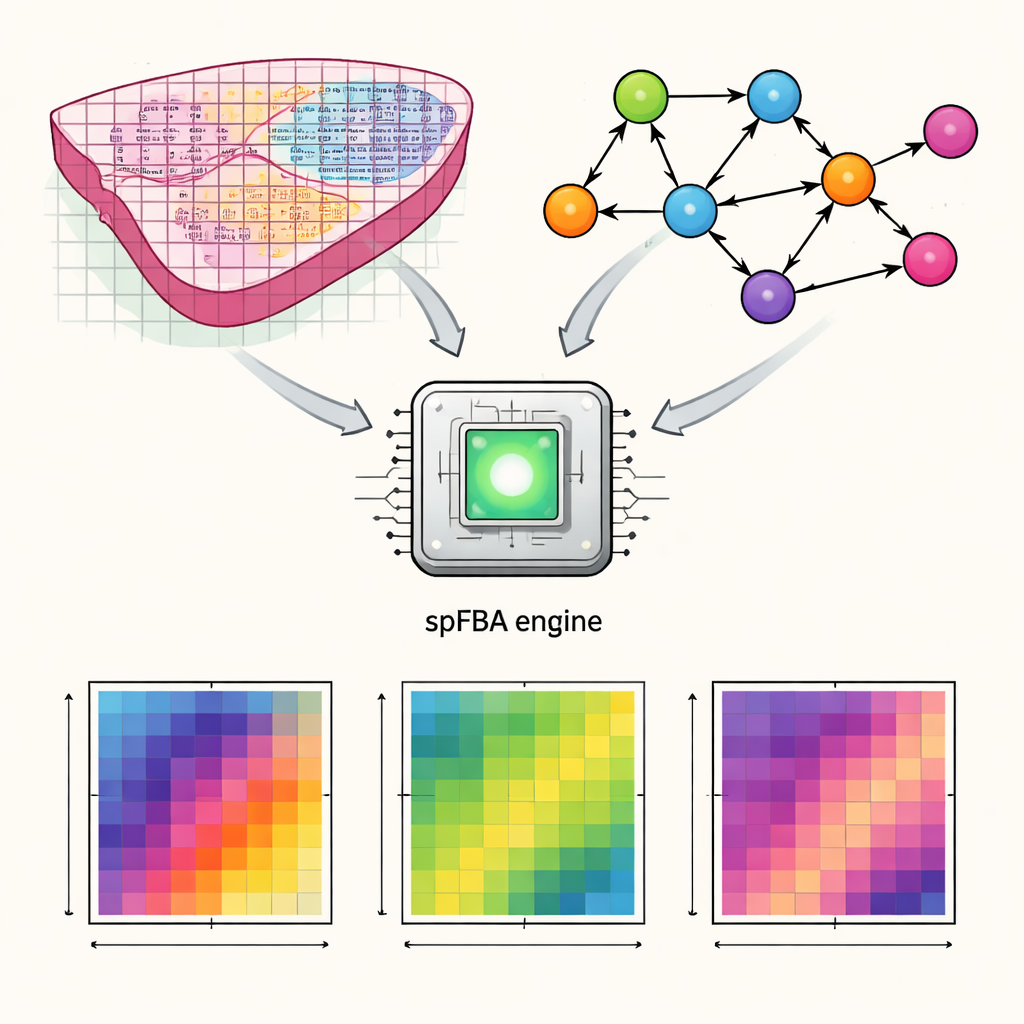
Wie Genkarten in Stoffwechselaktivität übersetzt werden
Die Autoren entwickelten ein rechnergestütztes Rahmenwerk namens spatial Flux Balance Analysis, kurz spFBA. Technologien der räumlichen Transkriptomik messen, welche Gene an tausenden winziger Punkte entlang einer dünnen Gewebeschicht aktiv sind. spFBA kombiniert diese räumlichen Genaktivitätskarten mit detaillierten Modellen des menschlichen Stoffwechsels, die beschreiben, wie Nährstoffe wie Glukose, Sauerstoff und Aminosäuren in Zellen umgewandelt werden. Anstatt anzunehmen, dass jede Region des Gewebes dasselbe metabolische Ziel teilt, behandelt spFBA jeden Punkt unabhängig und prüft, welche Reaktionsmuster dort unter den chemischen Gesetzen und der Massenbilanz möglich sind. Das Ergebnis sind sogenannte „Flussanreicherungs-Scores“, die für jeden Ort anzeigen, wie stark verschiedene metabolische Reaktionen wahrscheinlich ablaufen und in welche Richtung.
Methodenprüfung an Nierentumoren
Um zu prüfen, ob spFBA biologisch sinnvolle Ergebnisse liefert, wandte das Team die Methode zuerst auf das klarzellige Nierenzellkarzinom an, einen Nierentumor, der bekannt dafür ist, stark auf Zuckerabbau (Glykolyse) und Laktatausschüttung – dem Warburg-Effekt – zu setzen. Mit veröffentlichten räumlichen Daten aus zehn Nierentumorproben untersuchten sie, ob die vorhergesagten metabolischen Muster mit der bekannten Gewebearchitektur übereinstimmen. Sie fanden, dass sich Punkte nach ihren abgeleiteten Stoffwechselflüssen gut mit der histologischen Organisation unter dem Mikroskop und mit Clustern basierend auf reiner Genexpression deckten. Wichtig war, dass spFBA den erwarteten metabolischen Kontrast zwischen Tumor- und normalem Nierengewebe wiederfand: Tumorregionen zeigten höheren Glukoseverbrauch, stärkere Biomasseproduktion (ein Proxy für Zellwachstum) und ausgeprägte Laktatsekretion. Gleichzeitig blieb die Sauerstoffnutzung beträchtlich, was zeigt, dass verschiedene Bereiche desselben Tumors je nach lokaler Blutversorgung Fermentation und Atmung mischen können.
Kolorektale Tumoren erzählen eine andere Laktatgeschichte
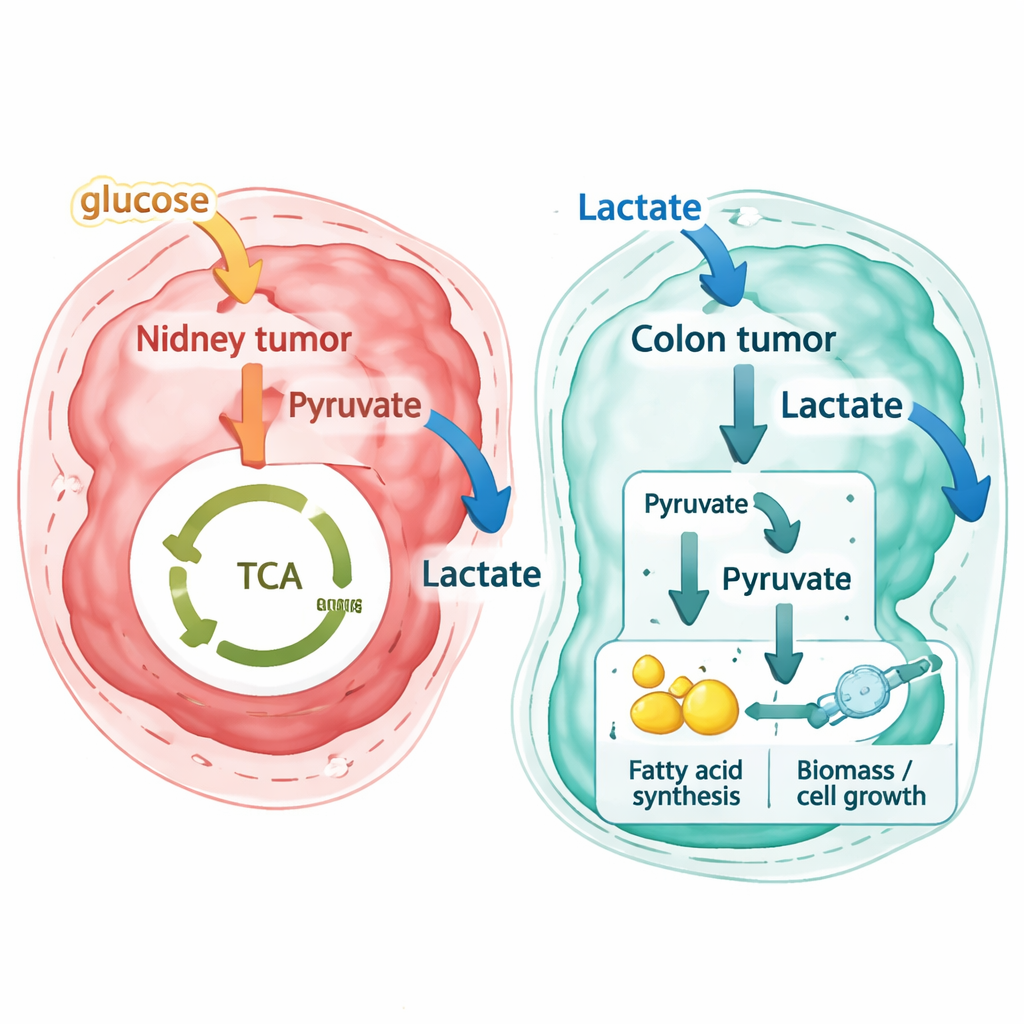
Die Forscher wandten die gleiche Pipeline anschließend auf neue hochaufgelöste räumliche Datensätze einer Patientin bzw. eines Patienten mit primärem kolorektalem Tumor und passenden Lebermetastasen sowie auf ein unabhängiges öffentliches kolorektales Datenset, das mit einer anderen Technologie erzeugt wurde, an. Hier fielen die Ergebnisse auffallend anders aus. Statt Laktat als Abfallstoff auszuscheiden, wurden die meisten kolorektalen Tumorregionen – sowohl im ursprünglichen Darmtumor als auch in den Lebermetastasen – vorhergesagt, Laktat aus ihrer Umgebung aufzunehmen. Stromazellen im angrenzenden Stützgewebe setzten tendenziell kleine Mengen Laktat frei, während Tumorzellen starke Konsumenten waren. Durch die Verfolgung reaktionsspezifischer Flussmuster zeigen die Autoren, dass diese metastatischen Zellen Laktat nicht einfach im üblichen energieerzeugenden Kreislauf der Mitochondrien verbrennen. Vielmehr wandeln sie Laktat in Bausteine um, die in Wege zur Fett- und anderen Biosynthesen eingespeist werden – ein „pseudo-reverser Warburg-Effekt“, bei dem Laktat zur Rohsubstanz für den Aufbau von Zellkomponenten wird.
Metabolische Nischen und die Tumor-Stroma-Grenze
Weil spFBA die räumliche Anordnung bewahrt, kann es genau aufzeigen, wo bestimmte metabolische Austausche stattfinden. In Nierentumoren offenbarte die Methode koexistierende metabolische „Nachbarschaften“: besser oxygenierte, blutreiche Schnittstellen, an denen Krebszellen sowohl atmen als auch fermentieren, und tiefere, schlecht vaskularisierte Kerne, die stärker auf Fermentation angewiesen sind. In kolorektalen Lebermetastasen hob spFBA scharfe Kontraste an der Grenze zwischen Tumor und Stroma hervor, wo sich der Umgang mit Glutamat und Laktat änderte und auf intensiven Austausch an der invasiven Front hindeutete. In allen Datensätzen korrelierten die vorhergesagten wachstumsbezogenen Flüsse mit unabhängigen genbasierten Maßen der Proliferation, was die biologische Plausibilität des Modells stützt. Entscheidenderweise sagte derselbe Algorithmus Laktatsekretion in Nierenkrebs, aber Laktataufnahme in kolorektalem Krebs voraus, was darauf hindeutet, dass die beobachteten Unterschiede aus den Daten selbst und nicht aus voreingenommenen Modellannahmen resultieren.
Was das für das Verständnis und die Behandlung von Krebs bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Krebsstoffwechsel ist nicht nur abnormal – er ist auch hochgradig lokalisiert. Derselbe Tumor kann mehrere metabolische Nischen beherbergen, und optisch ähnliche Tumoren in verschiedenen Organen können dieselben Moleküle gegensätzlich nutzen. Diese Arbeit zeigt, dass sich durch die Überlagerung räumlicher Genexpression mit detaillierten Stoffwechselmodellen ableiten lässt, wo Tumoren wahrscheinlich nach bestimmten Nährstoffen wie Laktat dürsten. Beim kolorektalen Krebs wirft die Entdeckung, dass Tumorzellen Laktat extensiv konsumieren und in wachstumsbezogene Prozesse einspeisen, neue Fragen danach auf, wie Ernährung, Darmmikrobiom und der eigene Leberstoffwechsel die Krankheitsentwicklung beeinflussen und ob das Blockieren der Laktatnutzung diese Tumoren therapieempfindlicher machen könnte.
Zitation: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Schlüsselwörter: Krebsstoffwechsel, räumliche Transkriptomik, Laktat, Warburg-Effekt, kolorektales Karzinom