Clear Sky Science · de
Dynamische Netzwerkanalyse zeigt langreichweitige Restkoppelungen an der pMHC-Schnittstelle, die verbesserte Immunogenität zugrunde liegen
Wie winzige virale Fragmente unsere Immunabwehr lenken
Unsere Killer‑T‑Zellen patrouillieren im Körper auf der Suche nach Anzeichen von Infektionen oder Krebs. Dazu scannen sie winzige Proteinfragmente, sogenannte Peptide, die von Molekülen der MHC‑Klasse I an der Zelloberfläche präsentiert werden. Diese Studie stellt eine feine, aber wichtige Frage: Wie kann eine einzige kleine Veränderung in einem dieser Peptide dazu führen, dass T‑Zellen viel stärker reagieren — oder überhaupt nicht? Die Antwort betrifft nicht nur statische Strukturen, sondern auch, wie das gesamte molekulare Ensemble sich im Laufe der Zeit bewegt und biegt.
Das Schloss, der Schlüssel und die beweglichen Teile
Um die Arbeit zu verstehen, hilft es, sich den Peptid–MHC (pMHC)‑Komplex als Schloss und den T‑Zell‑Rezeptor (TCR) als Schlüssel vorzustellen. Das Peptid sitzt in einer Rinne des MHC‑Moleküls und zusammen bilden sie die Oberfläche, die der TCR abtastet. Frühere Forschung hat gezeigt, dass sowohl die genaue Peptidsequenz als auch die konkrete MHC‑Variante stark beeinflussen, ob eine T‑Zelle reagiert. Wissenschaftler haben auch „veränderte Peptidliganden“ entwickelt, die kleine Änderungen tragen, um Immunantworten zu modulieren, etwa in der Krebsimmuntherapie. Doch während wir viel über die statischen Formen dieser Komplexe wissen, wissen wir deutlich weniger darüber, wie Bewegungen an einer Stelle des Peptids entfernte Bereiche der Schnittstelle beeinflussen können, an denen der TCR tatsächlich bindet.
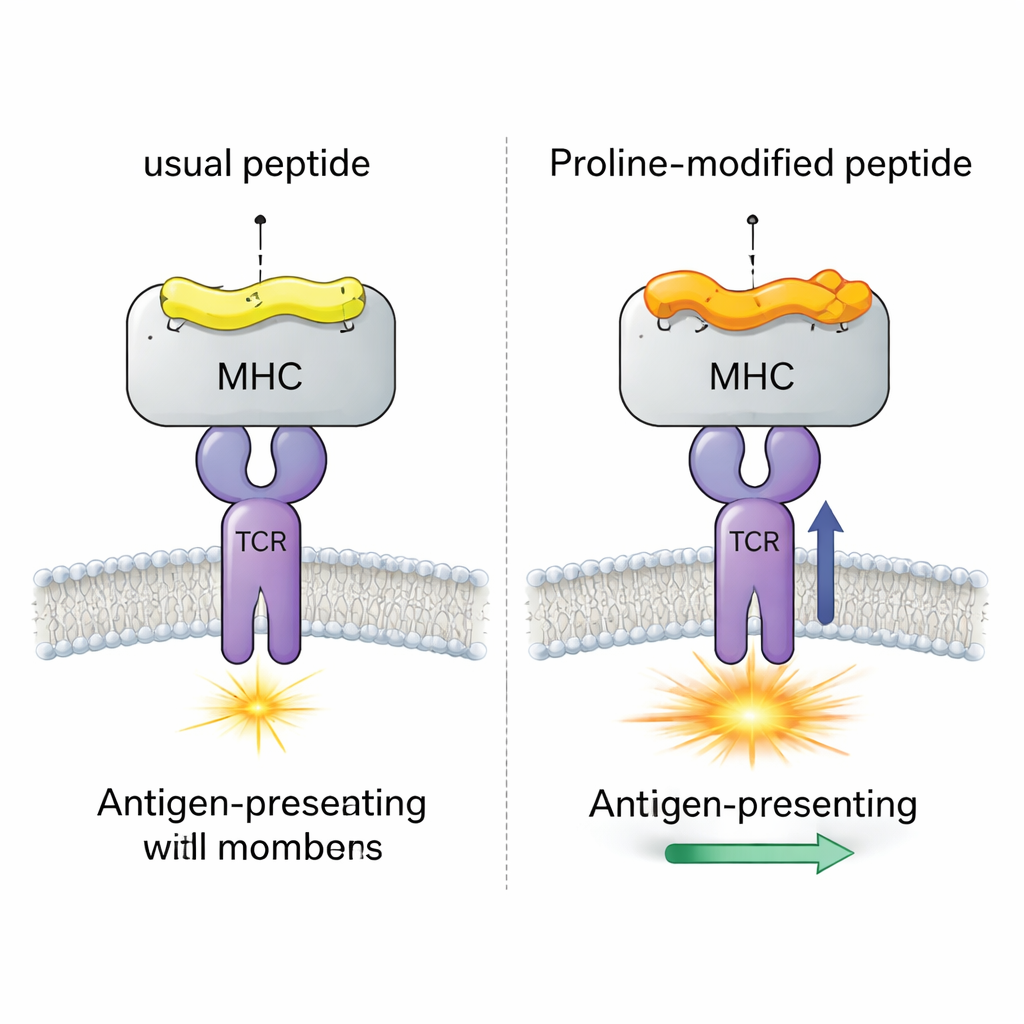
Ein virales Testsystem mit vier fast identischen Peptiden
Das Team konzentrierte sich auf ein gut untersuchtes Mausvirus‑(LCMV)‑System mit dem Peptid gp33, das normalerweise starke CD8+‑T‑Zell‑Antworten auslöst. Sie verglichen vier eng verwandte Versionen dieses Peptids, alle gebunden an dasselbe MHC‑Molekül (H‑2Db). Eine Version ist das ursprüngliche virale Peptid; eine trägt eine Immunflucht‑Mutation, die von T‑Zellen kaum erkannt wird; und zwei sind „Prolin‑veränderte“ Impfstoffkandidaten, bei denen eine einzelne Aminosäure nahe dem Peptidanfang gegen Prolin ausgetauscht wurde. Frühere Experimente zeigten, dass dieser Prolin‑Austausch die Stabilität des Peptid–MHC‑Komplexes erhöht und die Reaktion eines Modell‑TCR (genannt P14) stärkt, doch der genaue Mechanismus blieb unklar.
Moleküle beim Zappeln beobachten: Simulationen treffen Kristallographie
Um herauszufinden, was passiert, kombinierten die Autorinnen und Autoren hochauflösende Kristallstrukturen mit langen, atomgenauen Computersimulationen jeder pMHC‑Kombination in Bewegung. Sie untersuchten, wie stark sich jede Aminosäurerest über die Zeit hinweg schwankt und wie sich diese Schwankungen ändern, wenn die dritte Position des Peptids zu Prolin konvertiert wird. Durch Korrelation der Bewegungsmuster über viele gepaarte Simulationen bauten sie eine „dynamische Karte“ auf, welche Reste zusammen bewegen, selbst wenn sie räumlich weit voneinander entfernt sind. Diese Karte wandelten sie dann in ein Netzwerk um, in dem jeder Rest ein Knoten ist und Kanten statistisch verknüpfte Bewegungen repräsentieren, und analysierten dieses Netzwerk mit graphentheoretischen Werkzeugen, ähnlich denen aus der Sozialnetzwerkanalyse.
Fernkommunikation innerhalb des immunologischen Schlosses
Die zentrale Erkenntnis ist, dass die Veränderung der dritten Peptidposition zu Prolin mehr bewirkt, als nur diese lokale Stelle zu versteifen. Sie ändert, wie Bewegung entlang einer der MHC‑Helices übertragen wird, die die Peptidbindungsrinne begrenzen. Das wirkt sich wiederum auf das Verhalten einer anderen Peptidposition, Position sechs, aus, die direkt unter der TCR‑Kontaktfläche liegt und für die Erkennung kritisch ist. In den „guten“ prolinmodifizierten Varianten durchmisst dieser Rest eine größere Bandbreite an Konformationen, einschließlich solcher, die für die TCR‑Bindung optimal sind. In der Immunflucht‑Variante ohne Prolin ist dieser Rest stärker fixiert und nimmt selten die TCR‑freundliche Orientierung ein. Die Netzwerkanalyse zeigt, dass dieser Einfluss über spezifische Aminosäuren in der MHC‑Rinne weitergegeben wird und eine Kette dynamisch gekoppelte Reste bildet, die die Stelle der Prolin‑Änderung mit der TCR‑Kontaktregion verbinden.
Warum das für Impfstoffe und Immuntherapie wichtig ist
Diese Ergebnisse zeigen, dass Immunogenität — wie stark ein Peptid T‑Zellen auslöst — nicht nur davon abhängt, ob die Formen in einem einzelnen Moment zueinander passen, sondern auch davon, wie der Komplex im Laufe der Zeit „atmet“ und sich biegsam verhält. Eine subtile Veränderung an einer Position kann sich durch das molekulare Netzwerk fortpflanzen und dafür sorgen, dass wichtige Kontaktreste wahrscheinlicher TCR‑kompatible Posen einnehmen. Der rechnerische Workflow der Autorinnen und Autoren bietet einen Weg, solche langreichweitigen Kopplungen systematisch zu identifizieren, was die Gestaltung veränderter Peptide für Impfstoffe und Krebstherapien leiten könnte. Einfach gesagt demonstrieren sie, dass man durch gezieltes Tuning an der richtigen Stelle das gesamte Schloss in einen dynamischeren, „leicht zu öffnenden“ Zustand für den Schlüssel des Immunsystems bringen kann.
Zitation: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
Schlüsselwörter: T-Zell-Erkennung, Peptid‑MHC, Proteindynamik, veränderte Peptidliganden, Immunogenität