Clear Sky Science · de
Den Bereich der direkten zellulären Reprogrammierung mit DiReG navigieren
Eine Zellart in eine andere verwandeln
Stellen Sie sich vor, Sie könnten auf Abruf eine Hautzelle in eine Herz- oder Leberzelle verwandeln. Diese Form direkter Verwandlung, genannt zelluläre Reprogrammierung, könnte Ärztinnen und Ärzten erlauben, Ersatzgewebe zu züchten, Krankheiten im Labor zu modellieren und Medikamente sicherer zu testen. Die richtigen molekularen "Schalter" innerhalb einer Zelle zu finden, ist jedoch wie das Erraten einer Safe-Kombination: Es gibt Tausende von Möglichkeiten, und sie einzeln zu testen ist langsam und teuer. Diese Arbeit erklärt, wie Forschende Computer einsetzen, um die Optionen einzugrenzen, und stellt einen neuen Online‑Leitfaden vor, DiReG, der Forschende dabei unterstützt, Reprogrammierungsrezepte intelligenter zu entwerfen und zu prüfen.
Von Zufallsfunden zu systematischem Design
Die Geschichte der Zellreprogrammierung begann, als Forschende entdeckten, dass das Erzwungen-Einbringen eines einzigen Gens, MyoD1, in Bindegewebszellen diese in Muskelzellen verwandeln konnte. Später wurden andere Kombinationen gefunden, die Neuronen oder insulinproduzierende Zellen erzeugen, sowie die vier "Yamanaka-Faktoren", die erwachsene Zellen in einen stammesähnlichen Zustand zurückversetzen. Diese Durchbrüche zeigten, was möglich ist, doch ihre Entdeckung beruhte stark auf Expertenintuition und langwieriger Laborarbeit. Direkte Reprogrammierung—der direkte Sprung von einer ausgereiften Zellart zu einer anderen—bleibt besonders schwierig, weil viele Versuche halbfertig stecken bleiben, instabile "Hybrid"-Zellen erzeugen oder die vorherige Identität der Zelle nicht vollständig löschen.
Computer als Rezeptfinder
Im letzten Jahrzehnt sind mehrere computationalle Werkzeuge entwickelt worden, um vielversprechende Sets von Transkriptionsfaktoren auszuwählen—jene Gene, die als Hauptschalter für Zellidentität fungieren. Die Arbeit rezensiert sechs führende Methoden, die große Datensätze zur Genaktivität und DNA-Regulation durchsieben, um vorzuschlagen, welche Faktoren einen Wechsel von einer Zellart zu einer anderen antreiben könnten. Einige konzentrieren sich hauptsächlich darauf, welche Gene an- oder abgeschaltet sind, andere bauen schaltplanähnliche Regulationsnetzwerke auf, und neuere Methoden beziehen DNA‑Zugänglichkeit und Enhancer‑Informationen mit ein, wo viele Kontrollschalter sitzen. Jeder Fortschritt liefert nützliche Details, aber keine der Methoden hat sich als klarer Favorit herauskristallisiert—teilweise weil sie an unterschiedlichen Datensätzen und unter verschiedenen Bedingungen getestet wurden, was faire Vergleiche unmöglich macht.
Verborgene Komplexitäten in der Zelle
Die Autorinnen und Autoren weisen darauf hin, dass alle derzeitigen Werkzeuge mehrere Ebenen biologischer Nuancen übersehen. Ein einzelnes "Gen" kann in vielen leicht unterschiedlichen Proteinvarianten (Isoformen) existieren, die sich unterschiedlich verhalten, und heutige Modelle behandeln sie meist als einheitlich. Chemische Markierungen an der DNA, etwa Methylierung, können Kontrollproteine blockieren oder anziehen, doch die meisten Algorithmen ignorieren, ob eine Zielstelle überhaupt nutzbar ist. Viele entscheidende Helfer—Proteinpartner, konkurrierende Familienmitglieder, die um dieselben Bindungsstellen kämpfen, und winzige regulatorische RNAs, die unerwünschte Botschaften stummschalten—bleiben ebenfalls außen vor. Hinzu kommt, dass die meisten Methoden auf gemittelten Signalen aus gemischten Zellproben und auf RNA‑Leveldaten beruhen, die nur grob die tatsächlichen Proteinaktivitäten abbilden, die die Veränderung vorantreiben.
Ein neuer Leitfaden, um die Optionen zu navigieren
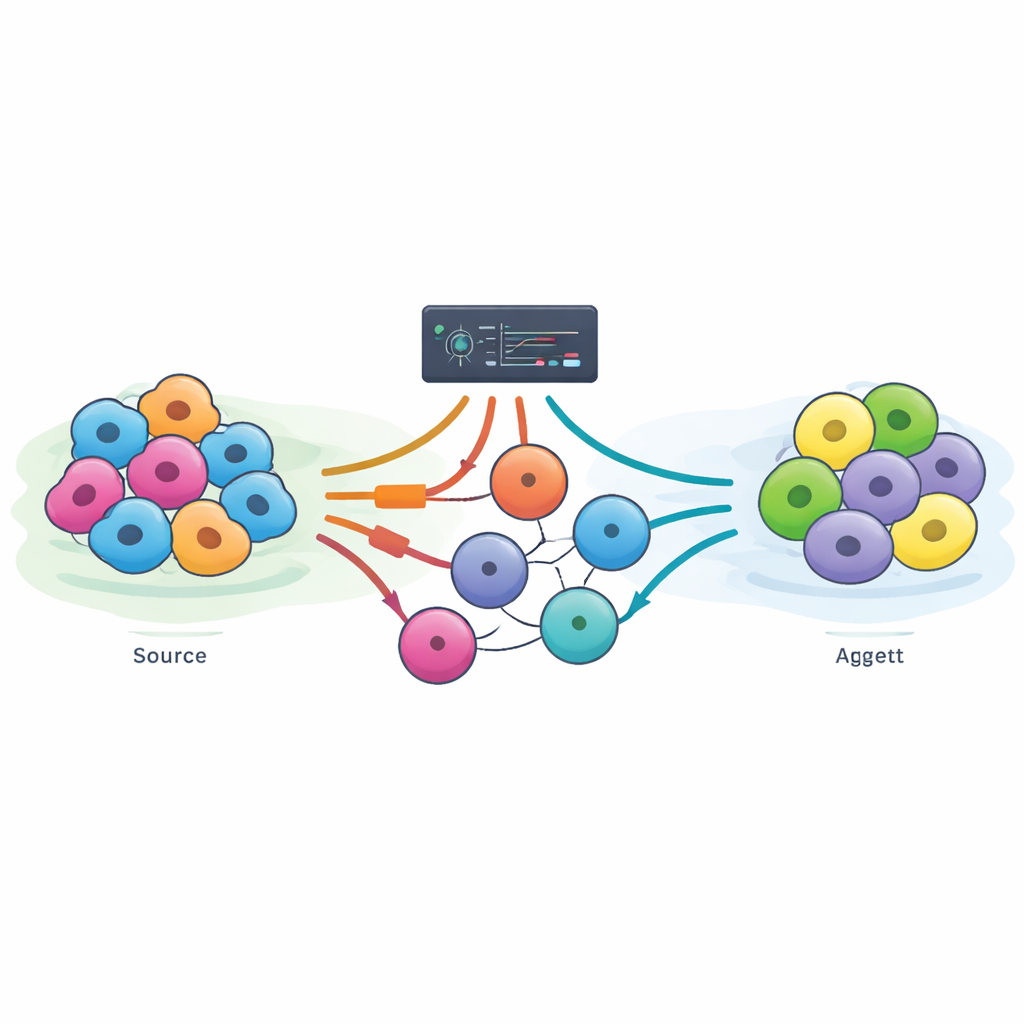
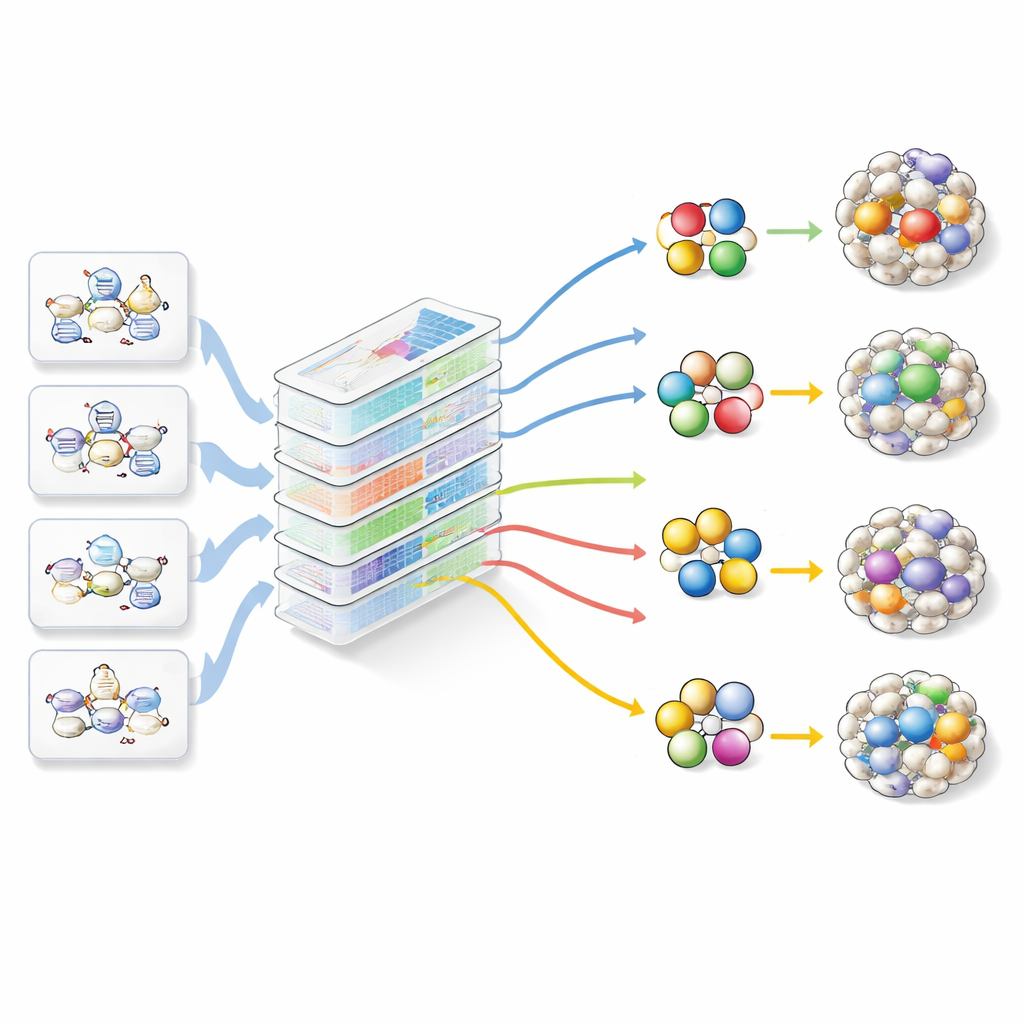
Um trotz dieser Lücken voranzukommen, entwickelten die Autorinnen und Autoren DiReG (Direct Reprogramming Guide), eine Webanwendung, die weniger wie ein allwissender neuer Algorithmus wirkt und mehr wie ein Kontrollzentrum. DiReG sammelt Vorhersagen aus den wichtigsten existierenden Werkzeugen, ergänzt eine einfache, motivationsbasierte Methode, die direkt aus offenen Chromatin‑Daten arbeitet, und verknüpft all dies mit einer kuratierten Bibliothek von Hunderten von Reprogrammierungsstudien. Mithilfe integrierter Frage‑Antwort‑Systeme können Forschende schnell Protokolle, Faktor‑Kombinationen und experimentelle Details in der Literatur finden. Anschließend können sie Kandidatenfaktorensets in einen Analysebereich übertragen, in dem DiReG deren Regulationsnetzwerke zeichnet, prüft, ob die betroffenen Gene denen des gewünschten Gewebes ähneln, untersucht, wo die Faktoren natürlicherweise aktiv sind, und bekannte Interaktionspartner sowie Isoformen hervorhebt, die die Umwandlung fördern oder behindern könnten.
Ein Schritt zu intelligenterer Zellkonversion
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass diese Arbeit noch kein Knopfdruck‑Rezept liefert, um jede Zelle in jede andere zu verwandeln. Stattdessen bietet sie eine zentrale, interaktive Karte dessen, was bekannt ist, was bereits versucht wurde und welche genetischen Schalter am ehesten zusammenwirken. Indem sie Forschende dabei unterstützt, Computer‑Vorhersagen schnell mit biologischem Kontext zu verknüpfen, zielt DiReG darauf ab, Sackgassen‑Experimente zu reduzieren und die Protokollgestaltung rationaler zu machen. Die Autorinnen und Autoren skizzieren auch, was noch fehlt—reichere Daten zu Proteinformen, chemischen Markierungen, Zell‑zu‑Zell‑Interaktionen und tatsächlicher Proteinaktivität. Wenn aufkommende Technologien diese Ebenen ergänzen, könnten künftige Werkzeuge, die auf den hier vorgestellten Ideen aufbauen, die direkte zelluläre Reprogrammierung zuverlässiger, sicherer und näher an der praktischen medizinischen Anwendung machen.
Zitation: Lauber, M., List, M. Navigating the landscape of direct cellular reprogramming with DiReG. npj Syst Biol Appl 12, 35 (2026). https://doi.org/10.1038/s41540-026-00652-z
Schlüsselwörter: zelluläre Reprogrammierung, Transkriptionsfaktoren, Computational Biology, genregulatorische Netzwerke, regenerative Medizin