Clear Sky Science · de
In-silico-Modellierung der Differenzierung des anterioren Vorderdarmendoderms hin zu lungären epithelialen Vorläuferzellen
Stammzellen zu lungenbildenden Zellen machen
Wissenschaftler lernen, wie man die eigenen Stammzellen eines Patienten dazu bringt, Ersatzgewebe für die Lunge zu bilden — was eines Tages Schäden durch Erkrankungen wie COPD, Fibrose oder schwere Infektionen reparieren könnte. Dieser Artikel beschreibt, wie Forscher computergestützte Modellierung nutzten, um einen entscheidenden Schritt auf diesem Weg zu kartieren und zu optimieren: die Umwandlung eines Zwischenzelltyps, des anterioren Vorderdarmendoderms, in frühe lungäre epithelialen Vorläuferzellen — die Ausgangszellen, die später die Atemwege und Lungenbläschen bilden können.
Warum Lungen-Starterzellen wichtig sind
Menschliche induzierte pluripotente Stammzellen (iPSCs) lassen sich aus erwachsenen Geweben rückprogrammieren und dann in Richtung vieler verschiedener Organe lenken. Um Lungengewebe zu erzeugen, durchlaufen diese Zellen zunächst mehrere entwicklungsgeschichtliche Stationen. Eine davon ist das anteriore Vorderdarmendoderm, eine Schicht, die im Embryo normalerweise Teile des Atmungs- und Verdauungssystems hervorbringt. Von dort können sich Zellen mit den richtigen chemischen Signalen zu lungären epithelialen Vorläufern entwickeln, die frühe Lungenmarker tragen und später zu spezialisierten Atemwegs- oder alveolären Zellen reifen können. Da künftige Zelltherapien Milliarden dieser Zellen benötigen werden, brauchen Forscher verlässliche Wege, Erträge zu steigern und Protokolle an verschiedene Patienten-Zelllinien anzupassen, ohne endlose Versuche und Irrtümer im Labor.
Aufbau einer virtuellen Version der Zelldifferenzierung
Das Team erweiterte ein früheres mathematisches Rahmenmodell, um nach eigenem Wissen das erste Populationsmodell dieses spezifischen Übergangs vom Vorderdarmendoderm zu Lungenvorläufern zu erstellen. Sie betrachteten zwei Darstellungsweisen der Zellen: eine einfache Version, die nur die Gesamtzahl lebender Zellen verfolgt, und eine detailliertere Version, die anteriore Vorderdarmzellen und Lungenvorläufer getrennt nachverfolgt. In beiden Fällen erfasst das Modell außerdem Glukose und Laktat im Kulturmedium, um Nährstoffe und Abfallprodukte darzustellen. Mit Methoden der Systembiologie konstruierten die Forscher viele Kandidatengleichungen dafür, wie Zellen wachsen, sterben und sich differenzieren, und verwendeten Identifizierbarkeitstests, um Modelle auszusortieren, deren Parameter sich selbst bei perfekten Daten niemals eindeutig bestimmen ließen.
Intelligentere Experimente mit dem Modell planen
Statt einfach vorhandene Daten zu überpassen, ließen die Forscher das Modell entscheiden, wie neue Experimente durchgeführt werden sollten. Sie nutzten simulierte Daten, um zu ermitteln, wie oft Zellzahlen und Nährstoffniveaus gemessen werden müssten, um Modellparameter genau zu schätzen, wobei sie statistische Präzision gegen Kosten und Arbeitsaufwand häufiger Probenahmen abwägten. Daraus entstand ein praktischer Plan: tägliche Messungen für Glukose und Laktat und Zellzählungen alle ein bis zwei Tage, unter vier Bedingungen, die variierten, wie stark die Kulturen am Tag 10 aufgeteilt wurden und ob das Wachstummedium täglich erneuert wurde. Anschließend führten sie diese Experimente durch und maßen sowohl die Gesamtzellpopulation als auch — mittels Durchflusszytometrie — die Anteile, die noch Vorderdarmzellen blieben oder sich zu Lungenvorläufern entwickelt hatten.
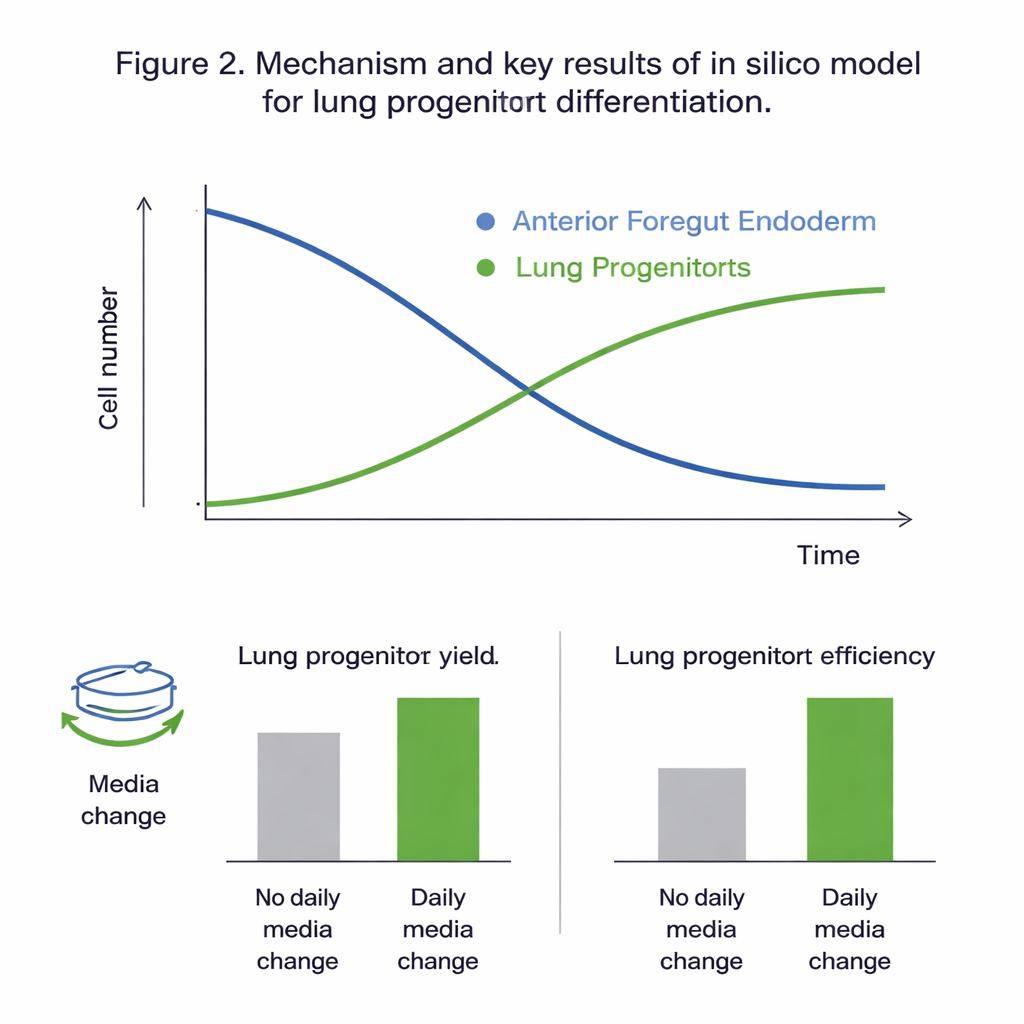
Was die virtuellen Experimente zeigten
Das Anpassen aller Kandidatenmodelle an die experimentellen Daten zeigte, dass das Zwei-Populations-Modell, das Vorderdarm- und Lungenvorläuferzellen getrennt verfolgt, zuverlässig kalibriert werden konnte und das beobachtete Verhalten am besten erfasste. Statistische Prüfungen deuteten darauf hin, dass in dem untersuchten Zeitfenster (Tage 11 bis 15 des Protokolls) die Dynamik hauptsächlich durch Proliferation und Differenzierung der Vorderdarmzellen bestimmt wurde, während die Proliferation der Lungenvorläufer selbst nur gering beitrug. Eine globale Sensitivitätsanalyse untermauerte dieses Bild und hob Wachstum, Sterberaten und Differenzierungsraten der Vorderdarmzellen — sowie den Einfluss der Glukose — als die wichtigsten Stellgrößen hervor, die das Ergebnis steuern. Das kalibrierte Modell reproduzierte nicht verwendete Daten mit Fehlern, die mit der natürlichen Variabilität der Experimente vergleichbar waren, was darauf hindeutet, dass es genau genug ist, um in silico „Was-wäre-wenn“-Szenarien zu untersuchen.
Optimierung von Medienwechseln und Zellaufteilung
Mit einem verlässlichen virtuellen System prüfte das Team, wie sich zwei praktische Protokollentscheidungen auf die Ergebnisse auswirken: wie stark die Kultur am Tag 10 verdünnt wird (Split-Verhältnis) und ob das Wachstummedium täglich ausgetauscht wird. Die Simulationen sagten voraus, dass tägliche Medienwechsel die Zahl der Lungenvorläuferzellen und den Ertrag pro ausgangszelle nahezu verdoppeln — vor allem, indem sie Nährstoffaufbrauch und die Anhäufung von Abfallstoffen und instabilen Signalstoffen verhindern. Die Experimente stimmten eng mit diesen Vorhersagen überein. Das Modell schlug außerdem vor, dass höhere Split-Verhältnisse — also das Verstreichen der Zellen am Tag 10 — die „Ausbeute pro Eingabezelle“ um etwa ein Viertel verbessern, obwohl sie die absolute Zellzahl verringern. In beiden Fällen hatten diese Änderungen wenig Einfluss auf den endgültigen Anteil der Lungenvorläufer in der Kultur; sie veränderten vor allem, wie viele Zellen effizient produziert werden konnten.
Was das für künftige Lungentherapien bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft, dass die Autoren eine Art Flugsimulator für einen kritischen Schritt beim Heranzüchten von Lungenzellen aus Stammzellen gebaut haben. Durch die Kombination sorgfältig geplanter Experimente mit strenger mathematischer Modellierung zeigen sie, wie einfache Protokollentscheidungen — etwa wie oft das Kulturmedium gewechselt wird und wie dicht Zellen angesät werden — die Menge der produzierten lungenbildenden Zellen drastisch beeinflussen können, ohne deren Qualität zu verändern. Solche in-silico-Modelle können helfen, künftige Protokolle zu straffen, experimentelles Rätselraten zu reduzieren und letztlich eine zuverlässigere und skalierbare Produktion von Lungenvorläufern für Forschung, Krankheitsmodellierung und schließlich regenerative Therapien zu unterstützen.
Zitation: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Schlüsselwörter: Lungenvorläuferzellen, induzierte pluripotente Stammzellen, in-silico-Modellierung, Zelldifferenzierung, regenerative Medizin