Clear Sky Science · de
Zusammenhang zwischen Kopienzahlveränderungen und dem immuntranskriptomischen Profil bei Krebs
Warum unsere Gene für die Krebsimmuntherapie wichtig sind
Krebsimmuntherapie wirkt, indem sie das Immunsystem unterstützt, Tumoren zu erkennen und anzugreifen, doch nur ein kleiner Teil der Patientinnen und Patienten profitiert langfristig. Diese Studie stellt eine grundlegende Frage mit weitreichenden klinischen Konsequenzen: Wie formt das genetische Chaos in Tumorzellen – insbesondere großflächige DNA-Gewinne und -Verluste, sogenannte Kopienzahlveränderungen – die Immunreaktion gegen Krebs, und lassen sich diese Effekte anhand von Genaktivitätsmustern ablesen?
Ein panoramischer Blick auf Krebsdaten
Um das zu untersuchen, stellten die Forschenden eine enorme Sammlung von 294.159 Genaktivitätsprofilen aus Tumoren und anderem Gewebe zusammen. Diese Profile, entnommen aus mehreren großen öffentlichen Datenbanken, erfassen, welche Gene in Tausenden von Proben über zahlreiche Krebsarten und experimentelle Bedingungen ein- oder ausgeschaltet sind. Statt einzelne Gene nacheinander zu betrachten, verwendete das Team eine mathematische Methode, um jedes Profil in zugrundeliegende „Komponenten“ zu zerlegen – wiederkehrende Genmuster, die tendenziell gemeinsam an- oder abschwellen und jeweils einen biologischen Prozess widerspiegeln, etwa eine Immunantwort oder die Wirkung einer DNA-Veränderung.
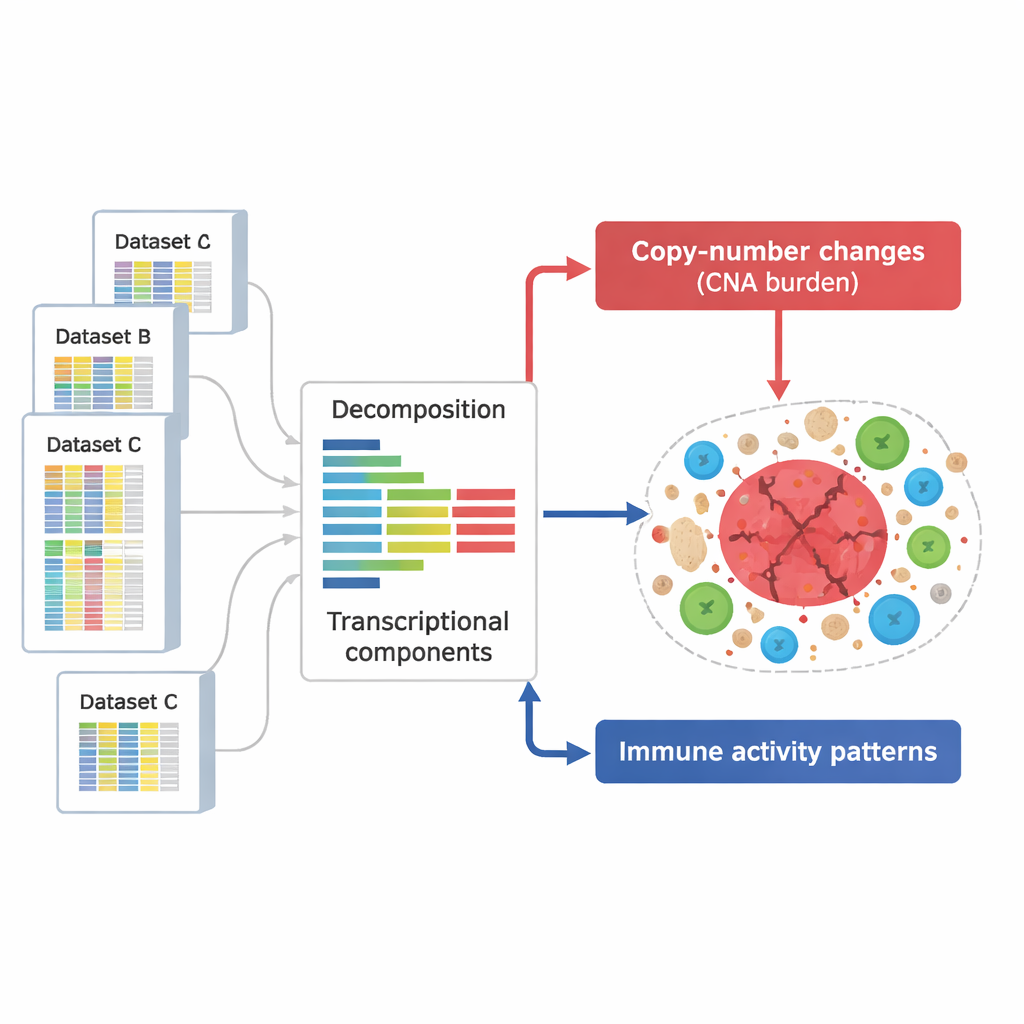
DNA-Schadenssignale von Immunsignalen trennen
Aus diesen Komponenten definierten die Wissenschaftlerinnen und Wissenschaftler zwei zentrale Gruppen. Eine Gruppe erfasste die Effekte von Kopienzahlveränderungen – Chromosomenabschnitte, die in Tumorzellen wiederholt gewonnen oder verloren werden. Diese Muster erstreckten sich über nahezu das gesamte Genom und zeigten, dass die meisten durch solche Veränderungen betroffenen Regionen eine nachweisbare Spur in der Genaktivität hinterlassen. Eine zweite Gruppe von Komponenten war für Gene angereichert, die an Immunfunktionen beteiligt sind, etwa T‑Zell‑Aktivierung, natürliche Killerzellen und Antigenpräsentation. Insgesamt identifizierten sie 657 DNA‑bezogene Komponenten und 283 immunbezogene Komponenten, von denen viele in unabhängigen Datensätzen und Technologien reproduzierbar waren – ein Hinweis darauf, dass sie robuste, allgemein gültige Merkmale der Tumorbiologie repräsentieren.
Mustern einen Bezug zur Therapie response geben
Das Team prüfte anschließend, ob diese immunbezogenen Muster dabei helfen könnten vorherzusagen, wer auf Immuncheckpoint-Inhibitoren anspricht, einer wichtigen Klasse von Krebsimmuntherapeutika. Mithilfe von Daten aus 13 klinischen Studien mit 1.167 Patientinnen und Patienten aus sieben Krebsarten trainierten sie Computermodelle, um Respondende von Nichtrespondenden allein anhand der Aktivität der Immunkomponenten in prätherapeutischen Tumorproben zu unterscheiden. Einige Modelle lieferten starke Vorhersagen, selbst wenn sie an völlig unabhängigen Patientengruppen getestet wurden; ein Modell, das an einer Brustkrebskohorte trainiert wurde, sagte beispielsweise Reaktionen in einer separaten Brustkrebskohorte korrekt voraus und zeigte nützliche Leistung in mehreren anderen Krebsarten. Eine kleine Gruppe von Immunmustern, darunter solche, die mit Interferonantworten, natürlichen Killerzellen und T‑Zell‑Aktivierung verknüpft sind, trug am stärksten zu diesen Vorhersagen bei.
Wie genetisches Chaos die Tumorimmunität umgestaltet
Mit diesem Rahmenwerk verknüpften die Forschenden systematisch die Gesamtbelastung durch Kopienzahlveränderungen – ein Maß dafür, wie umfassend die DNA eines Tumors gewonnen oder verloren wurde – mit der Aktivität jeder Immunkomponente über viele Krebsarten hinweg. Die meisten Immunmuster zeigten eine umgekehrte Beziehung: Tumoren mit hoher Belastung durch DNA‑Veränderungen wiesen tendenziell eine geringere Aktivität von Komponenten auf, die mit nützlichen Immunfunktionen assoziiert sind, etwa Antigenpräsentation und Infiltration durch wichtige Immunzellen. Eine auffällige Minderheit von Mustern bewegte sich jedoch in die entgegengesetzte Richtung. Tumoren mit hoher Veränderungsbelastung zeigten häufig erhöhte Signale von immunsuppressiven Zelltypen, darunter regulatorische T‑Zellen und bestimmte Makrophagen, sowie von entzündlichen Zellen, die das Tumorwachstum eher fördern als zerstören können. Räumliche Analysen von Tumorschnitten bestätigten, dass Regionen mit starken DNA‑Veränderungen häufig mit niedriger Aktivität hilfreicher Immunmuster zusammenfielen und mit „immun‑ausgeschlossenen“ Zonen, in denen Immunzellen auf die Tumorränder beschränkt waren.
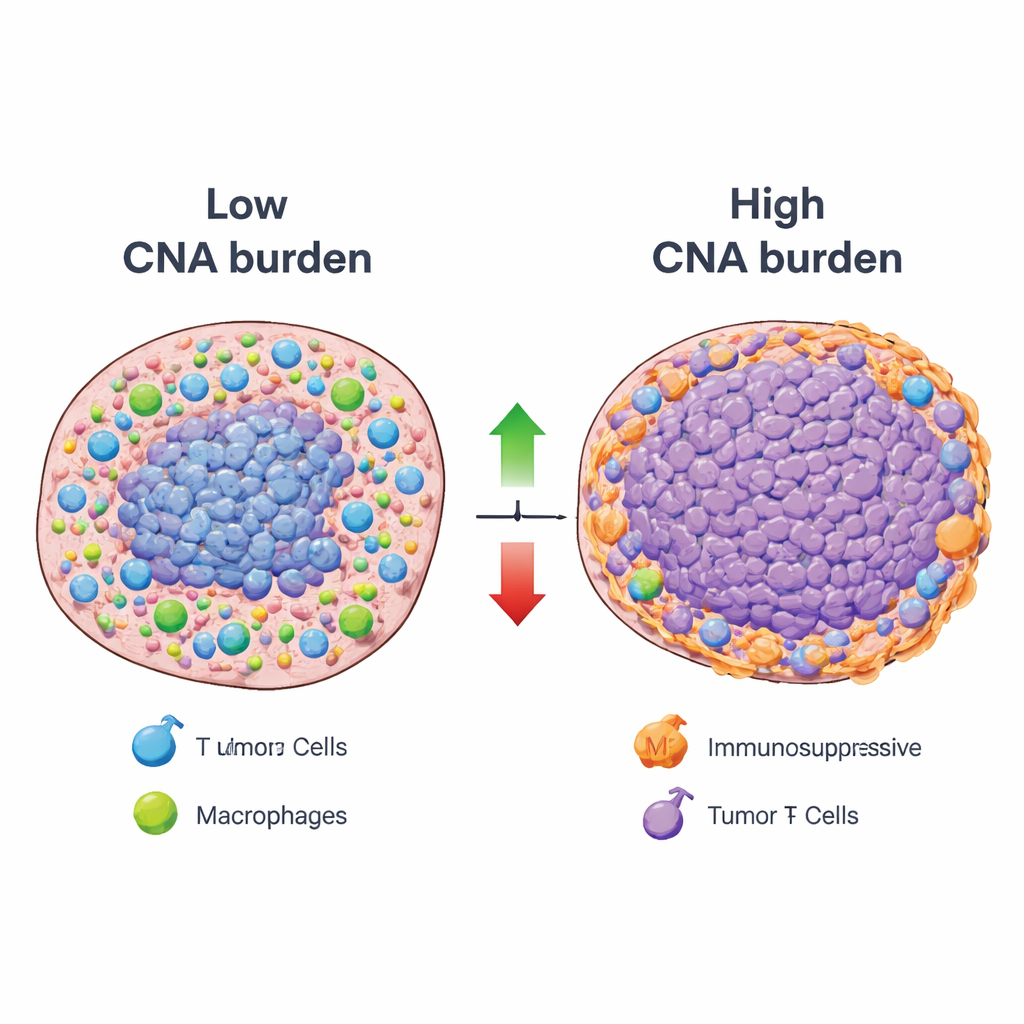
Was das für die künftige Krebstherapie bedeutet
Einfach gesagt zeigt die Studie, dass Tumoren, die von großflächigen DNA‑Gewinnen und ‑verlusten betroffen sind, dazu neigen, hilfreiche Immunantworten abzuschwächen und zugleich unterdrückende oder tumorfördernde Immunumgebungen zu begünstigen. Sie sind jedoch nicht immunologisch stumm; vielmehr zeigen sie spezifische, wiederkehrende Immunzustände, die anfällig für gezielte Therapien sein könnten – etwa Wirkstoffe, die IL‑17‑ oder IL‑23‑Signalwege blockieren, oder Strategien zur Umprogrammierung bestimmter Makrophagen. Indem die Arbeit diese DNA–Immun‑Beziehungen über verschiedene Krebsarten kartiert und die Ressource öffentlich zugänglich macht, liefert sie eine detaillierte Anleitung, warum einige genetisch instabile Tumoren aktuellen Immuntherapien widerstehen und schlägt neue Kombinationstherapie‑Strategien vor, die dem Immunsystem helfen könnten, diese Resistenz zu überwinden.
Zitation: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
Schlüsselwörter: Krebsimmuntherapie, Kopienzahlveränderungen, Tumormikroumgebung, Immuncheckpoint-Inhibitoren, Transkriptomik