Clear Sky Science · de
Simulationsbasierte Inferenz der Zellwanderungsdynamik in komplexen räumlichen Umgebungen
Wie Immunzellen sich durch dichtes Gewebe ihren Weg bahnen
Unsere Immunzellen müssen häufig durch dichtes, labyrinthartiges Gewebe hindurchquetschen, um Infektionsherde oder Lymphknoten zu erreichen. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wie navigieren Zellen durch solche überfüllten Umgebungen, und wie lässt sich ihr Verhalten zuverlässig aus unordentlichen Mikroskopdaten erschließen? Indem die Autoren präzise konstruierte Labor‑„Irrgärten“ mit fortgeschrittenen Computersimulationen und modernen maschinellen Lernverfahren kombinieren, zeigen sie einen neuen Weg, die Regeln zu entschlüsseln, die die Zellbewegung in komplexen Umgebungen steuern.
Ein winziges Labyrinth für Immunzellen bauen
Um zu untersuchen, wie die Umgebung die Bewegung prägt, konzentrierten sich die Forschenden auf dendritische Zellen — Immunwächter, die von peripheren Geweben zu Lymphknoten wandern müssen und dabei von chemischen Lockstoffen, sogenannten Chemokinen, geleitet werden. Sie fertigten einen mikrostrukturierten Chip: einen flachen „Säulenwald“ aus regelmäßig angeordneten Pfosten aus Silikonkautschuk (PDMS) mit engen 10‑Mikrometer‑Spalten, die die engen Räume im Gewebe nachahmen. Auf einer Seite des Chips wurden Zehntausende dendritischer Zellen platziert; die gegenüberliegende Seite enthielt eine Quelle des Chemokins CCL19, die über die Säulen hinweg einen stabilen Gradienten erzeugt. Mit Zeitraffermikroskopie verfolgten sie die Zellkerne einzelner Zellen alle 30 Sekunden, während diese versuchten, zur Chemokinquelle zu gelangen. 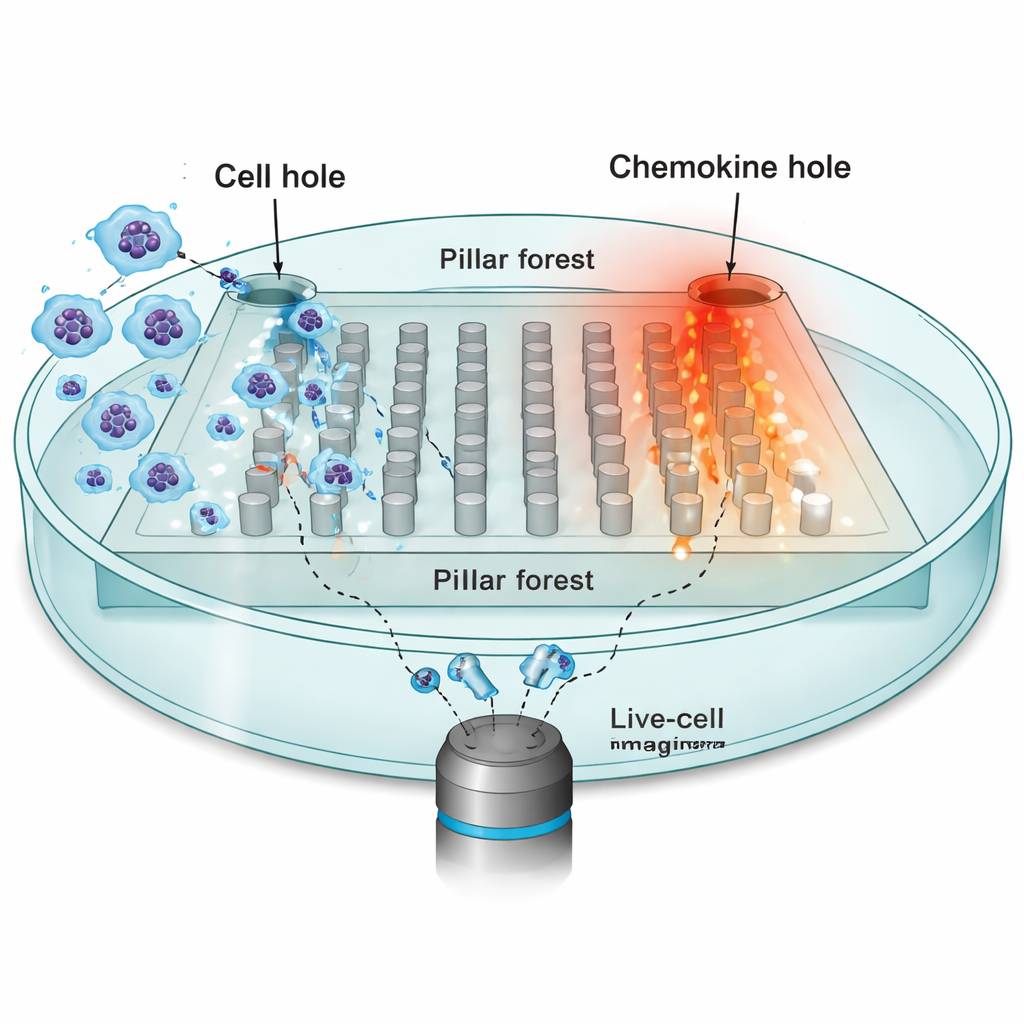
Biologie in ein virtuelles Experiment übersetzen
Um diese Diversität zu verstehen, entwickelte das Team ein detailliertes computergestütztes Modell der Zellmigration auf Basis des sogenannten Cellular‑Potts‑Modells. Anstatt eine Zelle als einfachen Punkt zu behandeln, repräsentiert dieser Ansatz jede Zelle als ausgedehnte Fläche auf einem Gitter, wodurch Formänderungen, das Durchquetschen zwischen Säulen und Reaktionen auf chemische Signale modellierbar werden. Das Modell enthält vier Schlüsselelemente: wie stark eine Zelle vom Chemokingradienten angezogen wird (mdir), wie ausgeprägt ihre Tendenz ist, in der aktuellen Bewegungsrichtung zu verharren (mrand), wie häufig sie ihre Orientierung ändert (beschrieben durch eine Rate λ) und ihre effektive Größe (a). Durch Variation dieser Parameter und das Ausführen von Simulationen erzeugt das Modell synthetische Bahnen, die direkt mit den aufgezeichneten Zellpfaden im Säulenwald verglichen werden können.
Warum handverlesene Messgrößen nicht ausreichen
Traditionell fassen Forschende solche Bewegungsdaten mit einigen vertrauten Kennzahlen zusammen — wie weit eine Zelle zurücklegt (Displacement), wie schnell sie sich bewegt (Geschwindigkeit) und wie sich ihre Richtung über die Zeit ändert (Winkeländerungen). Die Autoren verwendeten diese von Menschen gestalteten Maße zunächst in einer Methode namens Approximate Bayesian Computation (ABC), die nach Parametersätzen sucht, die simulierte Bahnen den experimentellen ähnlich machen. Sie stellten fest, dass diese Zusammenfassungen zwar breite Trends erfassen, aber viele feinräumige Strukturen der Daten übersehen. Infolgedessen blieben einige Modellparameter, insbesondere solche, die die zufällige Persistenz und das Timing der Neuorientierung steuern, schlecht eingegrenzt oder sogar verzerrt. Außerdem erforderte ABC Hunderttausende von Simulationen und viele Stunden Rechenzeit, um akzeptable Anpassungen zu erzielen.
Den neuronalen Netzen überlassen, was wichtig ist
Um diese Grenzen zu überwinden, wandte sich die Studie neueren Methoden zu, die als Neural Posterior Estimation (NPE) bezeichnet werden. Hier wird ein neuronales Netz direkt auf vielen Paaren aus simulierten Daten und zugrunde liegenden Parametern trainiert. Ein Teil des Netzes lernt automatisch eine kompakte Menge an „Zusammenfassungsmerkmalen“ aus ganzen Sammlungen von Zellbahnen; ein anderer Teil lernt, wie diese Merkmale auf wahrscheinliche Parameterwerte zurückgeführt werden. Wichtig ist, dass diese gelernten Merkmale explizit für eine präzise Parameterinferenz optimiert sind, nicht für menschliche Interpretierbarkeit. Die Autoren verwendeten die gelernten Zusammenfassungen anschließend erneut innerhalb eines ABC‑Rahmens und schufen so eine hybride Pipeline, die die Robustheit von ABC mit der Flexibilität neuronaler Netze kombiniert. 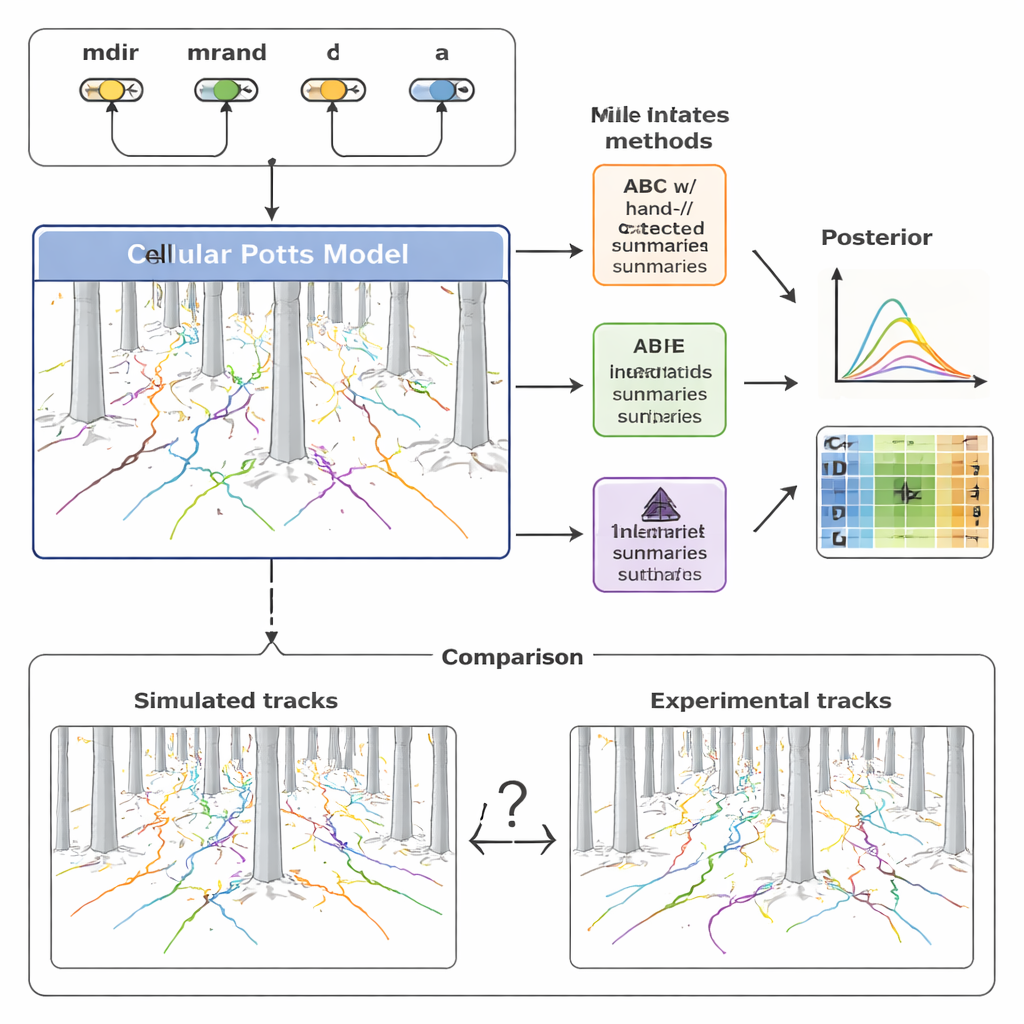
Was der neue Ansatz über Zellnavigation offenbart
Mit diesem kalibrierten Modell untersuchten die Forschenden, wie Chemokinsignale und physische Hindernisse gemeinsam die Migration formen. Die inferierte Zellgröße deutete darauf hin, dass sich dendritische Zellen effektiv verkleinern und verformen, um durch die 10‑Mikrometer‑Spalten zu passen — konsistent mit ihrer bekannten Flexibilität. Simulationen zeigten, dass persistente Zufallsbewegung ein wesentlicher Treiber dafür ist, wie weit sich Zellen ausbreiten, selbst ohne Chemokinführung, und dass der Säulenwald Zellen einfangen kann, wenn starke Richtungsreize und Persistenz zusammenwirken. Überraschend sagt das Modell voraus, dass ein Chemokinsignal, das frühzeitig nur kurz aktiv ist, in manchen Fällen mehr Zellen zum Ziel bringen kann als ein konstanter Reiz, weil anhaltende Anziehungskräfte die Zellen dazu bringen können, in Hindernissen zu kreisen, statt zu entkommen.
Warum das für Biologie und Modellierung wichtig ist
Für Nicht‑Spezialisten ist die Kernbotschaft zweigeteilt. Erstens: Die Migration von Immunzellen im Gewebe besteht nicht nur daraus, einer chemischen Spur zu folgen; sie entsteht aus dem fein abgestimmten Zusammenspiel zwischen Leitreizen, den eigenen Bewegungsgewohnheiten der Zellen und der physischen Struktur ihrer Umgebung. Zweitens: Um diese Regeln aus Bildgebungsdaten zu extrahieren, muss man dem Computer überlassen, welche Muster in den Daten am informativsten sind, statt sich allein auf einfache, vom Menschen entworfene Messgrößen zu stützen. Durch die Integration mikroengineeringbasierter Experimente, formauflösender Simulationen und neuronaler Inferenzmethoden liefert diese Arbeit eine leistungsfähige Vorlage dafür, zu untersuchen, wie Zellen unterschiedlicher Typen sich durch komplexe Umgebungen bewegen — mit potenziellen Anwendungen von der Erforschung der Immunüberwachung bis hin zur Entwicklung besserer Krebstherapien.
Zitation: Arruda, J., Alamoudi, E., Mueller, R. et al. Simulation-based inference of cell migration dynamics in complex spatial environments. npj Syst Biol Appl 12, 20 (2026). https://doi.org/10.1038/s41540-026-00648-9
Schlüsselwörter: Zellmigration, Dendritische Zellen, Chemokin‑Gradienten, simulationsbasierte Inferenz, mikrofluidische Säulenwälder