Clear Sky Science · de
Asthma-vermittelte Kontrolle des Wachstums von Sehnervgliomen über T-Zell–Mikroglia-Interaktionen: Ein mathematisches Modell
Wenn Atemprobleme mit Hirntumoren verbunden sind
Asthma und Hirntumoren wirken wie Welten auseinander: das eine betrifft unsere Atmung, das andere Sehen, Denken und Bewegung. Dennoch haben Ärztinnen und Ärzte ein rätselhaftes Muster beobachtet – Kinder mit Asthma scheinen seltener bestimmte Tumoren des Sehnervs zu entwickeln. Dieser Artikel untersucht, wie eine chronische Lungenerkrankung unerwartet das Gehirn schützen könnte, und verwendet ein mathematisches Modell, um die verborgenen chemischen Gespräche zwischen Immunzellen und Tumorzellen nachzuzeichnen.
Ein langsam wachsender Tumor mit großen Folgen
Sehnervgliome sind meist langsam wachsende Tumoren, die entlang des Sehnervs entstehen, am häufigsten bei Kindern mit einer genetischen Erkrankung namens Neurofibromatose Typ 1 (NF1). Auch wenn diese Tumoren als „niedrigrangig“ gelten, können sie dennoch Sehverluste und hormonelle Probleme verursachen. Bei NF1 führt ein defektes Gen dazu, dass ein Signalmolekül namens RAS überaktiv wird. Diese Überaktivität schaltet die Produktion eines weiteren Moleküls, Midkine, an, das im Sehnerv wie ein Lautsprecher wirkt, Immunzellen anlockt und die lokale Umgebung so umgestaltet, dass sie dem Tumor eher nützt als ihn bekämpft.
Ein tumorförderndes Gespräch zwischen Nerven- und Immunzellen
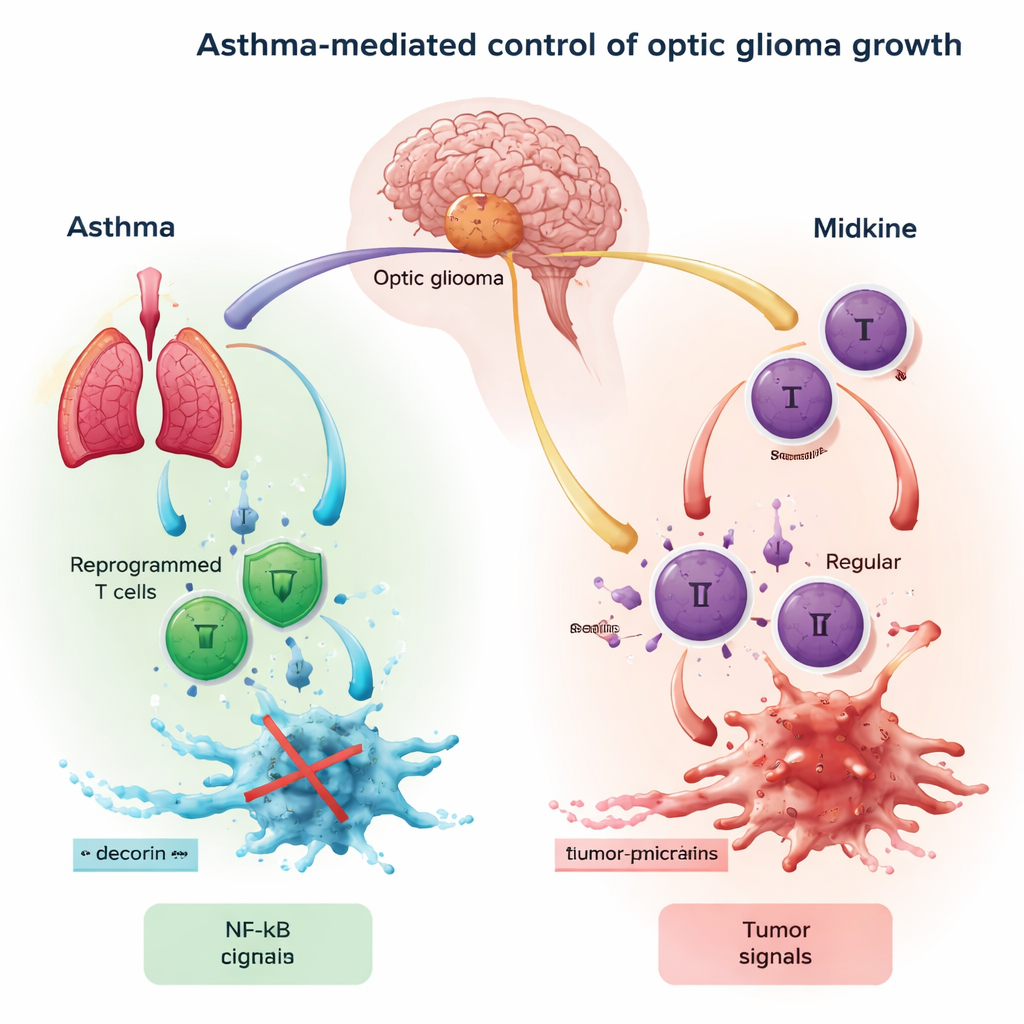
Die Autorinnen und Autoren konzentrieren sich auf eine Ereigniskette, die Sehnerv, Immunzellen und Tumorwachstum verbindet. Midkine aus dem Sehnerv aktiviert zunächst T‑Zellen, eine Art weißer Blutkörperchen, und veranlasst sie zur Freisetzung eines Signals namens CCL4. Dieses Signal bindet dann an Rezeptoren (CCR5 und CCR8) auf Mikroglia, den im Gehirn ansässigen Immunzellen. Wenn genügend CCL4 an diese Rezeptoren andockt, schaltet sich ein zentraler Schalter in den Mikroglia ein, bekannt als NF-κB. Einmal aktiviert, fördert NF-κB die Produktion eines weiteren Signals, CCL5, das die Optikusgliomzellen zu Wachstum, Migration und Immunflucht anregt. Effektiv bildet die Midkine–CCL4–NF-κB–CCL5-Achse ein zirkuläres „Go“-Signal für die Tumorausbreitung.
Wie Asthma T‑Zellen in Tumorbremsen umprogrammiert
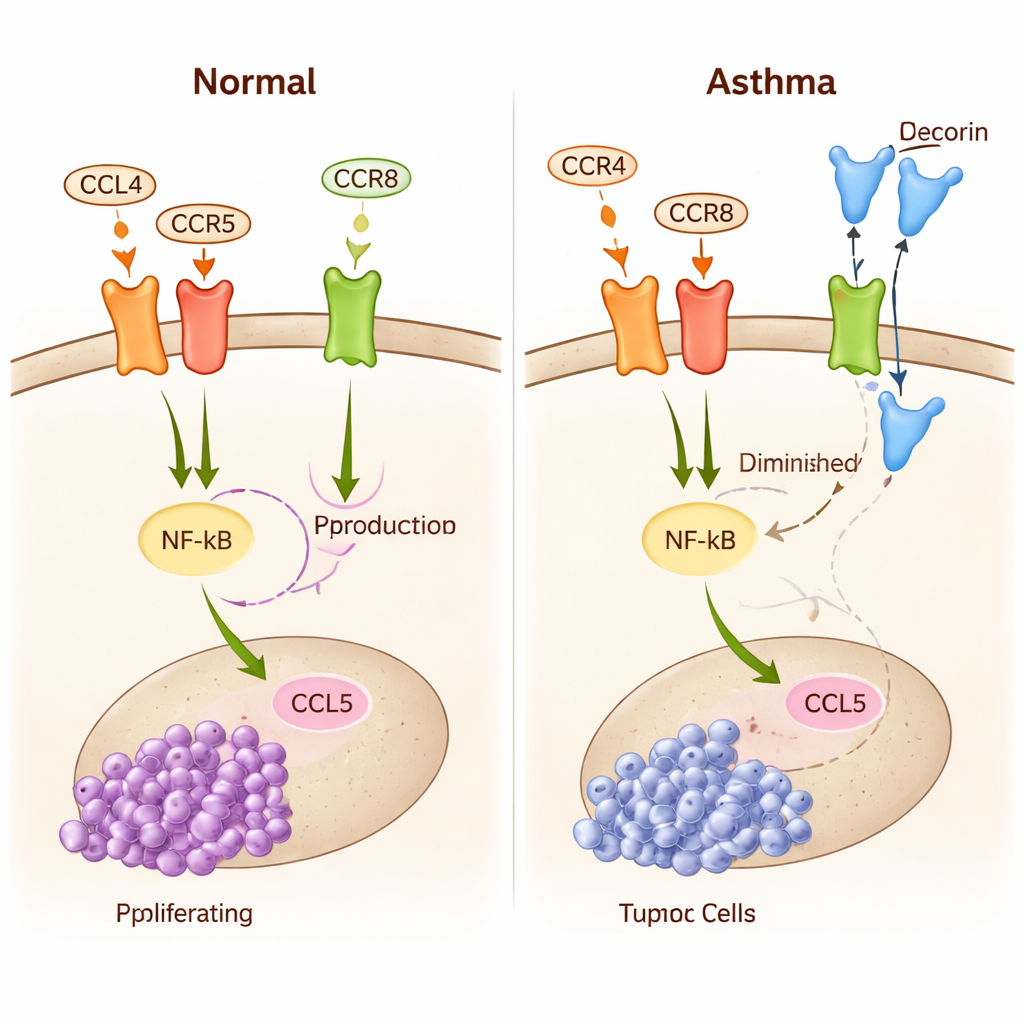
Asthma ist vor allem als Erkrankung chronischer Entzündung der Atemwege bekannt. Bei Menschen mit Asthma werden jedoch einige T‑Zellen in einen anderen Zustand „umprogrammiert“: sie verlieren einen Großteil ihrer direkten zelltötenden Wirkung und sezernieren stattdessen Moleküle, die ihre Umgebung umgestalten. Eines dieser Moleküle ist Decorin, ein kleines Protein mit bekannten antitumoralen Eigenschaften. Die zentrale Idee dieser Arbeit ist, dass asthma‑geprimte T‑Zellen von der Lunge ins Gehirn wandern und im Umfeld des Sehnervglioms Decorin freisetzen können. Decorin konkurriert mit CCL4 um den CCR8‑Rezeptor auf Mikroglia, blockiert damit effektiv Teile des tumorfördernden Gesprächs und verringert NF-κB‑ und CCL5‑Aktivität in den Immunzellen des Gehirns.
Mit Mathematik einem unsichtbaren Netzwerk folgen
Weil dieses Signalisationsnetz zu komplex ist, um es allein intuitiv zu erfassen, entwickelten die Forschenden ein detailliertes mathematisches Modell auf Basis von Differentialgleichungen. Das Modell verfolgt die Mengen wichtiger Moleküle (Midkine, CCL4, Decorin, NF-κB, CCL5), die Aktivität von Rezeptoren auf Mikroglia und das Tumorzellwachstum über die Zeit. Sie nutzten experimentelle Daten, um die Stärke der einzelnen Interaktionen zu kalibrieren, und simulierten zahlreiche Szenarien. Das Modell zeigt, wie kleine Veränderungen in der Bindungsstärke – wie leicht CCL4 oder Decorin an ihre Rezeptoren andocken – die Mikroglia zwischen zwei Modi umschalten können: einen tumorfördernden Zustand mit hohem NF-κB und CCL5 und einen tumorsuppressiven Zustand mit starker Decorin-Bindung und schwachen CCL4‑Signalen. Ein einfacher Index, basierend auf dem Verhältnis von Decorin‑gebundenen zu CCL4‑gebundenen Rezeptoren, sagt zuverlässig voraus, ob der Tumor tendenziell wächst oder ins Stocken gerät.
Entwurf klügerer immunbasierter Therapien
Über die Erklärung hinaus, warum Asthma gegen Sehnervgliom schützen könnte, dient das Modell dazu, Behandlungsstrategien zu untersuchen. Es legt nahe, dass Therapien, die Decorin‑Spiegel erhöhen oder CCL4s Bindung an seine Rezeptoren schwächen, das Tumorwachstum verlangsamen könnten. Die Autorinnen und Autoren testen digital Ansätze wie wiederholte Infusionen von Decorin-produzierenden T‑Zellen oder die Verwendung des Immunboten IL‑2, um diese nützlichen Zellen im Körper zu expandieren. Interessanterweise zeigen die Simulationen, dass nicht nur die Gesamtdosis, sondern auch das Timing solcher Behandlungen wichtig ist: moderate, gut getaktete Dosierungen können Mikroglia ebenso effektiv im tumorsuppressiven Zustand halten wie größere, seltener verabreichte Dosen – mit potenziell weniger Nebenwirkungen.
Was das für Patientinnen, Patienten und Familien bedeutet
Für Nicht‑Spezialisten ist die zentrale Botschaft, dass die chronische Entzündung bei Asthma, sonst meist als schädlich betrachtet, das Immunsystem gelegentlich so umgestalten kann, dass bestimmte Hirntumoren behindert werden. Indem sie T‑Zellen zu Fabriken für Decorin macht, scheint Asthma das Gleichgewicht im Sehnerv von einer wachstumsfördernden Umgebung hin zu einer für Krebs weniger günstigen zu verschieben. Niemand schlägt vor, Asthma als Therapie einzusetzen, doch die hier aufgedeckten Mechanismen könnten neue Behandlungen inspirieren, die dessen schützende Aspekte nachahmen – durch maßgeschneiderte T‑Zell‑Therapien oder Medikamente, die die blockierende Wirkung von Decorin imitieren, um Kinder mit Risiko für Sehnervgliom zu schützen.
Zitation: Lee, D., Lawler, S. & Kim, Y. Asthma-mediated control of optic glioma growth via T cell-microglia interactions: A mathematical model. npj Syst Biol Appl 12, 26 (2026). https://doi.org/10.1038/s41540-026-00647-w
Schlüsselwörter: Sehnervgliom, Asthma, Decorin, T-Zellen, mathematische Modellierung