Clear Sky Science · de
Optimale Steuerungstheorie als Methode zur Gestaltung multidrogiger adaptiver Therapieschemata
Warum das Zähmen von Krebs besser funktionieren kann als dessen Auslöschung
Die Krebsbehandlung zielt normalerweise darauf ab, so viele Tumorzellen wie möglich möglichst schnell zu töten. Doch dieses aggressive Vorgehen kann nach hinten losgehen: Es beseitigt häufig die medikamentensensiblen Zellen und räumt unbeabsichtigt den Weg für medikamentenresistente Zellen frei. Dieser Artikel untersucht eine kontraintuitive Idee – mit Mathematik und zwei Krebsmedikamenten zugleich zu arbeiten, um sensible und resistente Zellen im Wettbewerb zu halten, sodass der Tumor deutlich länger beherrschbar bleibt.
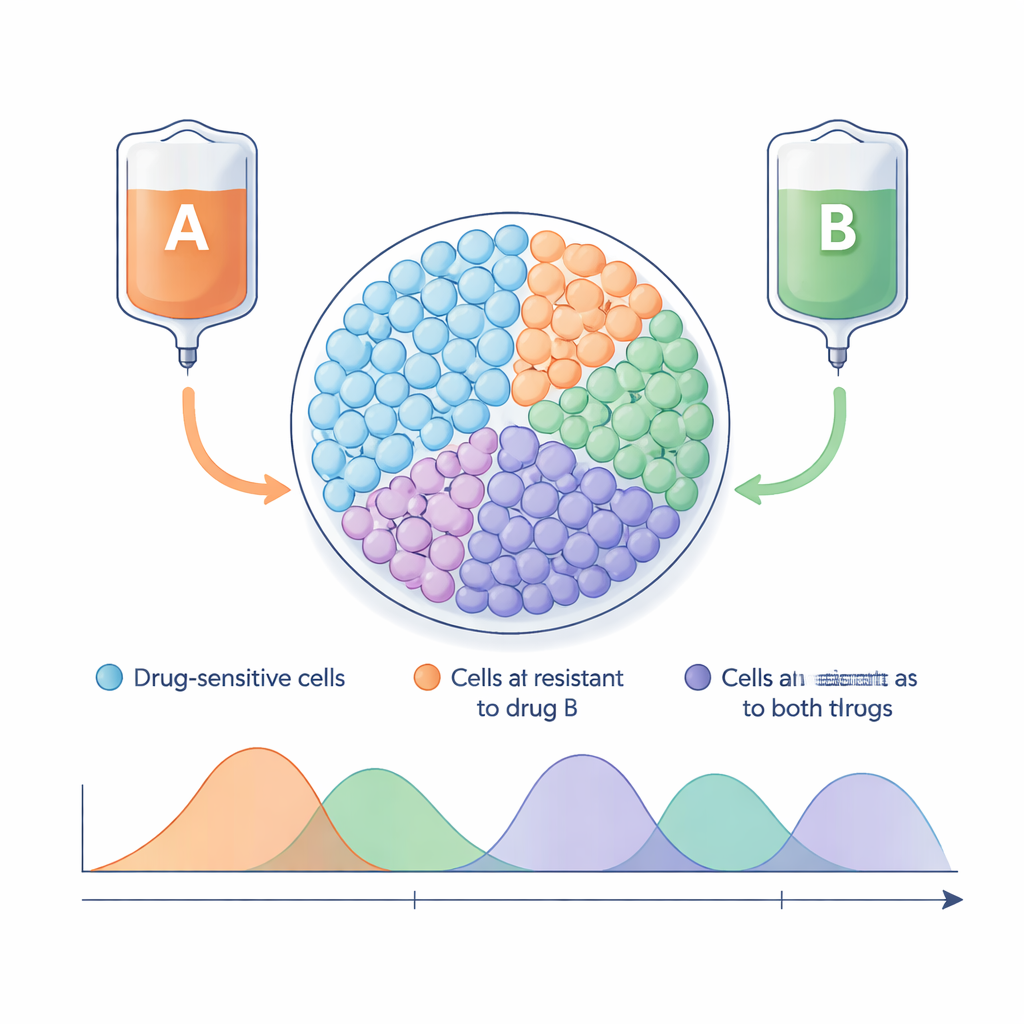
Neues Denken darüber, wie Tumoren sich unter Therapie entwickeln
Tumoren sind keine homogenen Massen identischer Zellen. Vielmehr sind sie gemischte Gemeinschaften, die Zellen enthalten, die leicht durch eine Behandlung getötet werden, und andere, die bereits gegenüber einem oder mehreren Wirkstoffen resistent sind. Standardchemotherapieschemata konzentrieren sich auf maximale Zellabtötung und berücksichtigen selten, wie diese Diversität dem Tumor ermöglicht, sich unter Arzneidruck weiterzuentwickeln. Wenn eine starke Behandlung sensible Zellen entfernt, können resistente Zellen nahezu ungehindert wachsen, was zu einem Rückfall führt. Adaptive Therapie kehrt diese Logik um: Anstatt auf vollständige Auslöschung zu zielen, soll eine stabile Population sensitiver Zellen erhalten werden, damit diese resistente Konkurrenten verdrängen und den gesamten Tumor auf einer für den Patienten tolerierbaren Größe halten.
Mathematik zur Gestaltung intelligenterer Multidrug‑Pläne
Die Autoren entwickelten ein mathematisches Modell eines Tumors, der aus vier Zelltypen besteht: Zellen, die gegenüber beiden Medikamenten sensibel sind, Zellen, die nur gegen Medikament A resistent sind, Zellen, die nur gegen Medikament B resistent sind, und Zellen, die gegen beide resistent sind. Das Modell nimmt an, dass diese Zellen begrenzten Raum und Ressourcen teilen, sodass ihr Wachstum langsamer wird, wenn der gesamte Tumor sich einer Maximalgröße nähert. Zusätzlich können die beiden Medikamente über die Zeit hoch- oder heruntergefahren werden. Das Team wandte dann die Theorie der optimalen Steuerung an — einen Zweig der Mathematik, der hilft, dynamische Systeme optimal zu lenken — um eine klinisch relevante Frage zu beantworten: Wie sollten die Dosierungen der beiden Medikamente im Zeitverlauf variiert werden, um den Tumor so lange wie möglich unter einer gewählten Größenschwelle zu halten?
Zellwettbewerb schlägt maximale Dosen
Die Analyse zeigte allgemeine Regeln für den Einsatz der Medikamente. Wenn der Tumor nahe der erlaubten Größenbegrenzung gehalten wird, konkurrieren sensible und teilweise resistente Zellen stark mit den vollständig resistenten, was deren Ausbreitung verlangsamt. Die erfolgreichsten Schemata, genannt Competition Maintenance (CM) — Wettbewerbs‑Erhaltungspläne — modulierten die Dosen gezielt so, dass die Gesamtgröße des Tumors nahe dieser Schwelle schwankte. Manchmal wurden beide Medikamente gemeinsam in einem festen Verhältnis und graduell erhöht; in anderen Fällen wurde ein Medikament adaptiv eingesetzt und das zweite später hinzugefügt. Im Gegensatz dazu schnitten Schemata, die stark darauf setzten, ein oder beide Medikamente auf ihren maximal erlaubten Dosen zu halten, tendenziell schlechter ab, weil sie zu viel Wettbewerb eliminierten und es den vollständig resistenten Zellen schließlich ermöglichten, zu dominieren.
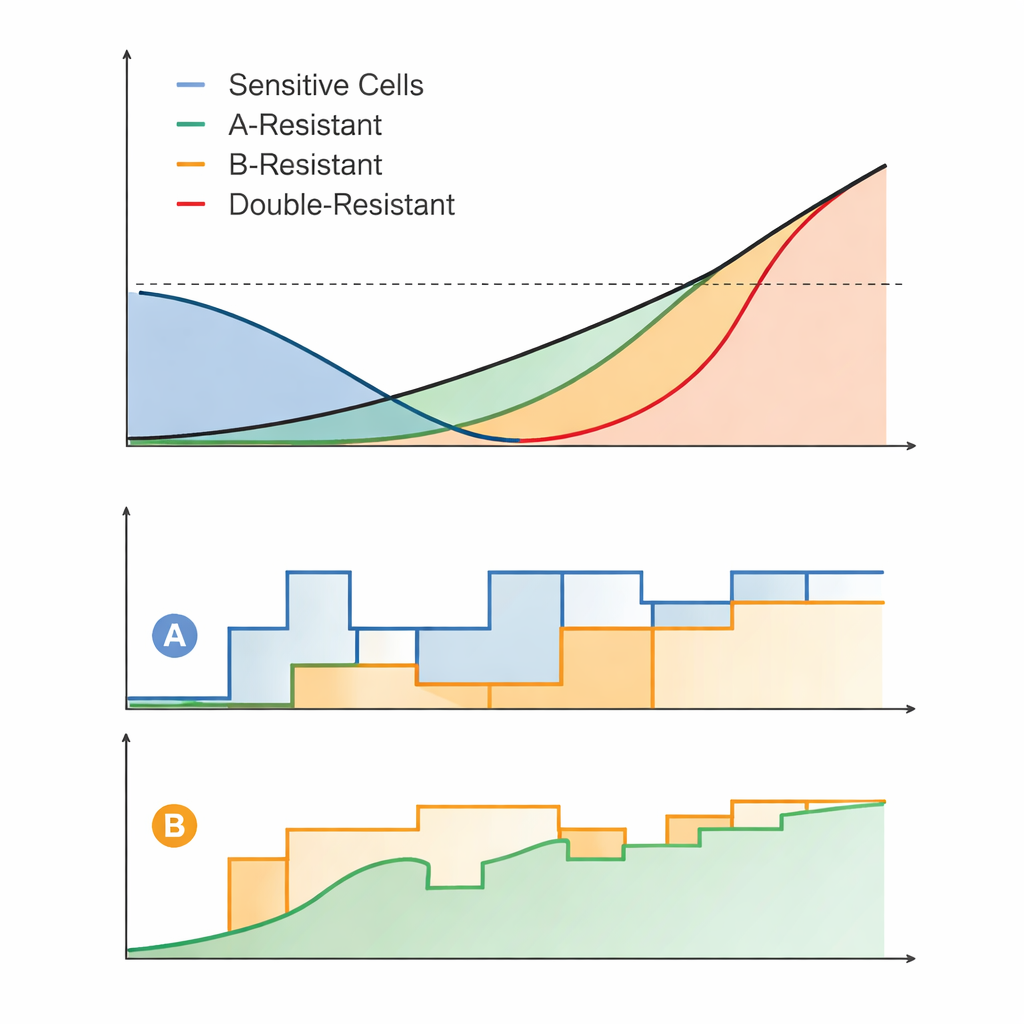
Vom idealen mathematischen Plan zu praktikablen Behandlungsplänen
Eine kontinuierlich perfekte Dosisanpassung ist in der Klinik oder selbst in Laborversuchen unrealistisch, daher entwickelten die Autorinnen und Autoren „praktische“ Versionen ihrer CM‑Pläne. In diesen vereinfachten Schemata wurden die Arzneidosen nur einmal pro Tag und in groben Schritten angepasst. Selbst unter diesen Einschränkungen kontrollierten die praktischen adaptiven Schemata den Tumor in der Regel deutlich länger als standard‑ähnliche Strategien, etwa beide Medikamente konstant hoch zu verabreichen oder erst dann von einem Volldosis‑Medikament auf das andere zu wechseln, wenn der Tumor wieder gewachsen war. Der Vorteil wettbewerbsbasierter Strategien war besonders deutlich, wenn die zugelassene Tumorgrößenschwelle und die maximalen Arzneidosen nicht extrem niedrig waren — Bedingungen, unter denen starker Wettbewerb aufrechterhalten werden kann.
Was das für die künftige Krebsversorgung bedeutet
Insgesamt zeigt die Studie, dass in einem Setting, in dem Arzneimittelresistenz bereits existiert, der Schlüssel zur Verlängerung der Kontrolle weniger in der Raffinesse der Zellabtötung liegt als darin, wie gut der Wettbewerb zwischen sensiblen und resistenten Zellen bei einer beherrschbaren Tumorgröße erhalten wird. Die Theorie der optimalen Steuerung bot eine systematische Methode, viele mögliche Zwei‑Medikamenten‑Schemata einzugrenzen und zu vergleichen, wobei robuste Muster hervorgehoben wurden statt eines fragilen „perfekten“ Plans. Obwohl die Arbeit auf einem vereinfachten Labor‑ähnlichen Modell basiert und experimentell überprüft werden muss, stützt sie eine wachsende Sichtweise: Für einige fortgeschrittene Krebserkrankungen könnte die beste Strategie darin bestehen, die Krankheit als chronisches, sich entwickelndes Ökosystem zu managen, statt zu versuchen, sie um jeden Preis zu vernichten.
Zitation: Widdershins, A., Hansen, E., Read, A. et al. Optimal control theory as a method for designing multidrug adaptive therapy regimens. npj Syst Biol Appl 12, 27 (2026). https://doi.org/10.1038/s41540-025-00613-y
Schlüsselwörter: adaptive Therapie, Arzneimittelresistenz, optimale Steuerung, Krebs‑Evolution, multidrug‑Schemata