Clear Sky Science · de
Lebensmitteltaugliche Lacticaseibacillus paracasei-Postbiotika unterdrücken die Bildung von Streptococcus mutans-Biofilmen im Mund und deren Kariogenität
Kariesbekämpfung mit lebensmittelbasierten Helfern
Zahnverfall ist eines der weltweit häufigsten Gesundheitsprobleme und wird größtenteils von zuckerliebenden Bakterien verursacht, die unseren Zahnschmelz angreifen. Diese Studie untersucht eine neuere Idee: Statt sich ausschließlich auf scharfe Mundspülungen oder lebende „gute Bakterien“ (Probiotika) zu verlassen, könnten wir unsere Zähne mit sicheren, stabilen Substanzen schützen, die von nützlichen Lebensmittelmikroben produziert werden. Die Forschenden zeigen, dass Postbiotika eines lebensmitteltauglichen Bakteriums, Lacticaseibacillus paracasei, einen wichtigen kariesauslösenden Keim und dessen klebrigen Zahnbelag schwächen können und damit auf neue Arten von Mundpflege-Lebensmitteln und -Spülungen hinweisen.
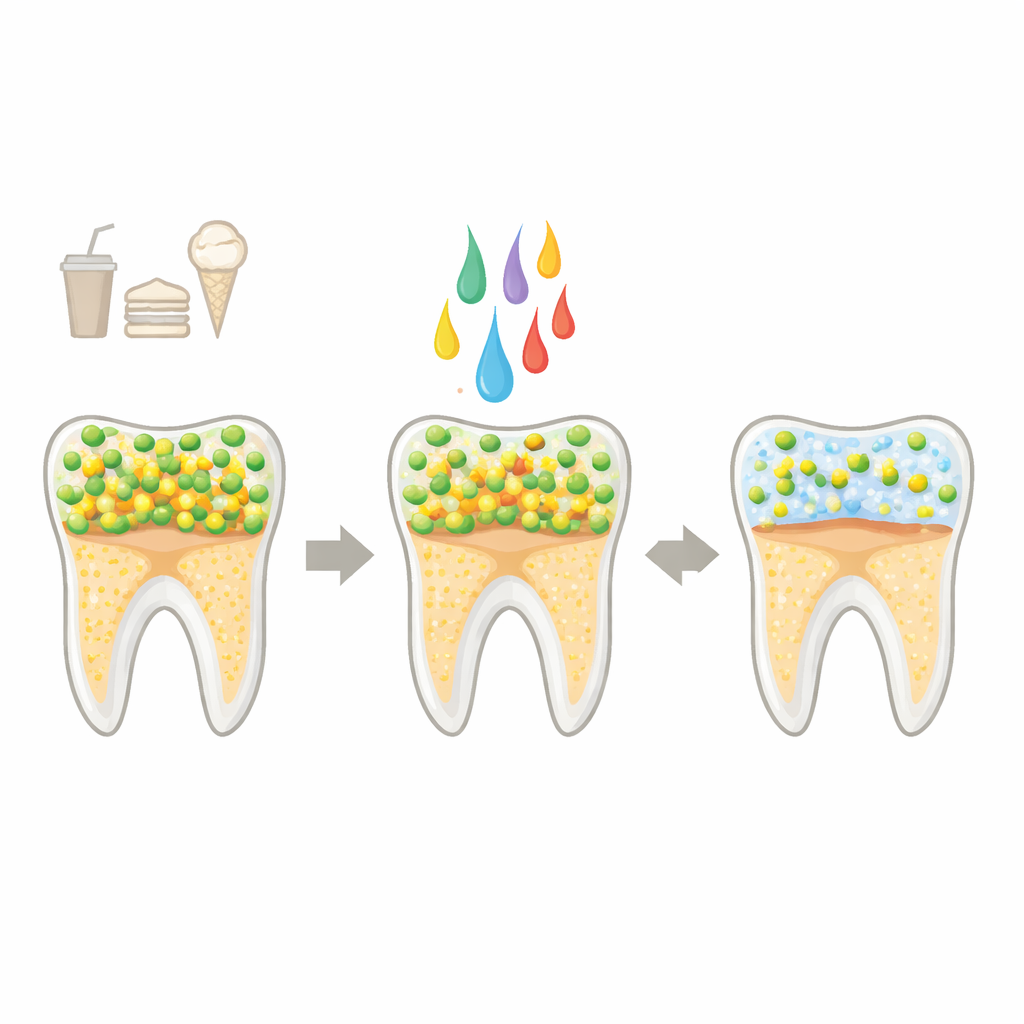
Der Kariesverursacher und ein neuer Verbündeter
Zahnverfall beginnt, wenn unser normales Mundmikrobiom aus dem Gleichgewicht gerät. Häufiger Zuckerkonsum nährt säurebildende Bakterien wie Streptococcus mutans, die dicke, kleberartige Schichten (Biofilme) auf den Zähnen aufbauen. Diese Biofilme halten Säuren am Schmelz fest, lösen Mineralien heraus und führen schließlich zu Karies. Zähneputzen, Zahnseide und chemische Spülungen helfen, sind aber im Alltag nicht immer perfekt anwendbar und können Nebenwirkungen haben. Probiotische Produkte mit lebenden Bakterien sind vielversprechend, werfen aber Fragen zu Stabilität, Lagerung und Sicherheit auf. Postbiotika — nicht lebende Zubereitungen aus nützlichen Bakterien oder deren sekretorischen Komponenten — bieten einen Mittelweg: Sie können lebensmitteltauglich, langlebig und leichter handhabbar sein und dennoch schädliche Mikroben in eine gesündere Richtung lenken.
Wie Postbiotika schädliche Mundbakterien schwächen
Das Team konzentrierte sich auf das zellfreie Überstand (cell-free supernatant, CFS) von L. paracasei, also die Brühe, die nach Entfernung der Bakterien übrigbleibt. Sie testeten, wie diese Flüssigkeit freischwimmende S. mutans-Zellen und in Biofilmen wachsende Bakterien beeinflusst. In Laborversuchen stoppte das CFS nahezu vollständig die Vermehrung von S. mutans. Im Elektronenmikroskop wirkten behandelte Zellen schrumpelig und beschädigt, mit rauen Oberflächen und Trümmern. Durchflussbasierte Zellmessungen bestätigten, dass ihre Membranen durchlässig wurden, ihr inneres elektrisches Gleichgewicht zusammenbrach und deutlich weniger Zellen metabolisch aktiv blieben. Das CFS machte die bakterielle Oberfläche zudem weniger wasserabweisend, was wichtig ist, da stärker haftende, hydrophobe Zellen leichter an den Zähnen und untereinander hängen bleiben, wenn Plaque entsteht.
Abbau klebrigen Plaques und Schutz des Schmelzes
Wenn S. mutans Biofilme bildete, hatte das Postbiotikum weiterhin starke Effekte. Das CFS verringerte die Gesamtmasse des Biofilms, und eine konzentrierte Form reduzierte sie noch stärker. Die Bakterien innerhalb dieser Filme wuchsen schlecht, bildeten kürzere Ketten und produzierten weniger der zuckerhaltigen Klebemasse (Exopolysaccharide), die dem Plaque seine Struktur verleiht. Dreidimensionale Aufnahmen zeigten dünnere, fleckigere Biofilme mit weniger lebenden, intakten Zellen und einer geschwächten Matrix. Um echte Zähne nachzuahmen, wuchsen die Forschenden S. mutans auf synthetischen Schmelzscheiben, die mit menschlichem Speichel beschichtet waren, und setzten sie dann wiederkehrend „Fütterung“ und „Spülung“ mit entweder CFS, einer Standardmundspülung (Chlorhexidin) oder einer Kontrolllösung aus. Die mit CFS behandelten Biofilme waren glatter und heller und — am wichtigsten — setzten weniger freien Kalzium aus dem Schmelz frei, ein direktes Zeichen reduzierter Demineralisierung, obwohl die umgebende Flüssigkeit weiterhin recht sauer blieb.
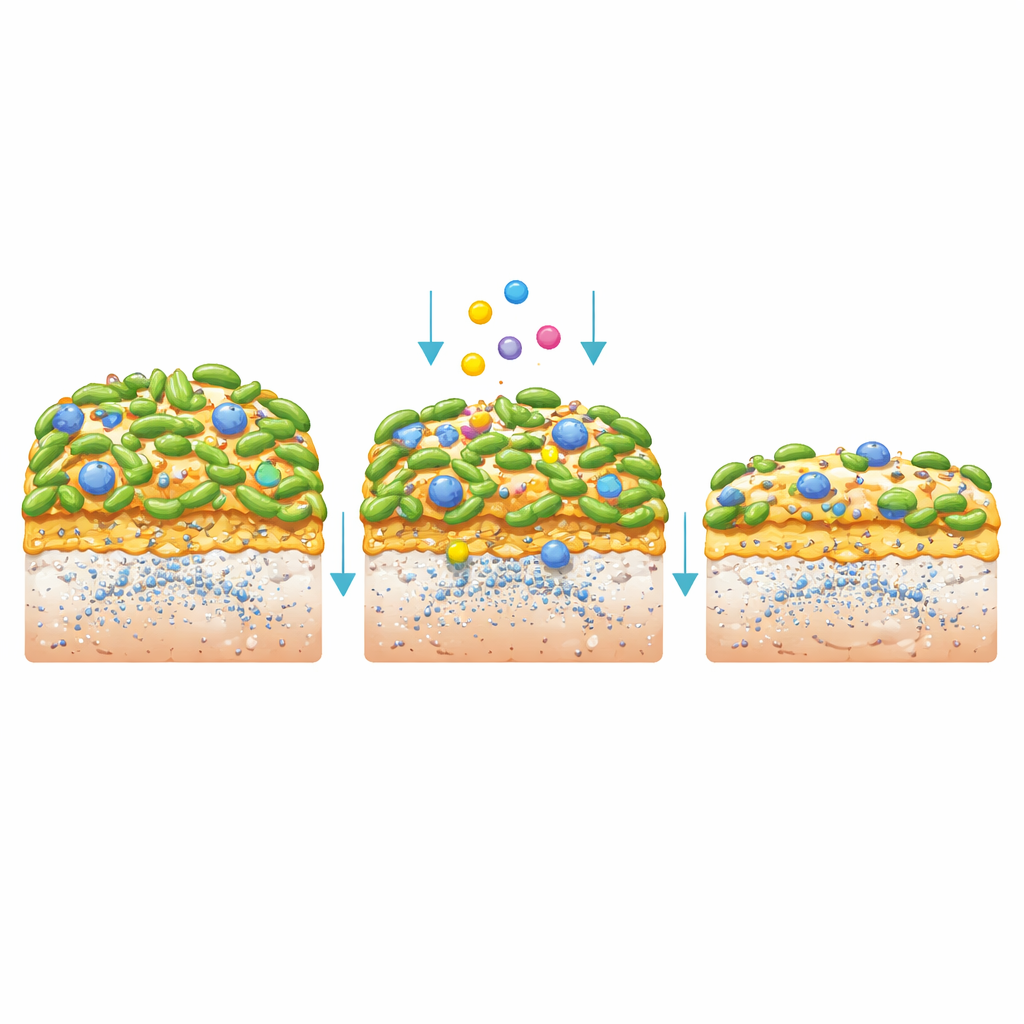
Ein Blick ins molekulare Spielbuch
Um herauszufinden, was im CFS die Wirkung erzielte, schalteten die Wissenschaftler gezielt mögliche Komponenten aus. Der Abbau von Proteinen, das Entfernen von Wasserstoffperoxid oder das Hinzufügen extrahierter Zucker aus der Brühe veränderte die antibakterielle Wirkung kaum. Aber das Neutralisieren der Säure schwächte die Wirkung deutlich, was darauf hindeutet, dass organische Säuren die Schlüsselfaktoren sind. Diese Säuren waren mehr als nur niedriger pH: dieselbe Säure erzeugt durch Mineralsäure allein unterdrückte S. mutans nicht annähernd so stark, was auf spezifische Mischungen organischer Säuren hindeutet, die zusammenwirken. Das Team untersuchte anschließend, welche bakteriellen Gene und kleinen Moleküle sich veränderten, als S. mutans mit CFS wuchs. Sie fanden eine geringere Aktivität in Genen, die mit Haftung, Kleberbildung, Stressresistenz und bakteriellen Kommunikationssystemen (Quorum Sensing) verbunden sind, die Gruppenverhalten koordinieren. Bestimmte Metaboliten, wie Kreatin und Phosphoenolpyruvat, veränderten sich in einer Weise, die zu geringerer Säureproduktion und schwächerer Virulenz passte, was half zu erklären, warum weniger Schmelzmineral verloren ging.
Was das für die tägliche Mundpflege bedeuten könnte
Einfach gesagt zeigt diese Arbeit, dass sichere, lebensmitteltaugliche Postbiotika von L. paracasei die Verteidigung eines wichtigen kariesverursachenden Bakteriums durchlöchern, dessen Plaque ausdünnen, seine Abwehrkräfte schwächen und die Säureschäden an zahnähnlichen Oberflächen verringern können. Da diese Postbiotika gegenüber Hitze, Lagerung und verschiedenen Bedingungen stabil sind, könnten sie in Lutschpastillen, Spülungen oder funktionelle Lebensmittel eingearbeitet werden und als sanfte, langanhaltende Unterstützung neben Zähneputzen und Zahnseide dienen. Sie ersetzen zwar nicht gute Mundhygiene oder regelmäßige Zahnarztbesuche, weisen aber auf eine Zukunft hin, in der clevere, lebensmittelbasierte Inhaltsstoffe die mikroskopische Gemeinschaft im Mund gezielt verändern, um Zähne länger stärker zu erhalten.
Zitation: Luo, SC., Hu, PF., Wei, SM. et al. Food-grade Lacticaseibacillus paracasei postbiotics suppress oral Streptococcus mutans biofilm formation and cariogenicity. npj Sci Food 10, 89 (2026). https://doi.org/10.1038/s41538-026-00742-6
Schlüsselwörter: Zahnkaries, orales Mikrobiom, Postbiotika, Streptococcus mutans, funktionelle Lebensmittel