Clear Sky Science · de
Lycopin mildert durch T-2-Toxin induzierte hepatische Ferroptose, indem es die Nrf2/Mitophagie-Achse bei Mäusen anvisiert
Warum ein Schimmelpilzgift in Alltagsgetreide wichtig ist
Viele Grundnahrungsmittel, darunter Weizen und Mais, können mit einem Schimmelpilzgift namens T-2-Toxin kontaminiert sein. Dieser unsichtbare Schadstoff übersteht Kochen und Verarbeitung, und eine langfristige Exposition kann stillschweigend lebenswichtige Organe schädigen, besonders die Leber. Die hier zusammengefasste Studie stellt zwei dringende Fragen: Wie genau schädigt T-2-Toxin die Leber, und kann eine natürliche Lebensmittelverbindung — Lycopin, das rote Pigment in Tomaten und anderen Früchten — vor diesem Schaden schützen?
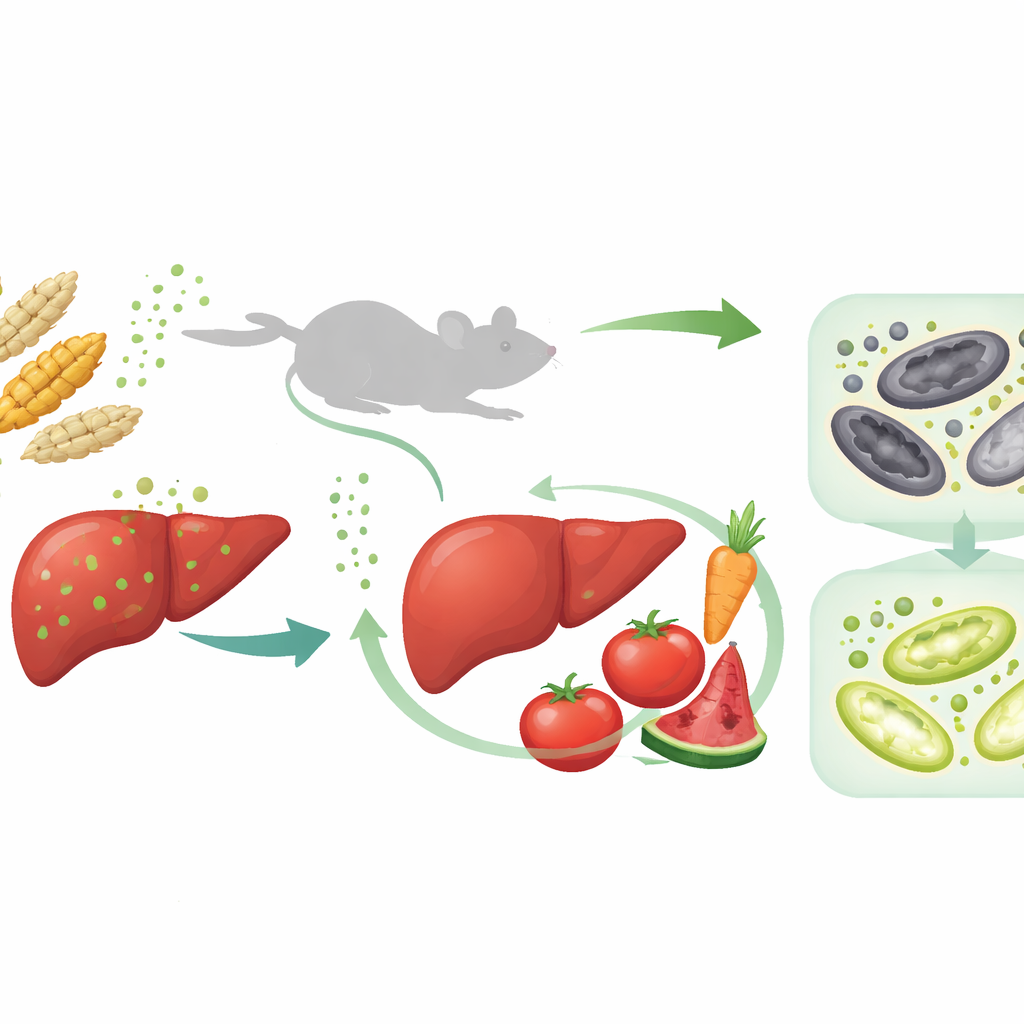
Wie das Toxin der Leber schadet
Die Forschenden fütterten Mäuse zunächst über vier Wochen mit abgestuften Dosen von T-2-Toxin, um eine andauernde diätetische Exposition zu simulieren. Mit steigenden Toxinmengen nahmen die Tiere weniger zu, ihre Lebern vergrößerten sich und wurden blassgelb, und Bluttests zeigten ansteigende Leberenzyme, die auf Verletzungen hinweisen. Unter dem Mikroskop wirkten Lebergewebe geschwollen und unstrukturiert, mit Vakuolen in Zellen und Anzeichen von Zelluntergang. Eine groß angelegte Proteinanalyse der Leberproben ergab, dass viele der am stärksten veränderten Signalwege mit Eisenstoffwechsel, Fettmetabolismus und einer spezifischen Form des Zelltods namens Ferroptose zusammenhängen, die durch Eisen und außer Kontrolle geratene Lipidoxidation angetrieben wird.
Eisenüberladung und ein rostähnlicher Zelltod
Tiefergehend maßen die Forschenden klassische Marker der Ferroptose. In toxinbelasteten Lebern stieg der Eisengehalt, während Moleküle, die Fettschäden anzeigen, zunahmen und die Aktivität eines wichtigen Schutz-Enzyms, GPx-4, sank. Proteine, die normalerweise Eisen sicher in Zellen speichern, nahmen zu, aber der wichtigste Eisen–"Exporteur" auf Leberzellen ging zurück, was darauf hindeutet, dass Eisen eingeschlossen wurde. Als die Wissenschaftler einigen Mäusen ein Medikament verabreichten, das speziell Ferroptose blockiert, verbesserten sich Leberstruktur und -funktion: Schwellungen verringerten sich, Verletzungswerte sanken und chemische Zeichen oxidativer Schäden gingen zurück. Das verband die Lebertoxizität des T-2-Toxins eindeutig mit einer eisengetriebenen, rostähnlichen Form des Zelltods.
Mitochondrien, Zellreinigung und ein Verteidigungsschalter
Das Team wandte sich dann den Mitochondrien zu — den Energiefabriken in Zellen, die sowohl Quelle als auch Ziel oxidativen Stresses sind. Bei toxinbehandelten Mäusen sank die mitochondriale Energieproduktion, während das Austreten von Cytochrom c und die Gesamtmenge reaktiver Sauerstoffspezies zunahmen; die Elektronenmikroskopie zeigte geschrumpfte, strukturell geschädigte Mitochondrien. Gleichzeitig wurde das Qualitätskontrollsystem der Zelle aktiviert — die Mitophagie, ein selektiver "Aufräum"-Prozess, der defekte Mitochondrien entfernt — über einen Pfad, an dem die Proteine PINK1 und Parkin beteiligt sind. Als die Forschenden Mäuse ohne Parkin verwendeten und somit keine normale Mitophagie aufbauen konnten, verursachte T-2-Toxin noch stärkere Eisenanlagerungen, ausgeprägtere Ferroptose-Signale und schwerwiegendere Leberschäden. Das zeigte, dass Mitophagie als schützende Bremse wirkt und durch Toxin verursachte Schäden begrenzt.
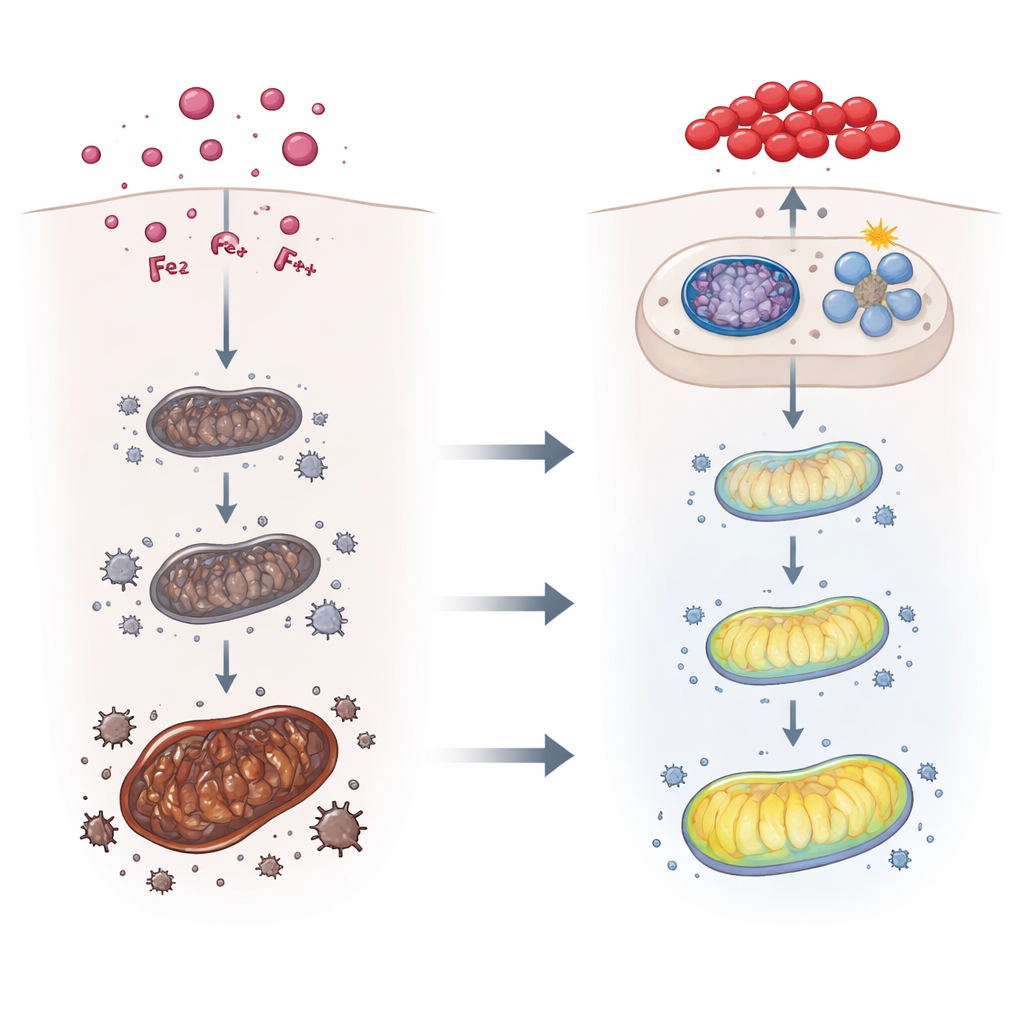
Ein eingebauter Schutzweg und die Rolle von Lycopin
Weil Eisenhaushalt, oxidativer Stress und Mitophagie miteinander verknüpft schienen, suchten die Autorinnen und Autoren nach einem übergeordneten Regulator und konzentrierten sich auf Nrf2, einen Master-Schalter, der Antioxidanzien- und Entgiftungsgene einschaltet. T-2-Toxin selbst aktivierte Nrf2 teilweise, doch als Mäusen eine bekannte Nrf2-aktivierende Verbindung verabreicht wurde, verbesserte sich der Leber-Eisenexport, fielen Ferroptose-Marker und nahm die Mitophagie zu — alles zusammen milderte die Wirkung des Toxins. Das Team prüfte dann, ob Lycopin als natürlicher Nrf2-Booster dienen könnte. Computermodelle deuteten darauf hin, dass Lycopin physisch sowohl an Nrf2 als auch an dessen Repressorprotein Keap1 binden kann, in einer Weise, die Nrf2-Aktivierung begünstigt. In lebenden Mäusen verbesserte eine Lycopin-Behandlung vor und während der Toxinexposition Körpergewicht, stellte das Leberbild und Blutwerte wieder her, verringerte Eisenanreicherung und oxidativen Schaden und aktivierte zusätzlich Nrf2 sowie den PINK1–Parkin-Mitophagie-Weg.
Was das für Lebensmittelsicherheit und Ernährung bedeutet
Kurz gesagt zeigt die Studie, dass T-2-Toxin die Leber schädigt, indem es überschüssiges Eisen in Zellen einschließt, Mitochondrien zerstört und Ferroptose auslöst. Der Körper reagiert, indem er Nrf2 und Mitophagie einschaltet, um beschädigte Mitochondrien zu entfernen und das Eisen wieder ins Gleichgewicht zu bringen, aber diese Abwehr kann überfordert werden. Lycopin scheint diese innere Schutzbarriere zu stärken, indem es der Leber hilft, Eisen zu exportieren, fehlerhafte Mitochondrien zu beseitigen und Ferroptose zu widerstehen. Zwar sind weitere Untersuchungen nötig, bevor sich diese Erkenntnisse auf den Menschen übertragen lassen, doch die Forschung legt nahe, dass bestimmte Pflanzenstoffe wie Lycopin eines Tages Teil von Strategien werden könnten, um die gesundheitlichen Folgen unvermeidbarer lebensmittelbedingter Toxine zu verringern.
Zitation: Yang, X., Song, W., Lu, Z. et al. Lycopene mitigates T-2 toxin-induced hepatic ferroptosis by targeting the Nrf2/mitophagy axis in mice. npj Sci Food 10, 94 (2026). https://doi.org/10.1038/s41538-026-00736-4
Schlüsselwörter: T-2-Toxin, Lycopin, Leberverletzung, Ferroptose, Mitophagie