Clear Sky Science · de
Optimierung von Muskel-Satellitenzellenquellen für kultiviertes Fleisch: Anatomische Herkunft beeinflusst zelluläre Eigenschaften und Qualitätsmerkmale
Warum es wichtig ist, Fleisch aus Zellen zu züchten
Kultiviertes Fleisch — Fleisch, das aus Tierzellen in Bioreaktoren statt auf Farmen gezüchtet wird — verspricht Steaks und Schnitzel mit deutlich geringerem Flächenbedarf, weniger Umweltverschmutzung und weniger Tierleid. Um diese Vision jedoch zu Supermarktprodukten zu machen, müssen Wissenschaftler zunächst die besten Zellen zum Wachsen finden. Diese Studie stellt eine überraschend einfache Frage mit weitreichenden Folgen: Verhalten sich Muskelstammzellen, die aus verschiedenen Körperregionen eines Schweins stammen — Hals, Rücken oder Bein — unterschiedlich, und könnte das Geschmack, Textur und Nährwert zukünftigen Labor-Schweinefleischs verändern?
Muskelzellen, die reparieren — und Fleisch aufbauen
In jedem Muskel gibt es sogenannte „Satellitenzellen“, eine Art Stammzelle, die beschädigtes Gewebe repariert und beim Muskelwachstum hilft. Dieselben Zellen sind die Arbeitspferde des kultivierten Fleisches: Sie müssen sich vielfach vermehren und anschließend zu Fasern verschmelzen, die echtem Muskel ähneln. Die Forschenden isolierten diese Satellitenzellen aus drei häufig verzehrten Schweinemuskeln: einem Halsaumuskeln, der der Haltung dient, einem Rückenmuskeln, aus dem beliebte Lendenstücke gewonnen werden, und einem Beinmuskel, der für Bewegung verantwortlich ist. Mit Zellsortier-Technologie reinigten sie die Satellitenzellen und bestätigten, dass alle drei Quellen unter dem Mikroskop ähnlich geformte, spindelförmige Zellen hervorbrachten. Allerdings unterschied sich die Zahl der gewinnbaren Satellitenzellen: Halsmuskeln lieferten am meisten, Rücken etwas weniger und Bein am wenigsten.
Gene behalten ihre Herkunft
Obwohl alle Zellen unter denselben Laborbedingungen kultiviert wurden, behielten ihre internen Genaktivitätsmuster weiterhin eine „Erinnerung“ an ihre ursprüngliche Körperstelle. Durch RNA-Sequenzierung — die Arbeitskopien der Gene — zeigten die Forschenden, dass Hals-, Rücken- und Beinzellen jeweils eigene Cluster bildeten, basierend darauf, welche Gene an- oder abgeschaltet waren. Ein zentraler Bestandteil dieses Unterschieds betraf HOX-Gene, eine Genfamilie, die während der Embryonalentwicklung den Körperplan festlegt. Halsabgeleitete Zellen exprimierten HOX-Gene, die mit Kopf- und Halsregionen verknüpft sind, während beinabgeleitete Zellen HOX-Gene bevorzugten, die mit Hintergliedmaßen assoziiert sind. Das deutet darauf hin, dass die positionsspezifische Identität aus der frühen Entwicklung in die Stammzellen für kultiviertes Fleisch hineinreicht und möglicherweise beeinflusst, wie sie wachsen und welche Art von Muskel sie bilden.
Wachstumsgeschwindigkeit versus Muskelqualität
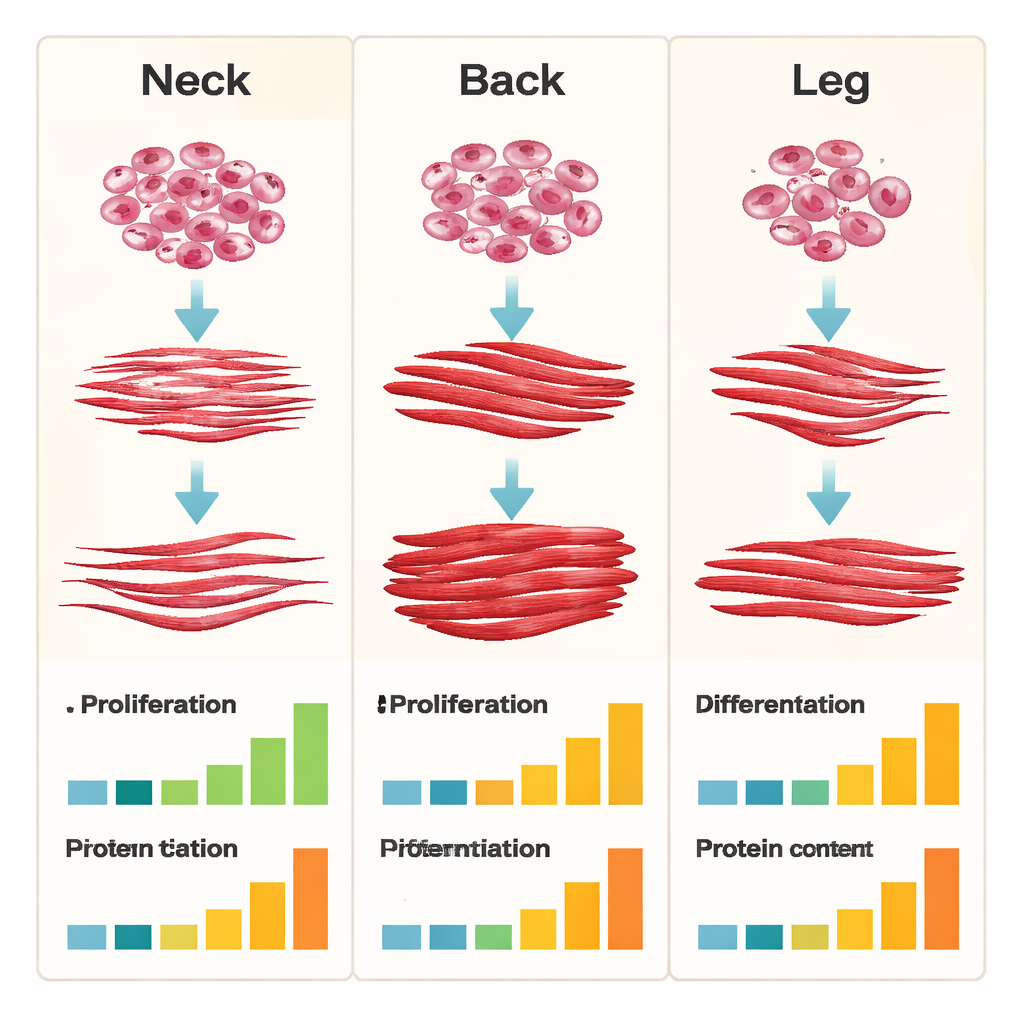
Für die großskalige Fleischproduktion sind zwei Eigenschaften entscheidend: wie schnell sich Zellen vermehren und wie gut sie zu ausgereiften Muskelfasern differenzieren. Halsabgeleitete Zellen punkteten bei der Proliferation. Über mehrere Wochen und Passagen in Kultur zeigten sie die höchsten Werte an Wachstumsmarkern und die stärkste Gesamtvermehrung, was sie attraktiv macht, um schnell große Zellmengen zu erzeugen. Wenn es jedoch an die Differenzierung — die Verschmelzung zu langen, faserartigen Strukturen — ging, stachen die rückengeleiteten Zellen hervor. Sie bildeten dickere, stärker verschmolzene Myotuben und behielten über Langzeitkulturen höhere Spiegel wichtiger Muskel-Differenzierungsgene bei. Beinabgeleitete Zellen hinkten sowohl in der Stammzellqualität als auch in der Differenzierung hinterher; ihre Fähigkeit, grundlegende Muskelstammzellmarker aufrechtzuerhalten und robuste Fasern zu bilden, nahm am schnellsten ab.
Fasertypen, Proteingehalte und Esserlebnis
Nicht alle Muskelfasern sind gleich. Slow-Twitch-Fasern sind eher auf Ausdauer ausgelegt, fettreicher und oxidative im Stoffwechsel und werden oft mit Zartheit und Saftigkeit in Verbindung gebracht. Fast-Twitch-Fasern sind auf schnelle Kraft spezialisiert und neigen dazu, magerer und proteinreicher zu sein. Die Forschenden fanden, dass halsabgeleitete Zellen eine Neigung zu Slow-Twitch-Fasergenen aufwiesen, während rückengeleitete Zellen preferential Fast-Twitch-Marker produzierten. Bei der Messung des Gesamtproteingehalts nach der Differenzierung hatten die rückengeleiteten Kulturen den höchsten Proteingehalt, während die halsabgeleiteten Kulturen den niedrigsten aufwiesen. Diese Unterschiede deuten darauf hin, dass die Ausgangszellquelle künftiges kultiviertes Fleisch in Richtung weicherer, möglicherweise reichhaltigerer Stücke (durch Slow-Twitch‑begünstigende Zellen) oder magererer, proteinreicher Produkte (durch Fast-Twitch‑begünstigende Zellen) abstimmen könnte.
Gestaltung besserer kultivierter Schweineprodukte
Für Nichtfachleute lautet die Kernbotschaft: „Woher man die Zellen nimmt“ ist wirklich wichtig für im Labor gezüchtetes Fleisch. Halsmuskelstammzellen sind exzellent, um Zellzahlen schnell aufzubauen, während rückengeleitete Zellen besser darin sind, zu dicken, proteinreichen Muskelfasern zu reifen und ihre Muskelidentität über viele Teilungsrunden hinweg zu bewahren. Beinabgeleitete Zellen tragen in beiden Bereichen weniger bei. Die Autorinnen und Autoren schlagen vor, dass rückengeleitete Satellitenzellen das beste Gesamtgleichgewicht für die Produktion von kultiviertem Schweinefleisch bieten, dass jedoch Mischungen von Quellen es Produzenten ermöglichen könnten, Textur, Nährwert und Geschmack zu individualisieren. Mit anderen Worten: Die kultivierten Koteletts von morgen könnten von Grund auf am Zellniveau konstruiert werden — beginnend mit dem richtigen Stück des Schweins.
Zitation: Lee, J., Park, J., La, H. et al. Optimizing muscle satellite cell sources for cultured meat: anatomical origin influences cellular properties and quality attributes. npj Sci Food 10, 56 (2026). https://doi.org/10.1038/s41538-026-00706-w
Schlüsselwörter: kultiviertes Fleisch, Muskelstammzellen, Schweine-Satellitenzellen, Fleischtextur, nachhaltiges Protein