Clear Sky Science · de
Aus dem Fett gewonnene Zweifachzelltherapie fördert Arteriogenese und Gliederhalt durch vaskuläre Integration bei kritischer Gliedmaßenischämie
Gliedmaßen retten durch Neubildung von Blutgefäßen
Wenn sich Arterien in den Beinen langsam zusetzen, können Menschen quälende Schmerzen, hartnäckige Geschwüre entwickeln und sogar eine Amputation drohen. Dieses schwere Stadium, als kritische Gliedmaßenischämie bezeichnet, ist besonders schwer zu behandeln, weil viele Patientinnen und Patienten nicht für Bypass-Operationen oder andere Standardverfahren infrage kommen. Die hier zusammengefasste Studie untersucht eine neue Strategie: zwei Arten von stammzellähnlichen Zellen aus dem eigenen Fettgewebe des Patienten zu verwenden, damit der Körper robuste neue Blutgefäße wachsen lässt, die das unterversorgte Gewebe retten können.
Eine verbreitete Erkrankung mit begrenzten Optionen
Die periphere arterielle Verschlusskrankheit entsteht, wenn sich Arterien in den Beinen verengen und den Blutfluss einschränken. In ihrer schwersten Form, der kritischen Gliedmaßenischämie, leiden Betroffene oft unter dauernden Schmerzen, schwarz verfärbten Zehen und einem hohen Risiko, einen Teil der Gliedmaße zu verlieren. Aktuelle Therapien wie cholesterinsenkende Medikamente, Angioplastie oder chirurgischer Bypass können helfen, doch viele Patientinnen und Patienten sprechen nicht ausreichend darauf an oder sind für diese Eingriffe zu krank. Frühere Versuche mit einzelnen Stammzelltypen förderten meist fragile, winzige Gefäße, die nicht genügend Durchfluss liefern, um die Gliedmaße zuverlässig zu retten. Deshalb wollten die Forschenden ein kompletteres „Ersatzleitungsnetz“ aufbauen, indem sie zwei kooperierende Zelltypen kombinierten.
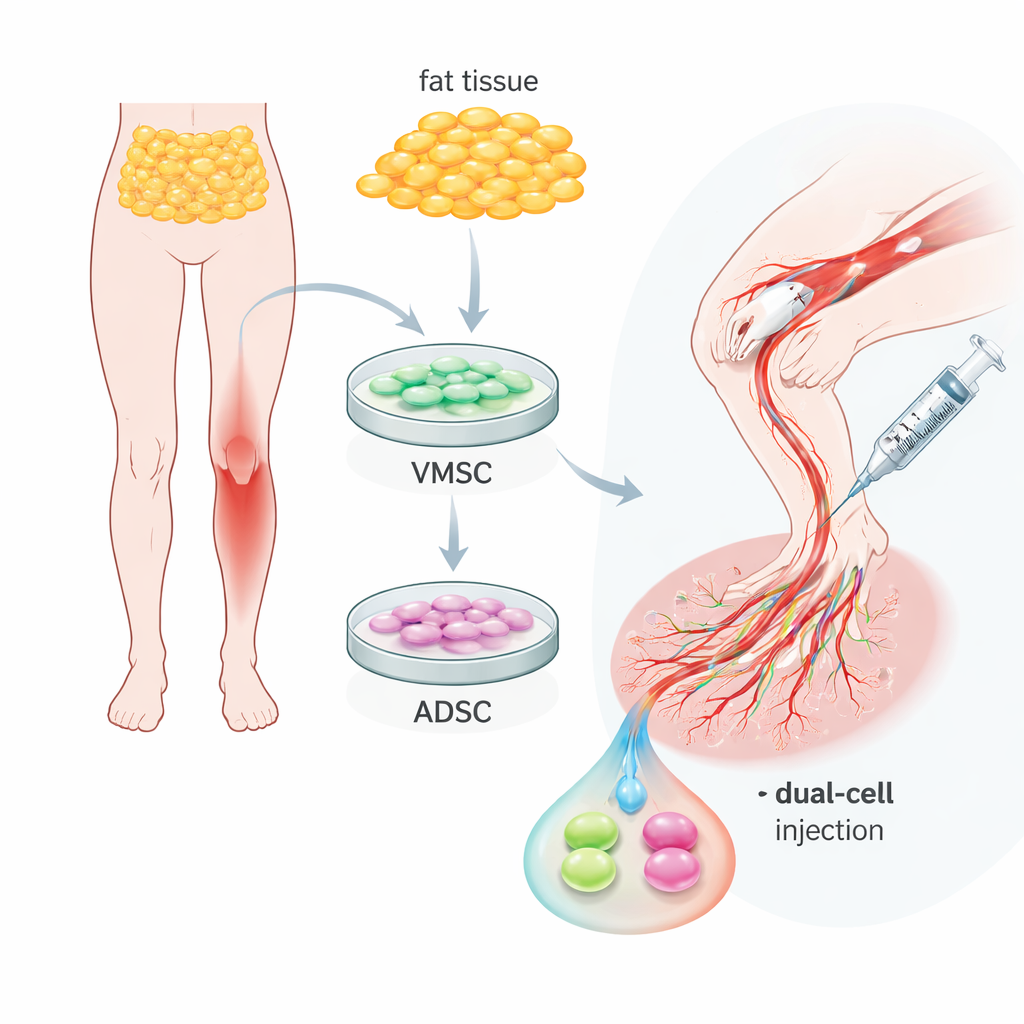
Zwei nützliche Zelltypen im gewöhnlichen Körperfett
Das Team konzentrierte sich auf das Fettgewebe – gewöhnliches Körperfett –, das sich mit vergleichsweise geringfügigen Eingriffen entnehmen lässt. Aus derselben Probe isolierten sie zwei verwandte, aber unterschiedliche Zellpopulationen. Die eine Gruppe, als vaskuläre multipotente Stammzellen bezeichnet, verhielt sich ähnlich wie frühe Endothelzellen: Sie trugen Oberflächenmarker, die für Endothelzellen typisch sind, und konnten in Zellkulturen kapillarähnliche Röhren ausbilden. Die zweite Gruppe, adipös abgeleitete Stammzellen, ähnelte eher Stützzellen, die Gefäße umgeben, und trug Marker, wie sie in glatten Muskel- und perivaskulären Zellen vorkommen. Beide Typen teilten sich gut und konnten sich in Fett-, Knochen- oder Knorpelzellen differenzieren, was ihre Vielseitigkeit bestätigte, doch ihre natürlichen Rollen rund um Blutgefäße waren eindeutig verschieden und komplementär.
Gemeinsames Wirken unter Stress
Um die harsche, entzündete Umgebung einer kranken Gliedmaße nachzuahmen, setzten die Forschenden die Zellen einem starken Entzündungssignal aus. Beide Zelltypen überlebten und passten ihr Verhalten an, indem sie Gemische aus Wachstumsfaktoren und Enzymen freisetzten, die Zellmigration und die Umgestaltung des umgebenden Gewebes fördern. Wuchsen die endothelähnlichen Zellen allein auf einem Gel, das Gefäßbildung begünstigt, konnten sie Grundröhren bilden, während sich die Stützzellen überwiegend verklumpten. Wurden sie jedoch im Verhältnis zwei zu eins gemischt, wurden die Röhren dichter, durchgängiger und widerstandsfähiger gegenüber entzündlichem Stress. Das deutet darauf hin, dass die beiden Zelltypen zusammen nicht nur mehr Gefäße bilden, sondern reifere und stabilere Netzwerke.
Prüfung der Zweifachzelltherapie in kranken Mausgliedmaßen
Die Forschenden gingen dann zu einem Mausmodell der kritischen Gliedmaßenischämie über, das durch Unterbindung einer Hauptbeinarterie erzeugt wurde. In den unterversorgten Beinmuskel injizierten sie die gemischten menschlichen Zellen. Über vier Wochen verloren unbehandelte Mäuse häufig Zehen oder ganze Füße, und ihre Muskeln zeigten Narbenbildung und starke Entzündung. Im Gegensatz dazu behielten die Tiere, die die Zweifachzellbehandlung erhielten, größtenteils ihre Gliedmaßen. Durchblutungsmessungen zeigten, dass die Zirkulation in behandelten Beinen auf etwa 70 Prozent des Normalwerts zurückkehrte, verglichen mit weniger als 20 Prozent in den Kontrollen. Mikroskopische und dreidimensionale Bildgebung erklärten warum: In behandelten Muskeln fanden sich deutlich mehr mittelgroße und große Gefäße – arterioolenähnliche Verzweigungen – mit starken ‚Ärmeln‘ aus Stützzellen, statt nur eines Netzwerks aus winzigen, instabilen Kapillaren.
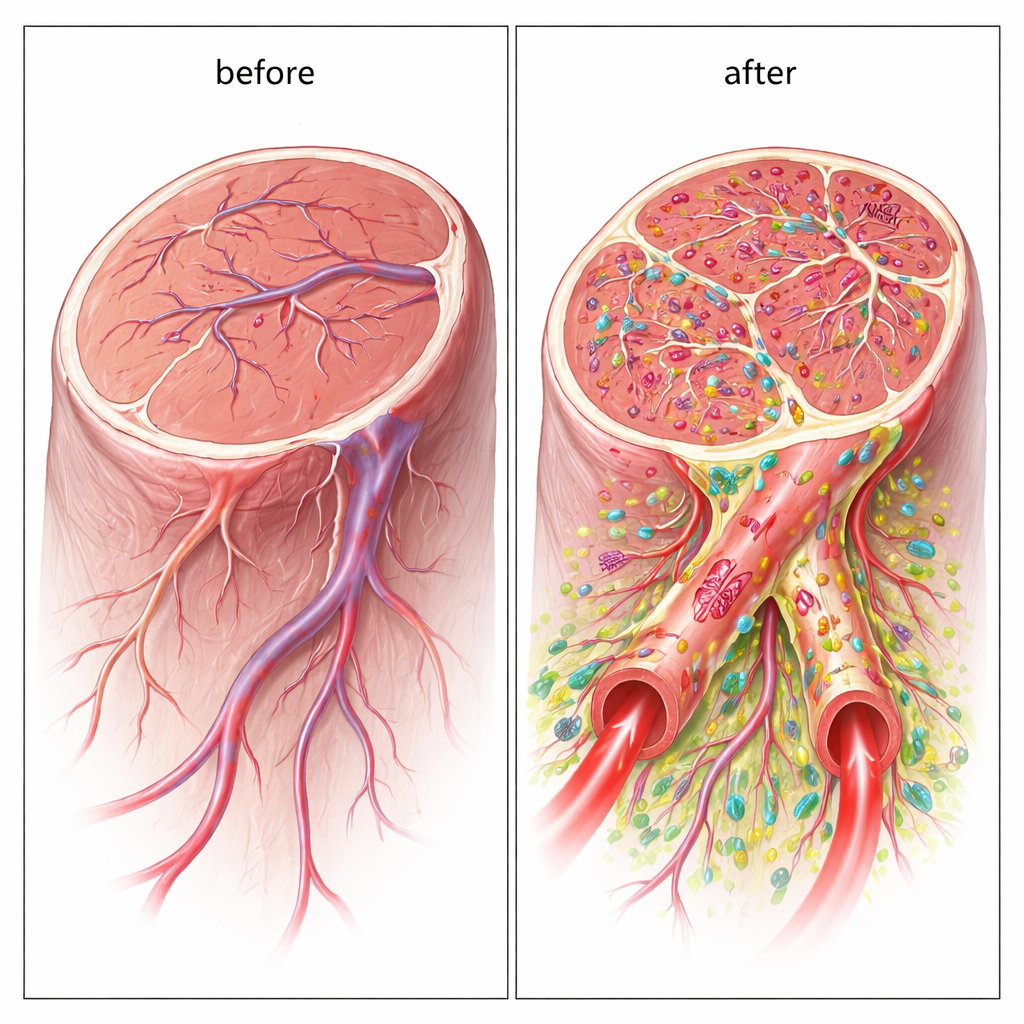
Hybride Gefäße aus Spenderzellen
Wichtig ist, dass die neuen Gefäße nicht nur indirekt durch Signale angeregt wurden; sie enthielten tatsächlich die transplantierten menschlichen Zellen als Teil ihrer Wand. Mit human-spezifischen Markern zeigten die Forschenden, dass die endothelähnlichen Zellen zur Bildung der inneren Auskleidung beitrugen, während die Stützzellen sich außen anschlossen. Viele dieser hybriden Gefäße waren breit genug, um als funktionstüchtige Blutleiter zu dienen, und fluoreszierende Tracer bestätigten, dass Blut hindurchfloss. Dieses direkte Bauen großer, perfundierter Gefäße unterscheidet den Zweifachzellansatz von den meisten bisherigen Stammzelltherapien, die hauptsächlich auf chemische Signale statt auf langfristige strukturelle Integration setzen.
Was das für Patientinnen und Patienten bedeuten könnte
Für Nicht-Spezialisten lautet die Botschaft: Forschende lernen möglicherweise, wie man sterbende Gliedmaßen mithilfe der eigenen, aus Fett gewonnenen Zellen „neu verkabelt“. Durch die Kombination zweier Zelltypen – einer, der das innere Rohr bildet, und einer, die die äußere Unterstützung aufbaut – erzeugt die Therapie starke, gut ausgekleidete Arterien und Arteriolen statt fragiler Sprosse. Bei Mäusen reichte dies aus, um den Blutfluss wiederherzustellen und den Verlust der Gliedmaße zu verhindern. Zwar sind weitere Arbeiten nötig, um Langzeitsicherheit und Wirksamkeit beim Menschen zu belegen, doch die Studie weist auf eine Zukunft hin, in der eine minimalinvasive Fettentnahme maßgeschneiderte Zellmischungen liefern könnte, um die Durchblutung bei amputationgefährdeten Patientinnen und Patienten wiederaufzubauen.
Zitation: Kim, D.Y., Hwang, D.Y., Park, G. et al. Adipose-derived dual cell therapy enhances arteriogenesis and limb preservation through vascular integration in critical limb ischemia. npj Regen Med 11, 13 (2026). https://doi.org/10.1038/s41536-026-00458-x
Schlüsselwörter: kritische Gliedmaßenischämie, Stammzelltherapie, aus Fett gewonnene Zellen, Neovaskularisation, periphere arterielle Verschlusskrankheit