Clear Sky Science · de
Neuartiges Kupfer‑ionen-koordiniertes Andrographolid-beladenes Hydrogel aktiviert die Rac1/JNK1‑Achse zur Verbesserung der Heilung diabetischer Wunden
Warum hartnäckige Wunden wichtig sind
Für viele Menschen mit Diabetes kann eine kleine Blase am Fuß sich zu einer chronischen Wunde auswachsen, die sich nicht schließt und im schlimmsten Fall eine Amputation nach sich zieht. Diese schwer heilenden Läsionen werden durch Infektionen, anhaltende Entzündungen und schlechte Durchblutung begünstigt. Die hier zusammengefasste Studie beschreibt ein neues gelartiges Verbandsmaterial, das alle drei Probleme zugleich angehen will, indem es eine Pflanzenverbindung und ein Spurenelement nutzt, um geschädigte Haut wieder in Richtung gesunder Reparatur zu lenken.
Ein intelligenter Verband aus Hydrogel
Die Forschenden entwickelten ein weiches, wasserreiches Material, bekannt als Hydrogel, das direkt auf der Wunde platziert wird. Es besteht aus Gelatine (einem aus Kollagen gewonnenen Protein) und einer modifizierten Form von Chitosan, einem zuckerbasierten Polymer. Kupferionen wirken wie winzige Verknüpfungen, die die Komponenten zu einem flexiblen Netzwerk verbinden und gleichzeitig das Pflanzenmolekül Andrographolid binden, das für seine entzündungshemmenden, antimikrobiellen und blutzuckersenkenden Eigenschaften bekannt ist. Diese Kupfer‑Koordination verbessert die Wasserlöslichkeit des Wirkstoffs erheblich und ermöglicht es, ihn gleichmäßig im Gel zu halten anstatt als Kristalle zu verklumpen — entscheidend für eine gleichmäßige Freisetzung in die Wunde.
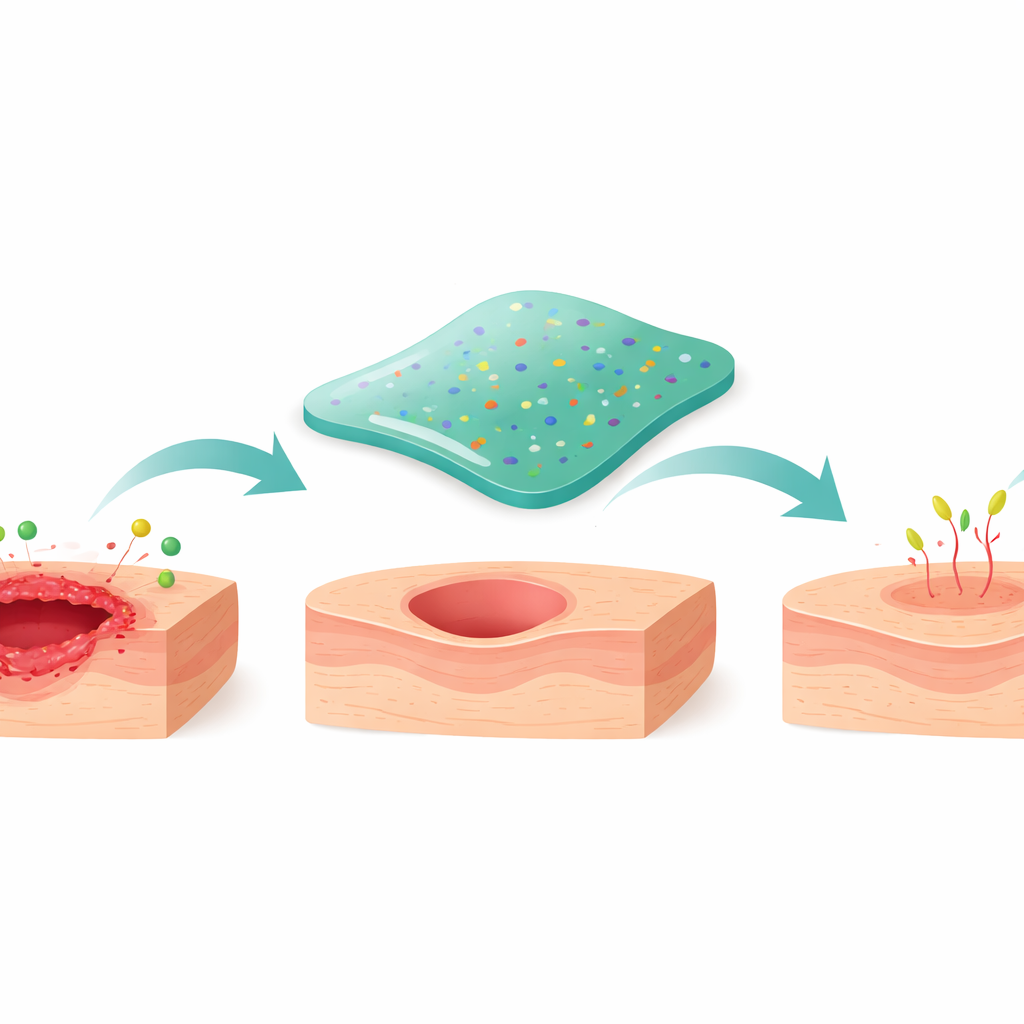
Gezielt so gestaltet, dass es haften bleibt und sich selbst repariert
Ein Wundverband muss an nasser, sich bewegender Haut haften, Flüssigkeit aufnehmen und dabei intakt bleiben. Detaillierte physikalische Tests zeigten, dass die optimierte Version des Gels (ASFH‑L genannt) sich wie ein weicher Feststoff verhält: Es kann sich verformen, um die Wundoberfläche anzupassen, widersteht aber dem Fließen. Unter dem Mikroskop zeigt es eine miteinander verbundene Porenstruktur, groß genug, damit Nährstoffe und Zellen hindurchwandern können, aber nicht so locker, dass es zerfällt. Wenn es gedehnt oder kurzzeitig beschädigt wird, bilden sich die kupferbasierten Verbindungen wieder, was dem Hydrogel eine „selbstheilende“ Fähigkeit verleiht, so dass ein zerschnittenes Stück innerhalb von Minuten wieder zusammenwächst. Auf feiner Schweinehaut blieb ASFH‑L bei wiederholtem Biegen und Drehen unter Wasser haften, was darauf hindeutet, dass es echte Wunden schützen kann, ohne ständig neu angewendet werden zu müssen.
Gegen Keime und zur Unterstützung der Zellmigration
Chronische diabetische Wunden sind oft von Bakterien besetzt. In Labortests gegen häufige Erreger wie Staphylococcus aureus und Escherichia coli verlangsamten alle Hydrogel‑Varianten das Bakterienwachstum, und jene mit mehr Andrographolid erzeugten größere Hemmzonen. Zugleich waren Extrakte aus ASFH‑L schonend zu menschlichen Hautzellen: Sie erhielten deren Lebensfähigkeit und förderten bei geeigneter Dosis sogar ihr Wachstum über 24 Stunden. Wurden Hautzellen unter hochzuckerigen Bedingungen kultiviert, die normalerweise ihre Wanderungsfähigkeit dämpfen, unterstützten die Hydrogelextrakte ihre Migration in Kratzlücken. Dieser Mobilitätsgewinn ist wichtig, denn das Verschließen einer Wunde hängt davon ab, dass Hautzellen zur Bedeckung der freiliegenden Fläche kriechen.
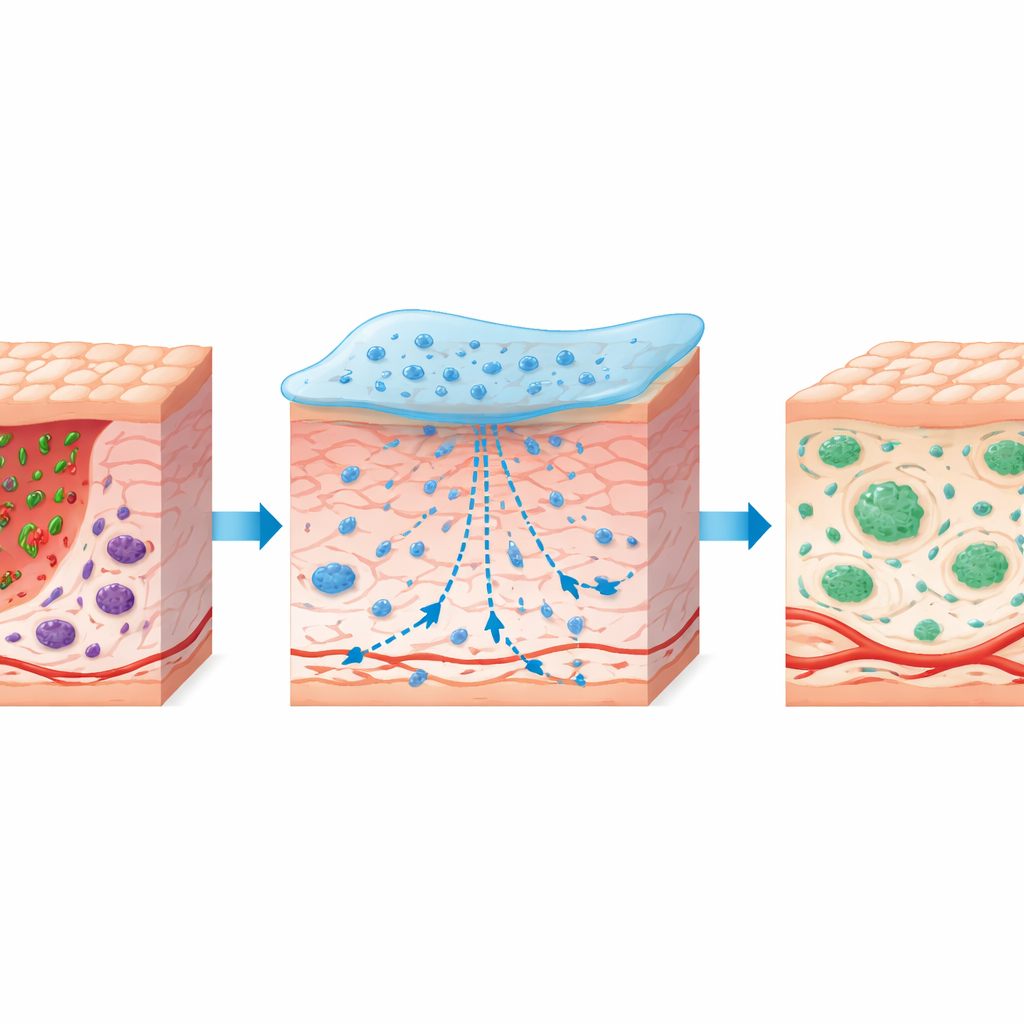
Den Körper von Entzündung zur Reparatur lenken
Bei diabetischen Mäusen mit kreisrunden Rückenhauten beschleunigte das ASFH‑L‑Hydrogel die Wundschließung im Vergleich zu unbehandelten Kontrollen und zu einem ähnlichen Gel ohne Pflanzenwirkstoff. Behandelte Wunden zeigten eine dickere neue Oberhaut, geordneter verlaufende Kollagenfasern und sogar das Nachwachsen von Haarfollikeln. Blutflussaufnahmen und Gewebefärbungen offenbarten dichtere Netzwerke kleiner Blutgefäße und mehr stützende muskelähnliche Zellen in deren Umgebung, was auf eine bessere Nährstoffversorgung hindeutet. Auf immunologischer Ebene veränderte der Verband das Verhalten von Makrophagen — den vordersten Abwehrzellen, die entweder Entzündungen anheizen (M1‑Typ) oder sie dämpfen und den Wiederaufbau unterstützen (M2‑Typ). ASFH‑L verringerte die pro‑entzündliche M1‑Population und vergrößerte die pro‑heilende M2‑Gruppe, während es schädliche Signale wie IL‑1β und TNF‑α senkte und den beruhigenden Botenstoff IL‑10 erhöhte. Diese koordinierte Verschiebung spiegelt den natürlichen Übergang von einer frühen „Aufräumphase“ hin zur echten Gewebereparatur wider, der bei diabetischen Wunden oft ins Stocken gerät.
Ein molekularer Schalter für Heilung
Um zu verstehen, wie eine Pflanzenverbindung in einem Gel diese Effekte steuern kann, nutzte das Team Computer‑Modellierung, Datenbankauswertung und biophysikalische Messungen. Sie fanden heraus, dass Andrographolid direkt an ein kleines Signalmolekül namens Rac1 binden kann und darüber eine Kaskade von Molekülen (JNK1, Jun und Fos) aktiviert, die gemeinsam Zellbewegung, Wachstum, Entzündung und Neubildung von Gefäßen regulieren. Simulationen zeigten eine stabile, energetisch günstige Bindung zwischen Andrographolid und Rac1, und oberflächenbasierte Experimente bestätigten diese Wechselwirkung in Echtzeit. In den Mauswunden waren Gene und Proteine entlang dieser Rac1/JNK1/Jun/Fos‑Achse in der Hydrogel‑Gruppe stärker aktiviert. Einfach ausgedrückt: Der Verband bedeckt die Wunde nicht nur — er liefert einen botanischen Wirkstoff, der einen eingebauten Reparaturschalter in den Zellen umlegt.
Was das für Patientinnen und Patienten bedeuten könnte
Diese Arbeit stellt einen „intelligenten“ Verband vor, der Infektionskontrolle, Immunberuhigung und Gefäßneubildung in einer selbstheilenden Hydrogelplattform vereint. Durch die Nutzung von Kupferionen, um Andrographolid zu lösen und langsam freizusetzen, macht das Material eine schwer zu verabreichende Pflanzenverbindung zu einer praktikablen lokalen Therapie. In diabetischen Tieren beschleunigt dieser Ansatz die Wundschließung, ordnet Narbengewebe und stellt das immunologische Gleichgewicht wieder her — und das alles über eine definierte molekulare Signalstrecke. Obwohl klinische Studien am Menschen noch nötig sind, deutet das Konzept auf künftige Verbände hin, die weit mehr tun als eine Wunde zu bedecken — sie begleiten geschädigtes Gewebe aktiv durch die einzelnen Schritte der Heilung.
Zitation: Ye, P., Dai, Y., Zhang, Q. et al. Novel copper-ion coordinated andrographolide-loaded hydrogel activates Rac1/JNK1 axis for enhancing diabetic wound healing. npj Regen Med 11, 14 (2026). https://doi.org/10.1038/s41536-026-00457-y
Schlüsselwörter: Heilung diabetischer Wunden, Hydrogel‑Verbandsmaterial, Andrographolid, Makrophagen‑Polarisation, Angiogenese