Clear Sky Science · de
Hemmung von CDK8 rettet beeinträchtigte ischämische Frakturheilung
Warum Blutfluss wichtig ist, wenn Knochen brechen
Die meisten gebrochenen Knochen verbinden sich schließlich wieder, doch bei Millionen Menschen jährlich bleibt dieser Prozess aus. Schlechte Durchblutung rund um einen Bruch — bekannt als Ischämie — erhöht dramatisch das Risiko, dass ein Bruch langsam, mangelhaft oder gar nicht heilt. Diese Studie untersucht, warum das auf zellulärer Ebene passiert, und testet eine experimentelle Tablette, die den Körper offenbar von einer narbenähnlichen Reparatur hin zu echter Knochenregeneration lenken kann.
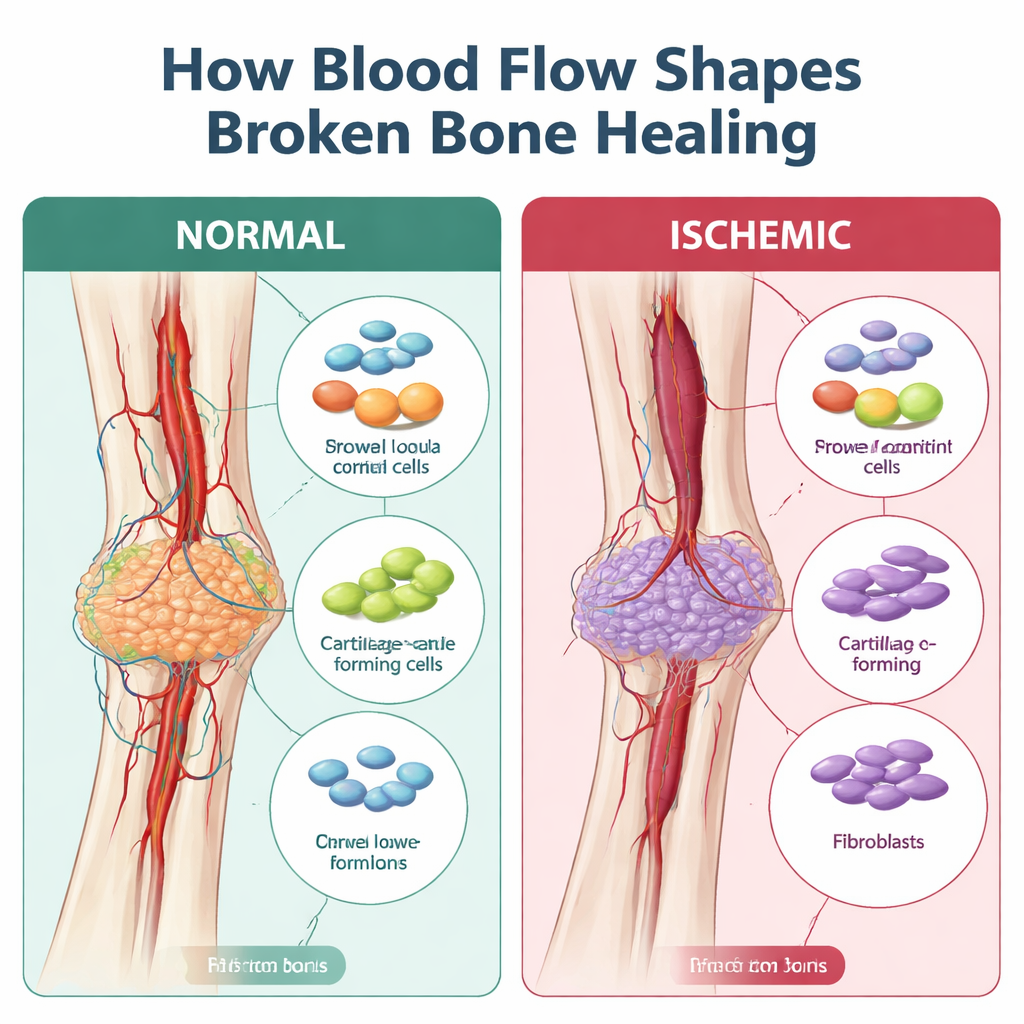
Wenn Heilung zur Narbenbildung statt zum Wiederaufbau wird
Knochen heilen normalerweise, indem zunächst eine weiche Knorpelbrücke gebildet wird, die allmählich durch harten Knochen ersetzt wird. Diese Brücke, der Kallus, ist auf eine Versorgung mit stammesähnlichen Stütz- (Stromal-)Zellen, Immunzellen und Blutgefäßen angewiesen, die die Reparatur koordinieren. Bei ischämischen Frakturen zeigte frühere Forschung, dass der Kallus tendenziell kleiner, schwächer und mit faserigem Gewebe gefüllt ist — eher eine Narbe als ein stabiler neuer Knochen. Es fehlte jedoch eine detaillierte Karte, welche Zellen wann auf dem Weg von korrekter Heilung abweichen.
Einzelzellen machen den Umweg zur Fibrose sichtbar
Die Forschenden verwendeten ein Mausmodell, bei dem eine Beinarterie zum Zeitpunkt des Bruchs chirurgisch geschädigt wird und damit den Blutverlust nachahmt, wie er bei schweren Verletzungen oder bei Menschen mit Gefäßerkrankungen oder Rauchern vorkommt. Anschließend setzten sie Einzelzell-RNA-Sequenzierung ein, eine Methode, die die aktiven Gene in Tausenden einzelner Zellen ausliest, auf Frakturkallusse vier und sieben Tage nach der Verletzung. In gut durchbluteten Frakturen war der frühe Kallus voller Immunzellen, die bald von expandierenden Stromalzellen — den Stützzellen, die zu Knorpel und Knochen werden — abgelöst wurden. Unter ischämischen Bedingungen gab es dagegen deutlich weniger knorpel- und knochenbildende Zellen und deutlich mehr Fibroblasten, also Zellen, die faseriges Gewebe ablagern. Rechnergestützte „Trajectory“-Analysen zeigten, dass sich Stromalzellen im ischämischen Knochen oft über einen fibroblastenähnlichen Zustand umleiteten, anstatt sich glatt von frühen Vorläufern in Knorpel zu entwickeln — ein Befund, der zum mikroskopisch sichtbaren narbenähnlichen Kallus passt.
Eine molekulare Bremse auf knochenbildenden Zellen
Bei der Untersuchung der Genaktivität dieser Zellen entdeckte das Team ein starkes Signal zellulären Stresses in ischämischen Kallussen, darunter hohe Spiegel von Hitzeschockproteinen. Zu den auffälligsten Änderungen gehörte ein Anstieg der Aktivität eines Gens namens Cdk8, das für ein regulatorisches Enzym kodiert, das Teil eines wichtigen Transkriptionskomplexes ist und die Reaktion von Zellen auf Signale bremsen oder umlenken kann. Cdk8 ist in anderen Kontexten bereits dafür bekannt, die Zelldifferenzierung zu blockieren. Hier war es besonders in frühen Stromalvorläufern im ischämischen Knochen erhöht. Auch menschliche mesenchymale Stromalzellen, die in sauerstoffarmen Laborbedingungen — als Modell für mangelhafte Durchblutung — gezüchtet wurden, steigerten CDK8, was einen direkten Zusammenhang zwischen Sauerstoffmangel und dieser potenziellen „Bremse“ für Knorpel- und Knochenbildung herstellt.
CDK8 ausschalten, um die Reparatur zu retten
Als Nächstes fragten die Forschenden, ob die Blockade von CDK8 Stromalzellen freimachen könnte, damit sie die richtige Heilung wieder aufnehmen. In Zellkulturen stärkten selektive CDK8-Inhibitoren bei Maus- und menschlichen Vorläuferzellen wichtige Knorpelgene und erhöhten die Produktion von Knorpelmatrix; außerdem förderten sie die Mineralisierung, wenn dieselben Zellen in Richtung Knochenbildung getrieben wurden. Das Team testete dann einen oral verabreichten CDK8/19-Inhibitor namens SNX631-6 in Mäusen mit ischämischen Frakturen. Wurde das Mittel während des frühen, knorpelbildenden Zeitfensters gegeben, nahm die Menge an Knorpel im Kallus zu. Wurde die Behandlung in die spätere Übergangsphase von Knorpel zu Knochen verlängert, zeigten die Kallusse insgesamt mehr Knochen, einen höheren Mineralgehalt und größere Gesamtgrößen in Mikro-CT-Scans und Gewebeschnitten — Anzeichen für eine robustere strukturelle Reparatur.
Von Laborbefunden zu möglichen neuen Therapien
In der Summe deuten die Ergebnisse darauf hin, dass Ischämie Heilungszellen teilweise durch Hochregulierung von CDK8 in einen gestressten, fibrotischen Zustand lenkt, der ihre Fähigkeit zur Differenzierung in Knorpel und Knochen einschränkt. Die Blockade dieses Enzyms scheint diese Bremse zu lösen, sodass früh mehr Knorpel gebildet und später mehr Knochen aufgebaut wird — selbst bei eingeschränkter Blutversorgung. Da CDK8-Inhibitoren bereits bei Krebspatienten erprobt werden, könnten sie eines Tages umgenutzt werden, um Menschen mit hohem Risiko für schlechte Bruchheilung — etwa ältere Erwachsene, Raucher oder Personen mit Gefäßerkrankungen — zu helfen, starken Knochen statt fragiler Narbenbildung wiederzubilden.
Zitation: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
Schlüsselwörter: Heilung von Knochenbrüchen, Ischämie, CDK8-Inhibitor, mesenchymale Stromalzellen, Fibrose