Clear Sky Science · de
Einnistung wildtypischer alveolärer Typ‑II‑Epithelzellen in Surfactant‑Protein‑C‑defizienten Mäusen
Warum die Reparatur winziger Lufträume wichtig ist
Atmen erscheint mühelos, beruht aber auf einem feinen Film namens Surfactant, der die Millionen winziger Lufträume in unseren Lungen auskleidet. Fehlt dieses Surfactant oder ist es fehlerhaft, wie bei einigen seltenen Lungenerkrankungen im Kindesalter, leiden Kinder an anhaltenden Atemproblemen und an einer Vernarbung der Lunge. Heute ist die einzige echte Heilung die Lungentransplantation, eine Option, die durch Spenderknappheit und erhebliche Risiken begrenzt ist. Diese Studie untersucht einen anderen Ansatz: beschädigte Lungen durch die Transplantation gesunder, Surfactant produzierender Zellen zu reparieren und damit möglicherweise sanftere, zielgerichtetere Behandlungen zu ermöglichen.
Wenn die Hüter der Lunge versagen
In jedem Luftraum (Alveolus) sitzen spezialisierte „Hüter“-Zellen, die sogenannten alveolären Typ‑II‑Zellen. Sie stellen Surfactant her und recyceln es, womit sie verhindern, dass die Lufträume kollabieren, und das Atmen erleichtern. Bei manchen Kindern stören Mutationen in Genen, die für die Surfactantproduktion erforderlich sind, darunter das Gen für Surfactant‑Protein C (SFTPC), diese Zellen. Das Ergebnis ist eine interstitielle Lungenerkrankung im Kindesalter (chILD), gekennzeichnet durch entzündetes, verdicktes Lungengewebe, Vernarbung und manchmal Atemversagen. Ärztinnen und Ärzte können nur unterstützende Medikamente und Sauerstoff anbieten; für die schwerstbetroffenen Patienten bleibt die Lungentransplantation das letzte Mittel. Die Autorinnen und Autoren wollten prüfen, ob das Ersetzen eines Teils der fehlerhaften Hüterzellen durch gesunde Zellen die Lungenschädigung verlangsamen oder rückgängig machen kann.
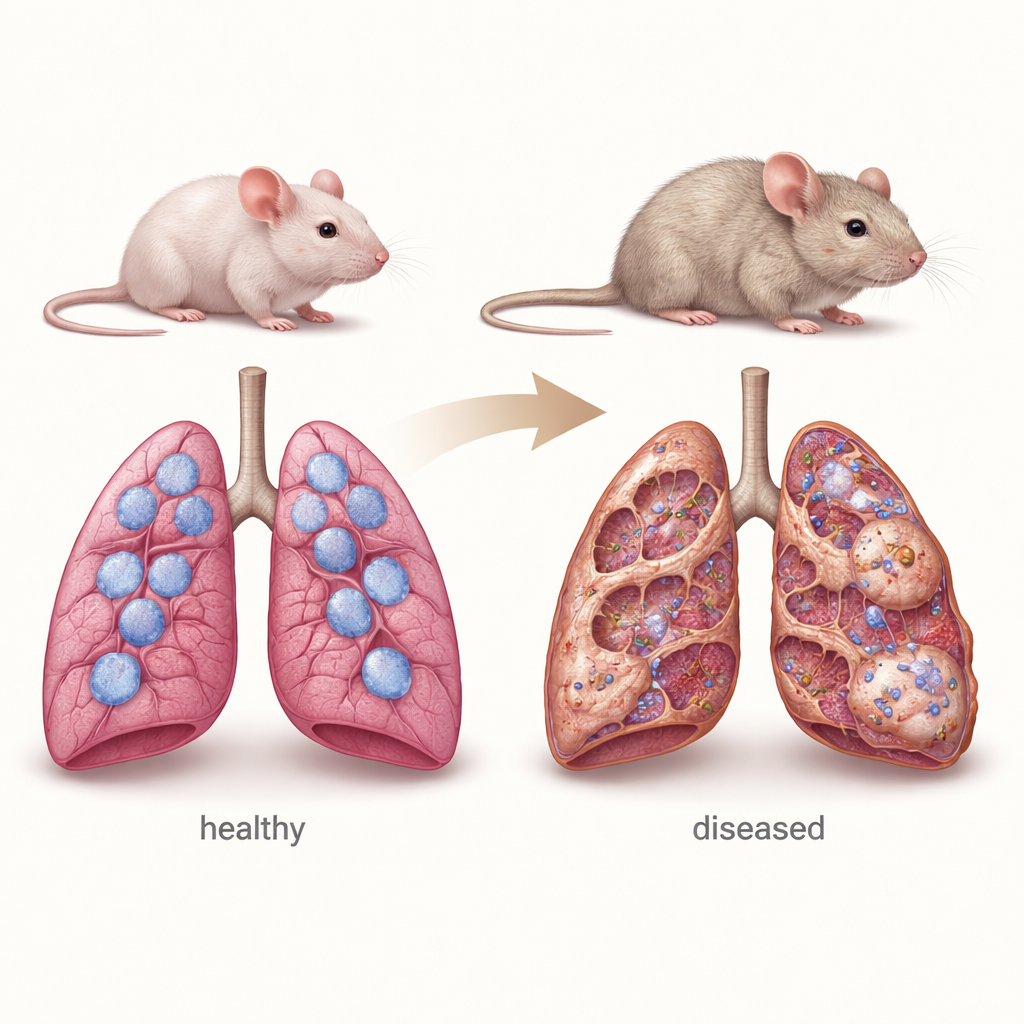
Ein Mäusemodell für die Lungenerkrankung von Kindern
Um zentrale Merkmale von chILD nachzuahmen, verwendeten die Forschenden Mäuse, denen das Sftpc‑Gen vollständig fehlte. Diese Tiere werden mit offenbar normalen Lungen geboren, entwickeln aber im Lauf des Alterns Kennzeichen chronischer Lungenerkrankung: verdickte Wände zwischen den Alveolen, zusätzliches narbiges Gewebe mit reichem Kollagenanteil, eine Vermehrung der Typ‑II‑Zellen und eine Anhäufung von Immunzellen. Detaillierte Messungen zeigten, dass sich ihre Lungenarchitektur zwischen dem 4. und 12. Lebensmonat stetig verschlechtert, ähnlich dem langsamen Fortschreiten, das viele menschliche Patienten zeigen. Das Team fand außerdem, dass diese Mäuse ungewöhnlich empfindlich gegenüber dem Chemotherapeutikum Bleomycin sind, das im Labor häufig verwendet wird, um Lungenschädigung und Fibrose zu induzieren, was die Verwundbarkeit ihrer surfactant‑defizienten Lungen zusätzlich unterstreicht.
Beschädigte Lungen für neue Zellen vorbereiten
Neue Zellen erfolgreich in ein bereits dicht besiedeltes Organ zu transplantieren, ist nicht trivial. Die Autorinnen und Autoren prüften, ob eine sorgfältig gewählte Niedrigdosis Bleomycin als eine Art „Konditionierungsbehandlung“ wirken könnte—einige der defekten residenten Zellen schädigen und Platz für Neuzugänge schaffen, ohne die Lunge zu zerstören. Bei Sftpc‑defizienten Mäusen verschlechterten selbst kleine Mengen Bleomycin die Vernarbung und senkten die Spiegel mehrerer wichtiger Typ‑II‑Zellmarker, was die Verletzung bestätigte. Bei der niedrigsten Dosis war der Schaden jedoch begrenzt und die eigene Reparaturantwort der Lunge blieb aktiv. Dieses Gleichgewicht deutete auf ein Fenster hin, in dem transplantierte Zellen die besten Chancen hätten, sich anzulagern, zu überleben und zur Heilung beizutragen.
Gesunde Surfactant‑Zellen ziehen ein und legen los
Das Team isolierte daraufhin gesunde Typ‑II‑Zellen aus normalen Mäusen und brachte eine Million dieser Zellen zehn Tage nach einer Niedrigdosis‑Bleomycin‑Behandlung direkt in die Atemwege der Sftpc‑defizienten Mäuse ein. Mittels Proteinfärbungen und genetischer Tests zeigten sie, dass Spenderzellen effizient einnisteten, besonders in jüngeren Tieren. Diese transplantierten Zellen produzierten reifes Surfactant‑Protein C—vollständig im Wirt fehlend—was darauf hindeutet, dass sie nicht nur präsent, sondern auch funktionell aktiv waren. Die neuen Zellen blieben mindestens zwei Monate nachweisbar. Wichtig ist, dass Mäuse, die Zelltransplantate erhielten, weniger Lungenschädigung und weniger stark geschädigte Bereiche aufwiesen als Mäuse, die nur Bleomycin bekommen hatten, was darauf hindeutet, dass schon eine teilweise Ersetzung erkrankter Zellen das Fortschreiten der Schädigung abschwächen kann.
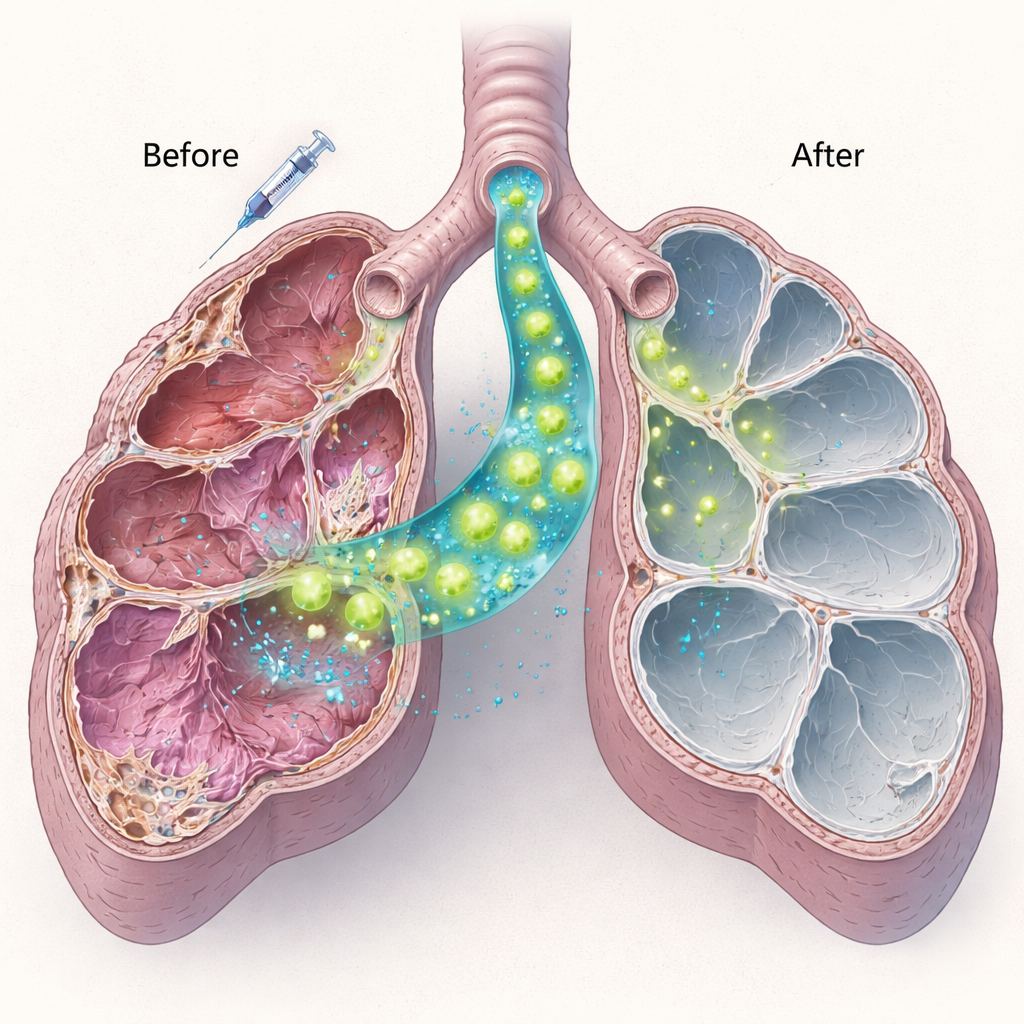
Vom Proof‑of‑Concept zu künftigen Therapien
Für Nichtfachleute lautet die Kernbotschaft: Diese Studie zeigt einen realistischen Weg auf, um Lungen bei bestimmten genetischen Erkrankungen im Kindesalter zu reparieren statt sie zu ersetzen. Indem gezeigt wird, dass eine überschaubare Anzahl gesunder, Surfactant produzierender Zellen in einer chronisch kranken Lunge Fuß fassen, das fehlende Protein herstellen und die Verletzung lindern kann, liefert die Arbeit eine Grundlage für künftige Therapien auf Basis genetisch korrigierter oder aus Stammzellen gewonnener Lungenzellen. Viele Hürden bleiben, etwa sicherere Methoden, menschliche Lungen für eine solche Behandlung vorzubereiten, und die Gewährleistung eines langanhaltenden Nutzens. Dennoch verlagert diese Forschung die Diskussion weg vom reinen Symptommanagement hin zu der Möglichkeit, die eigene maschinerie der Lunge für gesundes Atmen wiederaufzubauen.
Zitation: Predella, C., Lapsley, L., Ni, K. et al. Engraftment of wild-type alveolar type II epithelial cells in surfactant protein C deficient mice. npj Regen Med 11, 11 (2026). https://doi.org/10.1038/s41536-026-00455-0
Schlüsselwörter: interstitielle Lungenerkrankung im Kindesalter, Surfactant‑Protein C, alveoläre Typ‑II‑Zellen, Zelltherapie, Lungenfibrose