Clear Sky Science · de
Die olfaktorische Sinneskarte ist gestört in einem transgenen Mausmodell der Parkinson-Krankheit mit Überexpression des humanen Wildtyp-α‑Synucleins
Warum Geruchsverlust bei Parkinson wichtig ist
Viele Menschen denken bei Parkinson an eine Bewegungsstörung, doch bei den meisten Betroffenen ist das erste, was gestört wird, der Geruchssinn. Dieser Verlust kann Jahrzehnte vor Tremor oder Steifheit auftreten und ist daher ein kraftvolles Frühwarnzeichen. Die hier beschriebene Studie stellt eine grundlegende, aber noch unbeantwortete Frage: Was genau gerät in der Geruchsschaltung des Gehirns aus dem Gleichgewicht, wenn Parkinson-assoziierte Veränderungen beginnen? Indem die Forschenden diese Frage in einem sorgfältig konstruierten Mausmodell untersuchen, zeigen sie, wie ein zentrales Parkinson-Protein die interne „Geruchskarte“ des Gehirns stört und weisen auf eine neue, leicht zugängliche Quelle früher Krankheitsanzeichen hin.
Die Geruchskarte des Gehirns
Unsere Nasen enthalten Millionen spezialisierter Riechzellen, die jeweils auf bestimmte Duftmoleküle reagieren. Diese Zellen senden lange, dünne Fasern in den vorderen Teil des Gehirns, wo sie in winzige Knoten, die Glomeruli, innerhalb der Riechkolben zusammenlaufen. Jeder Duft aktiviert ein spezifisches Muster von Glomeruli und bildet so eine präzise Sinneskarte, die dem Gehirn erlaubt, Kaffee von Zimt oder Rauch von Parfüm zu unterscheiden. Bei gesunden Mäusen projizieren Zellen mit einem bestimmten Geruchsrezeptor (genannt M72) und einem anderen (genannt P2) zuverlässig auf jeweils zwei gut definierte Glomeruli pro Kolben und erzeugen damit eine hoch geordnete und reproduzierbare Karte.
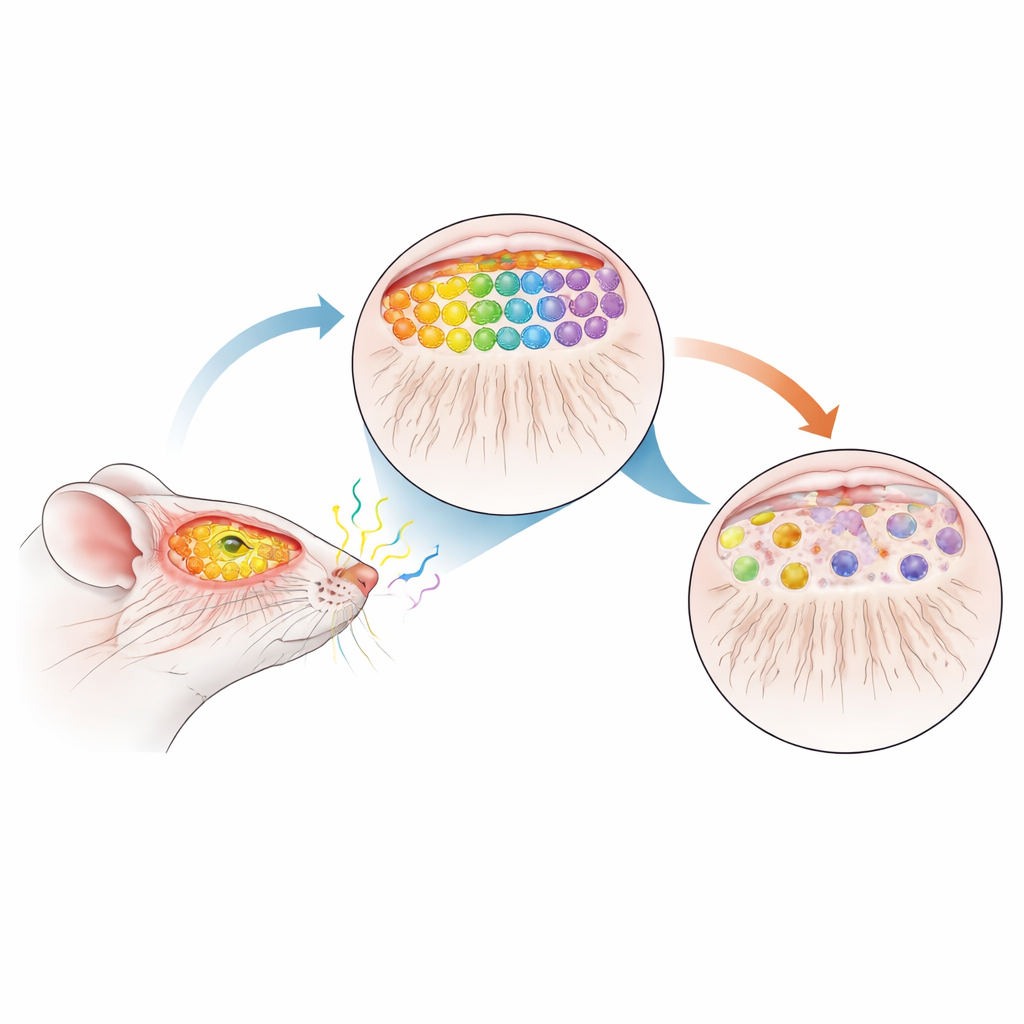
Eine Maus als Stellvertreter für frühes Parkinson
Um zu untersuchen, wie Parkinson diese Karte stören könnte, verwendete das Team Mäuse, die normales humanes α‑Synuclein überproduzieren — dasselbe Protein, das sich im Gehirn von Parkinson-Patienten verklumpt. Diese Tiere kreuzten sie mit M72- und P2-markierten Mäusen, sodass sie ausgewählte Riechzellen und deren Verbindungen visuell verfolgen konnten. Wichtig ist, dass das zusätzliche α‑Synuclein erst nach der Geburt aktiviert wird und mit dem Alter allmählich akkumuliert, womit der langsame, progressive Verlauf der menschlichen Erkrankung nachgeahmt wird. Im Alter von 12 Monaten — ungefähr mittleres Alter für eine Maus und vergleichbar mit einer prodromalen, also vor der Diagnose liegenden Phase beim Menschen — untersuchten die Forschenden die olfaktorischen Systeme der Tiere im Detail.
Wenn die Geruchskarte auseinanderfällt
Durch Anfärben der markierten Neurone und Verfolgen ihrer Bahn fanden die Wissenschaftler eine auffällige Auflösung der Geruchskarte in den α‑Synuclein-überexprimierenden Mäusen. Die Zahl der M72- und P2-Neurone in der Nase sank stark — etwa ein Verlust von drei Vierteln für M72 und nahezu die Hälfte für P2 — während ihre Fasern zum Kolben stark reduziert waren. Anstatt sich ordentlich auf zwei robuste Glomeruli zu konzentrieren, bildeten die verbleibenden Fasern oft mehrere, kleinere Glomeruli unterschiedlicher Größe und Lage. Diese „zusätzlichen“ Knoten erschienen nicht an konsistenten Positionen von Maus zu Maus, was auf einen Verlust der normalen topographischen Genauigkeit hinweist. Ein breit angelegter Marker für Riechzellterminale, VGLUT2, war im Kolben ebenfalls um etwa 44 % reduziert, was darauf hindeutet, dass diese Degeneration weit über die beiden markierten Rezeptortypen hinausreichte.
Verknüpfung zerstörter Schaltkreise mit Geruchsverlust
Die strukturellen Schäden übersetzten sich in messbare Geruchsprobleme. Ältere α‑Synuclein-Mäuse benötigten länger, um versteckte Nahrung zu finden, zeigten eine schlechtere Fähigkeit, einen Geruch von einem anderen zu unterscheiden, und zogen es nicht vor, sich in Bereichen mit ihrem eigenen Geruch aufzuhalten — Verhaltensprüfungen, die zusammen Hyposmie und beeinträchtigte Geruchsdiscrimination offenbaren. Sie benötigten zudem deutlich höhere Duftkonzentrationen, um zu reagieren, was auf eine reduzierte Sensitivität hindeutet. Diese Defizite traten nicht bei jüngeren Mäusen auf, bei denen die markierten Neurone und ihre Karten noch weitgehend normal aussahen, wodurch der zeitliche Verlauf des Funktionsverlusts an den späteren Zusammenbruch der Sinneskarte und nicht an die frühe Entwicklung gebunden wurde. Bemerkenswert ist, dass das problematische Protein zwar im Riechkolben reichlich vorhanden war, jedoch nicht in der sensorischen Schleimhaut der Nase selbst nachgewiesen werden konnte, was auf Veränderungen innerhalb der Kolbenschaltkreise — insbesondere in Mitralzellen, die Geruchsinformationen weiterleiten — als wahrscheinliche Treiber der Kartendysfunktion hindeutet.
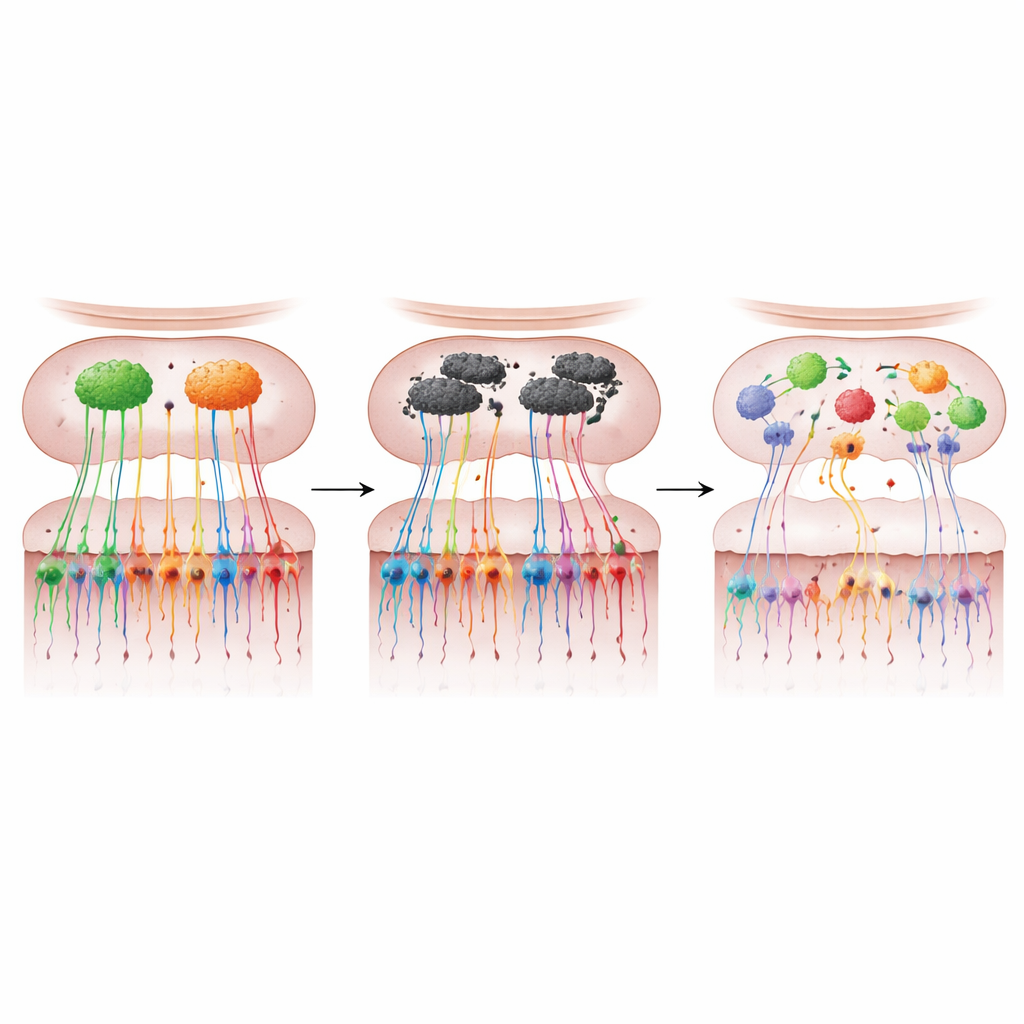
Riechzellen als Fenster zur frühen Erkrankung
In der Summe unterstützt die Arbeit eine klare Botschaft für Nicht-Spezialisten: In diesem Parkinson-ähnlichen Mausmodell führt die Überproduktion von α‑Synuclein im Riechkolben sowohl zu Verlust als auch zu Fehlverdrahtung von Riechneuronen, verzerrt die Geruchskarte des Gehirns und verursacht frühe Geruchsprobleme. Da die sensorischen Zellen der Nase entwicklungsbedingt mit dem Gehirn verwandt sind und gleichzeitig mit minimalinvasiven Abstrichen oder Biopsien entnommen werden können, argumentieren die Autoren, dass ähnliche Veränderungen beim Menschen ein mächtiger früher Biomarker für die Parkinson-Krankheit sein könnten. Das Kartieren der molekularen Fingerabdrücke dieser Zellen könnte ihrer Ansicht nach nicht nur helfen, Personen Jahre vor Auftreten motorischer Symptome als gefährdet zu identifizieren, sondern auch neue Einsichten liefern, wie die Erkrankung beginnt und sich ausbreitet — und wie man sie verlangsamen oder verhindern könnte.
Zitation: Biju, K.C., Hernandez, E.T., Stallings, A.M. et al. Olfactory sensory map is perturbed in a human wild-type α-synuclein overexpressing transgenic mouse model of Parkinson’s disease. npj Parkinsons Dis. 12, 70 (2026). https://doi.org/10.1038/s41531-026-01288-w
Schlüsselwörter: Parkinson-Krankheit, olfaktorische Dysfunktion, alpha-Synuclein, Sinneskarte, Biomarker