Clear Sky Science · de
LRRK2R1627P-Mutation verstärkt umweltbedingte Risikofaktoren, die chronische Entzündung und α-Synuclein-Aggregation im Darm von Ratten auslösen
Warum der Darm bei einer Hirnerkrankung wichtig ist
Morbus Parkinson ist vor allem für Tremor und Bewegungsstörungen bekannt, doch zunehmende Evidenz deutet darauf hin, dass seine Wurzeln weit entfernt vom Gehirn liegen können, tief im Darm. Diese Studie untersucht, wie eine spezifische genetische Veränderung, die mit Parkinson in asiatischen Populationen in Verbindung gebracht wird, zusammen mit Alterung und Toxinexposition allmählich den Darm von Ratten schädigen kann. Indem die Forschenden im Laufe des Lebens der Tiere beobachteten, was im Darm geschieht, verfolgen sie, wie alltägliche Abwehrmechanismen des Immunsystems in eine chronische Entzündung umschlagen können und so ein Umfeld schaffen, in dem krankheitsassoziierte Proteine sich anreichern und letztlich das Gehirn bedrohen könnten.
Ein risikobehaftetes Gen im Verdauungstrakt
Die Wissenschaftler richteten ihr Augenmerk auf eine Variante des Gens LRRK2, das seit langem mit Morbus Parkinson und bestimmten entzündlichen Darmerkrankungen in Verbindung steht. Sie erzeugten Ratten mit der entsprechenden Mutation, genannt LRRK2R1627P, und verglichen diese lebenslang mit normalen Ratten. Obwohl die Menge der LRRK2-mRNA im Darm unverändert blieb, waren das Gesamtniveau des LRRK2-Proteins und einer seiner wichtigen Aktivitätsmarker reduziert, was darauf hindeutet, dass die Mutation die normale Funktion dieses Proteins im Darm schwächt. Diese subtile molekulare Veränderung verursachte keine dramatischen Frühschäden, veränderte jedoch unauffällig die Art und Weise, wie sich Darmzellen erneuern und organisieren, während die Tiere älter wurden.
Altern des Darms unter langsamer, anhaltender Belastung
Im Laufe der Monate entwickelten die mutierten Ratten deutlich gestörte Darmstrukturen. Ihre Dünndärme wurden kürzer, und die feinen fingerartigen Zotten sowie die Krypten, die Nährstoffe aufnehmen, verkleinerten sich. Bestimmte spezialisierte Zellen der Schleimhaut, die schützenden Schleim und antimikrobielle Substanzen produzieren – Becherzellen und Paneth-Zellen – waren reduziert, während Proteine, die Nachbarzellen helfen, dichte, undurchlässige Verbindungen zu bilden, ebenfalls abnahmen. Unter dem Mikroskop wurden diese Verbindungen kürzer oder weiter, was auf eine geschwächte Barriere hindeutet. Wichtig ist, dass die Gesamtarchitektur nicht zusammenbrach; stattdessen zeigte der Darm ein schleichenderes Muster verringerter Erneuerung und Schutzfunktion, das ihn anfälliger für Reizungen und Infektionen machen kann. 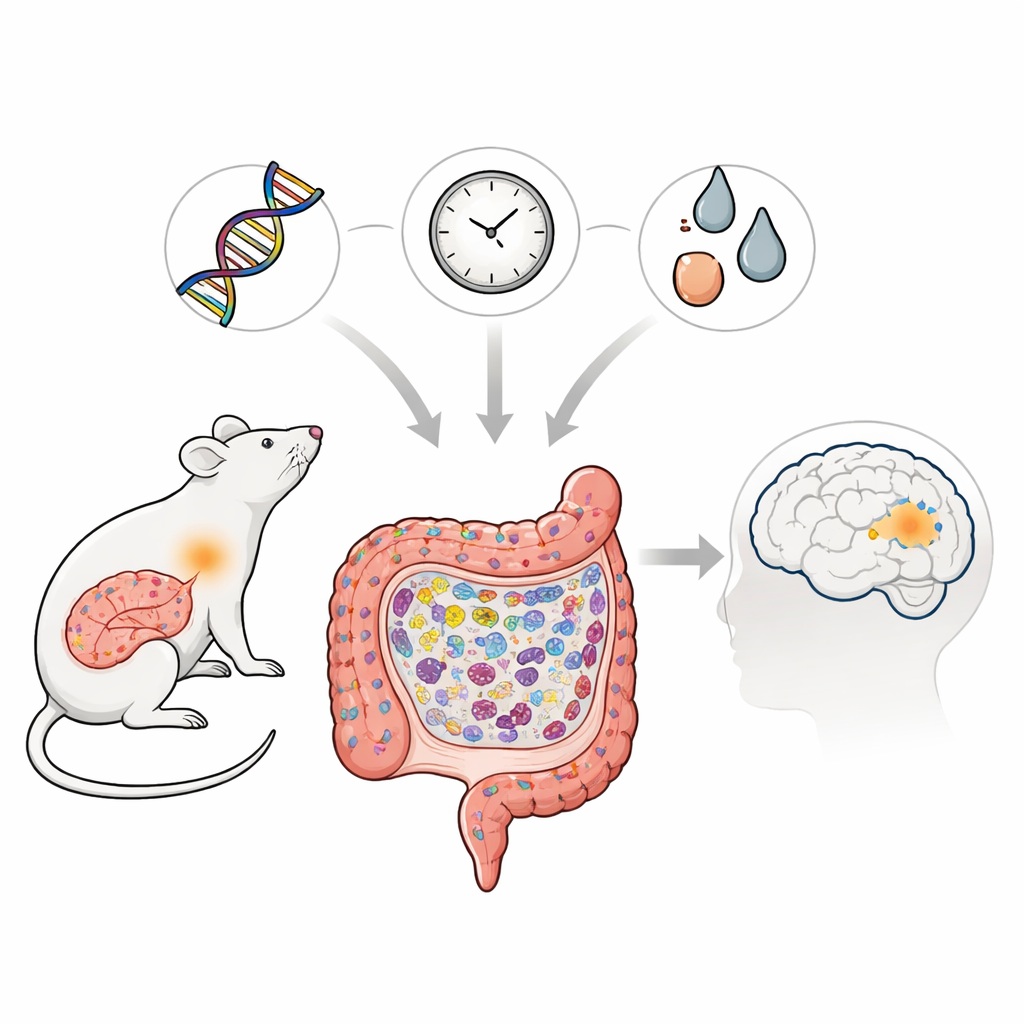
Immunsystem auf Anschlag
Um zu verstehen, warum der Darm aus dem Gleichgewicht geriet, untersuchte das Team Genaktivität und Immunzellen in der Darmwand. Sie fanden, dass Signalwege, die mit dem Sensor TLR4 und seinem Partner NF-κB verbunden sind, bei älteren mutierten Ratten überaktiv waren. Diese Sensoren helfen normalerweise, schädliche Mikroben zu erkennen, trieben hier jedoch die Ansammlung von „zuerst angreifen“-Immunzellen, den M1-Makrophagen, voran. Diese Zellen setzten entzündungsfördernde Moleküle frei und verwandelten den Darm in ein chronisch gereiztes Umfeld. Auffällig war, dass das mit Parkinson assoziierte Protein α-Synuclein in seiner krankheitsassoziierten phosphorylierten Form nicht in Darmneuronen, sondern in diesen aktivierten Makrophagen des Dünndarms zu akkumulieren begann, vor allem in älteren Tieren.
Besonders empfindlich gegenüber Umweltreizen
Die genetische Mutation allein war nicht die ganze Erklärung. Als junge Ratten kurzzeitig bakteriellen Toxinen (LPS) ausgesetzt wurden, die TLR4 stimulieren, entwickelten die Tiere mit der LRRK2-Mutation wesentlich schwerere Darmentzündungen als ihre normalen Gegenstücke. Ihre Darmoberfläche verlor mehr Zellen, Barriereproteine fielen weiter ab und proinflammatorische Makrophagen nahmen stark zu, wobei wiederum anormales α-Synuclein akkumulierte. Dies deutet darauf hin, dass Menschen mit ähnlichen Mutationen besonders empfindlich gegenüber umweltbedingten Störungen des Darms sein könnten, etwa durch bestimmte Infektionen oder Toxine, was ihr Langzeitrisiko verstärken würde.
Das Alarmsignal dämpfen
Da TLR4 im Zentrum dieses Entzündungssturms stand, testete das Team ein Medikament, TAK-242, das spezifisch die TLR4-Signalgebung dämpft. Über mehrere Monate verabreicht an mittelalte Ratten stellte der Inhibitor weitgehend die Länge des Dünndarms, Zotten- und Kryptengröße, schleimproduzierende Zellen und Barriereproteine wieder her. Er reduzierte überaktive Makrophagen, senkte entzündliche Moleküle und verringerte stark die Ansammlung von abnormalem α-Synuclein im Darm. Gleichzeitig normalisierte sich eine gestörte mikrobielle Gemeinschaft: die Diversität stieg, ein Überwuchs von Lactobacillus nahm ab und mehrere nützliche Bakteriengruppen erholten sich, während prognostizierte mikrobiell vermittelte Funktionen sich von krankheitsassoziierten Mustern wegbewegten. 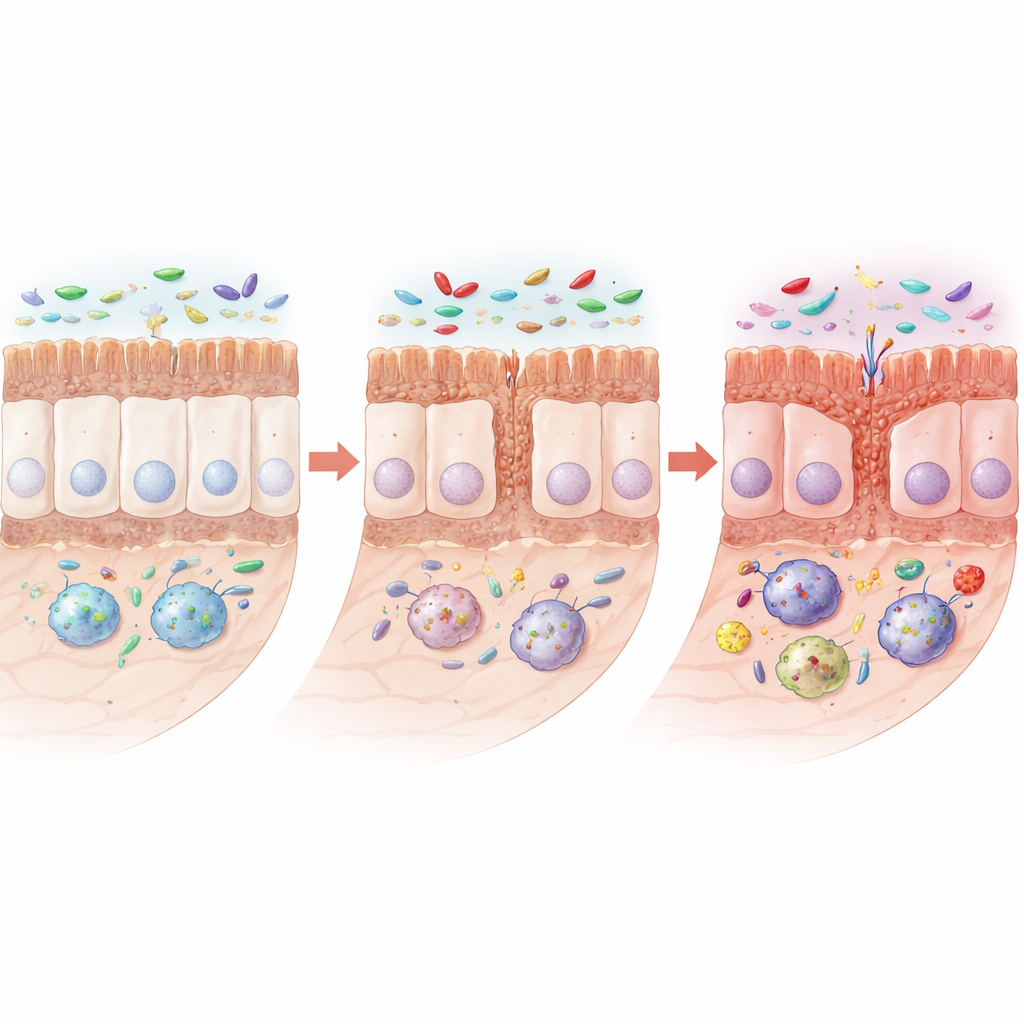
Was das für das Parkinson-Risiko bedeutet
Für Nichtfachleute lautet die Botschaft, dass ein „Parkinson-Gen“ über die Zeit die immunologischen Abwehrmechanismen des Darms unauffällig umgestalten kann, insbesondere in Gegenwart von Alterung und Umweltstress. Bei diesen Ratten führt das zu einer chronischen, niedriggradigen Entzündung, die die Darmbarriere schwächt, die ansässigen Mikroben stört und Parkinson-assoziiertes Protein in Immunzellen anreichern lässt – noch kein ausgewachsenes Parkinson, aber ein biologisches Umfeld, das spätere Hirnerkrankungen begünstigen könnte. Indem die Studie zeigt, dass die Blockade eines einzigen immunologischen Darmwegs viele dieser Veränderungen rückgängig machen kann, hebt sie den Darm als praktisch zugängliches frühes Ziel hervor: den Darm zu schützen und Entzündungen im Darm zu zähmen könnte helfen, Parkinson bei genetisch gefährdeten Menschen zu verzögern oder zu verhindern.
Zitation: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
Schlüsselwörter: Morbus Parkinson, Darmentzündung, LRRK2-Mutation, Mikrobiom, angeborene Immunabwehr