Clear Sky Science · de
Systematische Bewertung von Regulatoren der Mitochondrienmorphologie zur Verbesserung neuronaler α-Synucleinopathie
Warum winzige Kraftwerke bei Hirnerkrankungen wichtig sind
Mitochondrien, die „Kraftwerke“ der Zelle, sind entscheidend dafür, dass Nervenzellen überleben und ihre Verbindungen funktionsfähig bleiben. Bei Erkrankungen des Gehirns wie dem Morbus Parkinson erscheinen diese kleinen Strukturen häufig geschädigt oder fragmentiert, doch es war schwierig zu unterscheiden, welche Veränderungen schädlich sind und welche Schalter man sicher umlegen kann, um sie zu schützen. Diese Studie testet systematisch zentrale „Formregulatoren“ der Mitochondrien in einem Labor-Modell für Parkinson‑ähnliche Proteinansammlungen und verwendet ein Werkzeug der künstlichen Intelligenz, um Mitochondrienformen in verschiedenen Bereichen von Neuronen zu messen. Die Arbeit weist auf einen bestimmten Regulator, genannt Fis1, als vielversprechendes Ziel hin, um Mitochondrien — und Synapsen — gesund zu halten, ohne neue Nebenwirkungen zu verursachen.
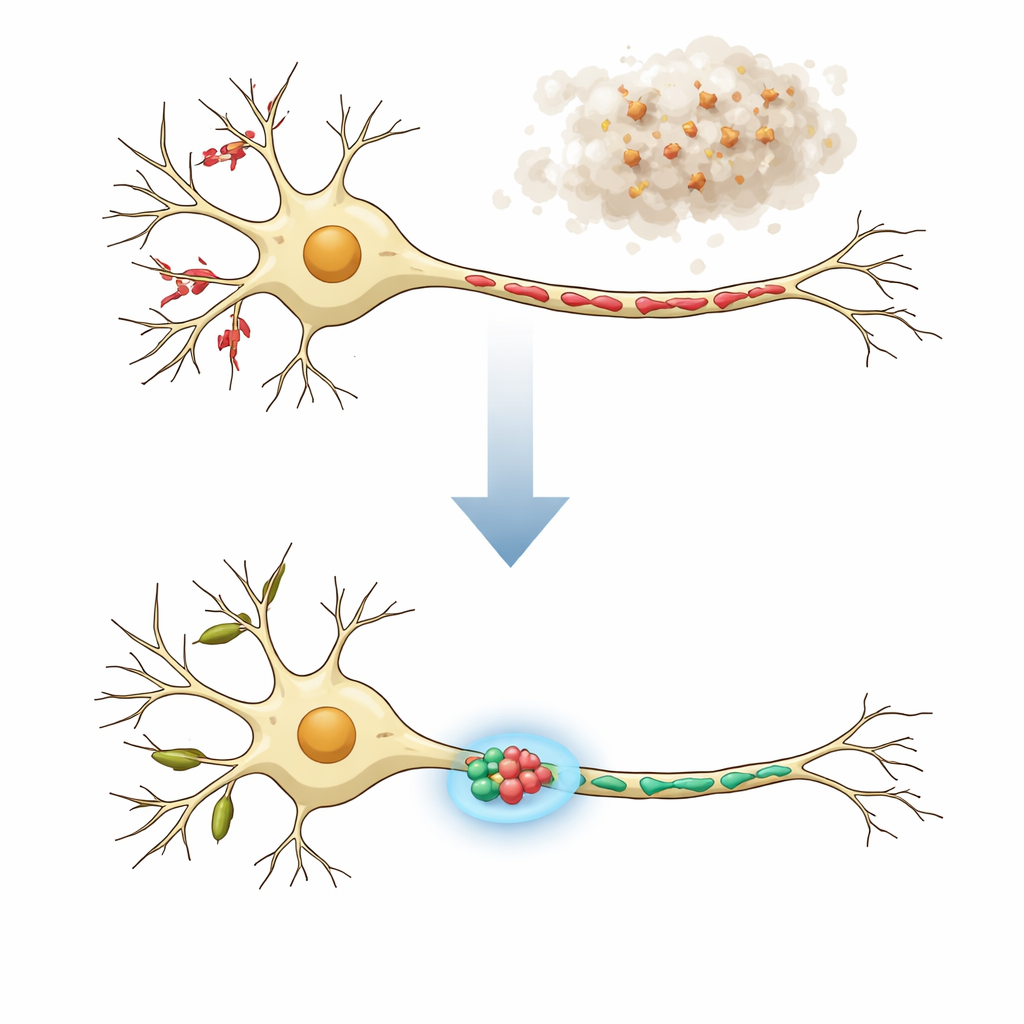
Die zwei Nachbarschaften einer Nervenzelle
Neuronen sind nicht einheitlich: Ihre baumartigen Verästelungen (Dendriten) und langen Kabel (Axone) haben unterschiedliche Aufgaben und beherbergen Mitochondrien sehr unterschiedlicher Form. In gesunden Nervenzellen finden sich in Dendriten tendenziell lange, schlauchförmige Mitochondrien, die die lokale Proteinproduktion und flexible Kommunikation an Empfangsstellen, den dendritischen Dornfortsätzen, unterstützen. Axone, die Signale senden, tragen dagegen viele kurze Mitochondrien, die Energie liefern und helfen, Calciumspiegel an präsynaptischen Endungen zu regulieren. Bei neurodegenerativen Erkrankungen können sowohl Funktion als auch Struktur dieser Mitochondrien gestört sein und sich als Fragmente, geschwollene Formen oder perlenartige Ketten zeigen. Die Autoren folgerten, dass wirklich wirksame Behandlungen die Mitochondrien sowohl in Dendriten als auch in Axonen in ihre normalen, kompartment-spezifischen Formen zurückführen müssen.
Aufbau eines Parkinson‑ähnlichen Stresstests
Um ein zentrales Merkmal der Parkinson‑Krankheit und verwandter Erkrankungen nachzuahmen, setzten die Forschenden kultivierte kortikale Mausneuronen vorgeformten Fibrillen von Alpha‑Synuclein aus, einem Protein, das sich zu schädlichen Aggregaten verklumpen kann. Innerhalb weniger Tage führten diese Fibrillen zur Ablagerung abnormer Alpha‑Synuclein‑Klümpchen in den Zellen und zu ausgeprägter mitochondrieller Fragmentierung sowohl in Dendriten als auch in Axonen. Mithilfe von MitoVis, einem Deep‑Learning‑Bildanalysesystem, konnte das Team automatisch Dendriten von Axonen in Mikroskopaufnahmen trennen und Länge, Fläche und Form von hunderten Mitochondrien pro Bild etwa zehnmal schneller messen als durch manuelles Nachzeichnen. Dieser Hochdurchsatzansatz bestätigte, dass der krankheitsähnliche Zustand Mitochondrien verkürzte und runder machte, was mit Befunden aus Tiermodellen und Patientengewebe übereinstimmt.
Prüfung der Formschalter der Mitochondrien
Die Gruppe untersuchte dann, ob das Beeinflussen spezifischer Fusions‑ und Spaltungsproteine diesen Schaden verhindern könnte. Eine Erhöhung zweier Fusionsproteine (Mfn1 und Mfn2) oder die Herunterregulierung eines Spaltungsproteins (Mff) schützte dendritische Mitochondrien vor der durch Alpha‑Synuclein ausgelösten Verkürzung und bewahrte zudem dendritische Dornfortsätze vor dem Verlust. Allerdings führten dieselben Manipulationen dazu, dass axonale Mitochondrien übermäßig lang wurden — ein Zustand, der in früheren Arbeiten mit Problemen bei der Signalabgabe und der Axonverzweigung in Verbindung gebracht wurde. Im Gegensatz dazu stellte die Reduktion eines anderen Spaltungsproteins, Fis1, die mitochondriale Länge sowohl in Dendriten als auch in Axonen nahezu normal wieder her, ohne Überlängerung zu erzeugen. Wichtig ist, dass in diesem Versuchsaufbau die Verringerung von Fis1 die Neuronen nicht abtötete und, ähnlich wie die anderen Interventionen, die Dichte dendritischer Dornfortsätze bewahrte, die unter Alpha‑Synuclein‑Stress sonst schrumpfen würden.
Calcium im Gleichgewicht halten
Da Mitochondrien in Axonen beim Ausgleich von Calcium während elektrischer Aktivität helfen, prüften die Forschenden, ob eine Formveränderung dieses empfindliche Gleichgewicht beeinflusst. Sie nutzten einen fluoreszenten Calciumsensor, der zu Mitochondrien in präsynaptischen Boutons zielgerichtet war, und stimulierten Axone mit kurzen Aktionspotential‑Bursts. Im Alpha‑Synuclein‑Zustand zeigte das Calcium‑Handling in leicht verkürzten axonalen Mitochondrien ein ähnliches Muster wie normal. Wurden axonale Mitochondrien jedoch durch Überexpression von Mfn1 oder durch Mff‑Herunterregulierung übermäßig lang, nahmen sie nach der Stimulation mehr Calcium auf als üblich. Diese verstärkte Aufnahme könnte die präsynaptische Funktion stören. Im Gegensatz dazu bewahrte die Fis1‑Herunterregulierung, die die mitochondriale Länge normalisierte, ohne zu überziehen, mitochondriale Calciumantworten, die eng an gesunde Kontrollen anschlossen — ein Hinweis auf weniger versteckte Abwägungen.
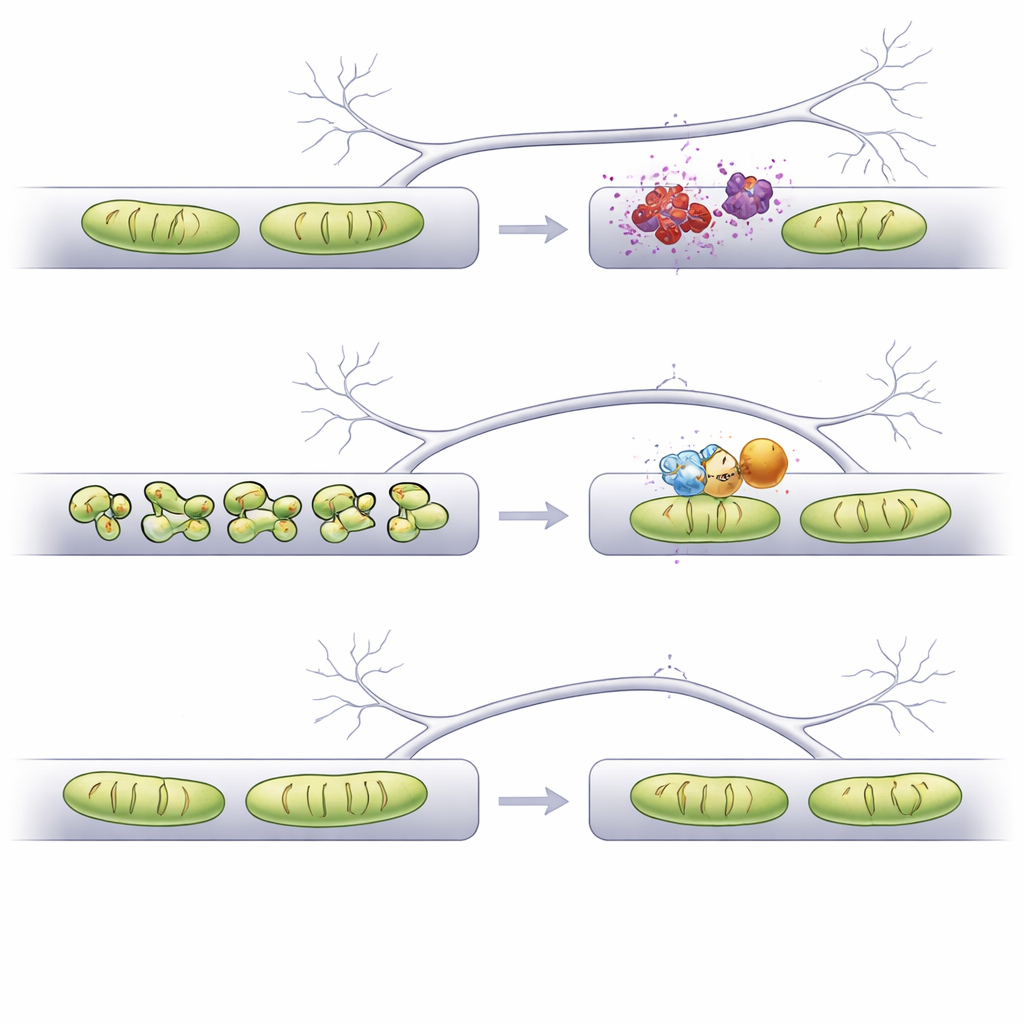
Was das für künftige Therapien bedeuten könnte
Insgesamt zeigt die Studie, dass es nicht ausreicht, Mitochondrien einfach länger zu machen — entscheidend ist, ihre Form in der richtigen Größe im richtigen Kompartment wiederherzustellen. Mithilfe eines KI‑gestützten Bildgebungs‑Workflows identifizieren die Autoren Fis1 als ein besonders attraktives Ziel: Dessen Herunterregulierung stabilisiert die Mitochondrien strukturell in Dendriten und Axonen, verhindert den Verlust dendritischer Dornfortsätze und vermeidet abnormales Calcium‑Handling in präsynaptischen Endungen. Diese Ergebnisse stützen die Idee, dass eine sorgfältige Feinabstimmung der Mitochondrienform, möglicherweise mit Medikamenten oder Antisense‑Molekülen, die auf Fis1 abzielen, dazu beitragen könnte, empfindliche Synapsen bei Parkinson‑verwandter Alpha‑Synucleinopathie und möglicherweise anderen Hirnerkrankungen zu schützen, bei denen Mitochondrien aus dem Gleichgewicht geraten.
Zitation: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
Schlüsselwörter: Morbus Parkinson, Mitochondrien, Alpha-Synuclein, synaptische Dysfunktion, Neurodegeneration