Clear Sky Science · de
Klinischer Nutzen evozierter Potentiale zur Programmierung subthalamischer Tiefer Hirnstimulation bei Parkinson-Krankheit
Warum diese Geschichte vom Hirnschrittmacher wichtig ist
Bei vielen Menschen mit Parkinson-Krankheit versagen Medikamente mit der Zeit in ihrer konsistenten Wirkung. Sie können zwischen Steifheit und unkontrollierten Bewegungen schwanken, und die Feinabstimmung der Behandlung wird zu einem frustrierenden Kreislauf aus Klinikbesuchen. Dieser Übersichtsartikel untersucht, wie Ärztinnen und Ärzte die elektrischen Echos des Gehirns — sogenannte evokierte Potentiale — nutzen können, um die tiefe Hirnstimulation (THS) schneller und objektiver zu programmieren. Im Kern geht es um die Frage, ob sich THS von sorgfältigem Rätselraten zu einem datenbasierten, personalisierten Hirnschrittmacher machen lässt.
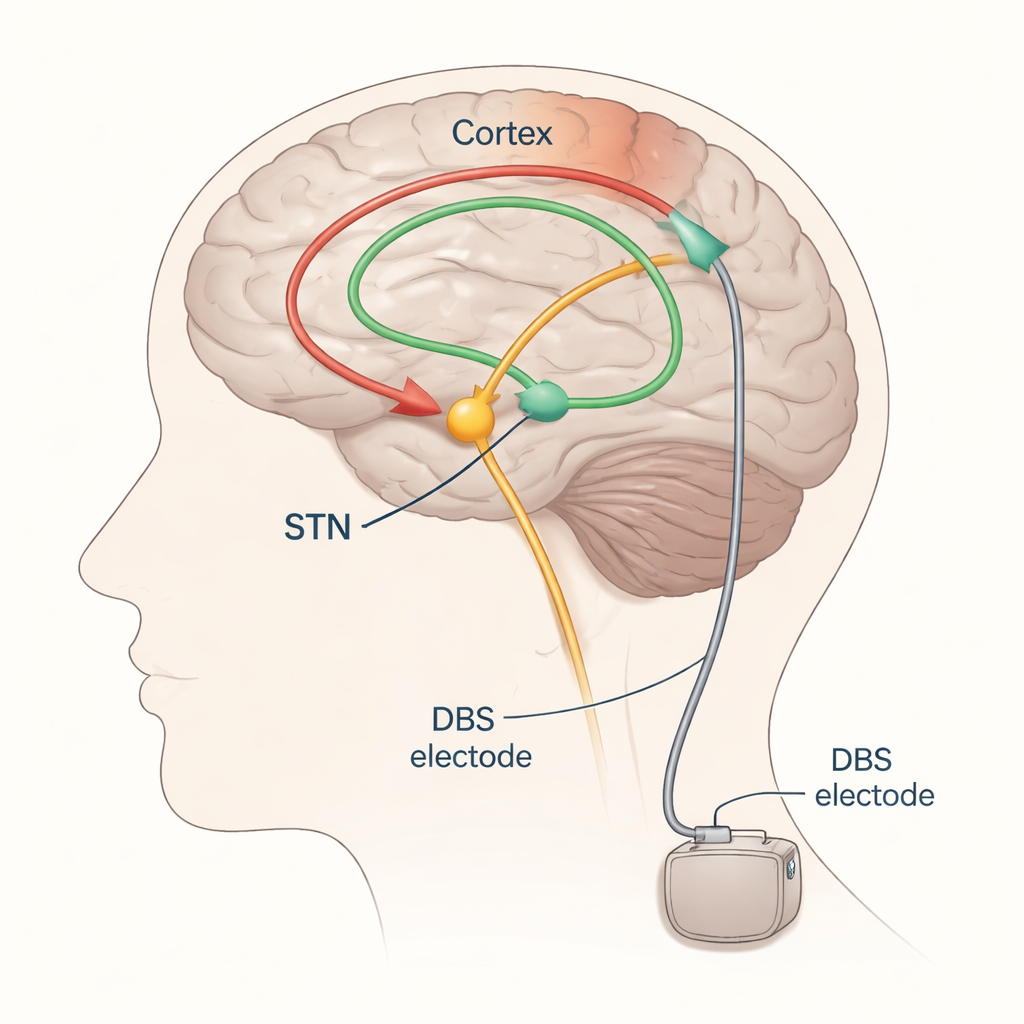
Vom Ausprobieren zum gezielten Abstimmen
Bei Parkinson zielt die THS meist auf eine kleine, tief im Gehirn gelegene Struktur, den subthalamischen Kern (STN). Dort werden Elektroden implantiert und mit einem Impulsgeber unter der Haut in der Brust verbunden. Richtig eingestellt kann STN-THS Zittern, Verlangsamung und Steifheit lindern; breitet sich das elektrische Feld jedoch zu weit aus, kann es versehentlich benachbarte Bahnen reizen, die Muskeln oder Empfindungen steuern, was zu Nebenwirkungen wie Muskelzucken oder Kribbeln führt. Heute passen Neurologinnen und Neurologen die THS meist an, indem sie Einstellungen schrittweise verändern und Bewegungen sowie Nebenwirkungen beobachten — ein zeitaufwändiges Vorgehen, das davon abhängt, wie sich die Patientin oder der Patient an diesem Tag fühlt, und oft mehrere Nachsorgetermine erfordert.
Den elektrischen Echos des Gehirns lauschen
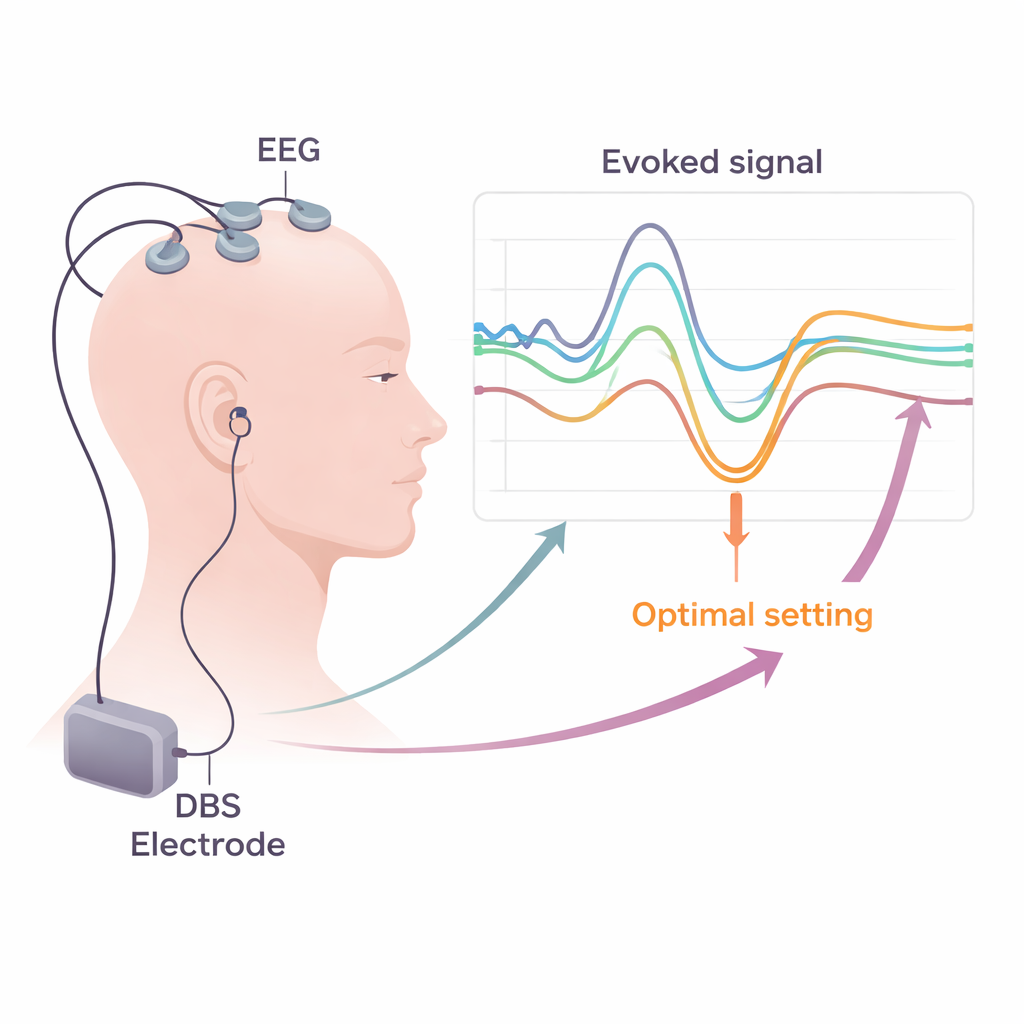
Die Autoren konzentrieren sich auf evokierte Potentiale — winzige, zeitlich gebundene elektrische Antworten im Gehirn oder in Muskeln nach einem Reiz — als mögliche Wegweiser für gute und schlechte THS-Einstellungen. Wenn der STN stimuliert wird, laufen Aktivitätswellen entlang von Nervenbahnen, die mit EEG auf der Kopfhaut, mit EMG in der Muskelaktivität oder gelegentlich mit Elektrodenstreifen direkt auf der Hirnoberfläche messbar sind. Durch wiederholte Niedrigfrequenzstimulation und Mittelung der Antworten können Forscher zuverlässig charakteristische Wellen erkennen, die in unterschiedlichen Verzögerungen (Millisekunden) nach jedem Impuls auftreten. Frühe Wellen, die innerhalb von etwa zwei Tausendstelsekunden eintreffen, spiegeln vornehmlich die Aktivierung schneller motorischer Bahnen wider, die in der Nähe der Elektrode verlaufen. Etwas spätere Wellen, bei etwa drei Millisekunden (häufig als „P3“-Komponente bezeichnet), werden als Ausdruck einer direkten Verbindung zwischen dem frontalen Kortex und dem STN gedeutet, bekannt als der hyperdirekte Weg. Noch spätere Wellen durchlaufen vermutlich längere, verschlungene Schaltkreise, die Thalamus und andere tiefe Kerne einschließen.
Die richtige Stelle finden und Probleme vermeiden
In vielen Studien zeichnet sich ein konsistentes Bild ab: Kontakte an der DBS-Elektrode, die eine starke, kurzlatente P3 erzeugen, liegen tendenziell im hilfreichsten Bereich des STN und sind mit besseren Verbesserungen der Parkinson-Motorik und einem größeren „therapeutischen Fenster“ vor dem Auftreten von Nebenwirkungen verbunden. Im Gegensatz dazu signalisieren sehr frühe Wellen, die motorischen Bahnen zuzuordnen sind, und bestimmte Antworten bei etwa 8–10 Millisekunden oft, dass die Stimulation in benachbarte Strukturen ausläuft, wodurch das Risiko für Muskelkontraktionen oder andere unerwünschte Effekte steigt. Getrennte Messungen motorischer evozierter Potentiale (EMG-Antworten in Gesichts- und Extremitätenmuskulatur) und somatosensorischer evozierter Potentiale (EEG-Muster im Zusammenhang mit Berührungsbahnen) können subtile Aktivierung des inneren Kapselsystems oder des medialen Lemniskus offenbaren — Faserbündel, die motorische Befehle und sensorische Informationen übertragen. Solche Veränderungen frühzeitig zu erkennen ermöglicht es Klinikern, den Strom von riskanten Bereichen wegzulenken, indem sie andere Kontakte wählen oder Impulsform und Polarität anpassen.
Die Labortechniken klinikfähig machen
Um diese Erkenntnisse in die Routineversorgung zu überführen, sind praktikable Lösungen nötig. Der Review erklärt, wie Standard-EEG- und EMG-Systeme in Krankenhäusern bereits die meisten benötigten Signale aufzeichnen können, sofern sie hohe Abtastraten verwenden und sorgfältige Methoden zur Entfernung elektrischer „Störsignale“ der DBS-Impulse einsetzen. Die Autoren erörtern Strategien zur Artefaktreduktion, wie geschicktes Re-Referencing, Templatesubtraktion und fortgeschrittene Computeralgorithmen, die echte Gehirnaktivität von Störresten der Stimulation trennen. Sie vertreten die Auffassung, dass kurze, strukturierte Testsequenzen — kombiniert aus kurzen Perioden niedriger Frequenz-DBS, Kopfhautaufzeichnungen und Muskelüberwachung in Ruhe und bei leichter Kontraktion — in die übliche programmierende Woche nach der Operation integriert werden könnten. Evokierte-Potential-Karten für jeden Kontakt könnten dann mit Bildgebung und anderen Biomarkern kombiniert werden, um langfristig zu steuern, welche Kontakte und Einstellungen verwendet werden.
Was das für Menschen mit Parkinson bedeutet
Der Artikel schließt, dass evokierte Potentiale vielversprechende Kandidaten sind, um die THS-Programmierung präziser, effizienter und vorhersehbarer zu machen. Insbesondere scheint die kurzlatente P3-Welle ein starker Marker dafür zu sein, dass die Stimulation den richtigen Schaltkreis trifft, um die motorischen Symptome von Parkinson zu lindern, während motorische und sensorische evozierte Antworten warnen können, wenn Strom in Bahnen ausläuft, die Nebenwirkungen verursachen. Auch wenn weitere Arbeiten nötig sind, um die Techniken zu standardisieren und Vorteile in der alltäglichen Praxis zu belegen, zielt dieser Ansatz auf eine Zukunft, in der Ärztinnen und Ärzte beim Programmieren „dem Gehirn zuhören“, schnell die individuelle optimale Stelle finden und die Belastung durch Ausprobieren für Menschen mit Parkinson-Krankheit verringern.
Zitation: Hale, B., Latorre, A., Rocchi, L. et al. Clinical utility of evoked potentials for programming subthalamic deep brain stimulation in Parkinsons disease. npj Parkinsons Dis. 12, 54 (2026). https://doi.org/10.1038/s41531-026-01274-2
Schlüsselwörter: Parkinson-Krankheit, tiefe Hirnstimulation, evokierte Potentiale, Gehirnkartierung, Neurophysiologie