Clear Sky Science · de
Entschlüsselung der Auswirkungen visueller Zustände auf Feedback-Signale der adaptiven Tiefenhirnstimulation bei Bewegungsstörungen
Warum es für Hirnimplantate wichtig ist, die Augen zu schließen
Für Menschen mit Parkinson-Krankheit oder Dystonie kann die Tiefenhirnstimulation (THS) wie ein Schrittmacher für fehlgesteuerte Hirnnetzwerke wirken. Neuere „adaptive“ THS-Systeme versprechen, die Stimulation in Echtzeit automatisch anzupassen, indem sie auf Gehirnsignale hören. Diese Studie zeigt, dass etwas so Einfaches und Alltägliches wie das Schließen der Augen diese Signale stark verändern kann – das heißt, künftige Hirnimplantate müssen zunächst den Zustand der Person erkennen, bevor sie entscheiden, wie sie stimulieren.
Lernende und adaptive Hirnschrittmacher
Die herkömmliche THS liefert rund um die Uhr konstante elektrische Impulse in tiefe Hirnregionen. Das kann Symptome wie Zittern und Steifheit lindern, aber auch Batterie verschwenden und gelegentlich Nebenwirkungen verursachen, weil die Stimulation nicht auf wechselnde Patientenbefindlichkeiten reagiert. Adaptive THS will das korrigieren, indem die Stromstärke anhand von „lokalen Feldpotenzialen“ (LFPs) hoch- oder heruntergeregelt wird – winzige rhythmische Spannungen, die an denselben Elektroden gemessen werden, die auch therapieren. Diese Rhythmen sind in Strukturen wie dem subthalamischen Nukleus (STN) und dem Globus pallidus internus (GPi) am stärksten, wichtige Knoten im Bewegungsnetzwerk. 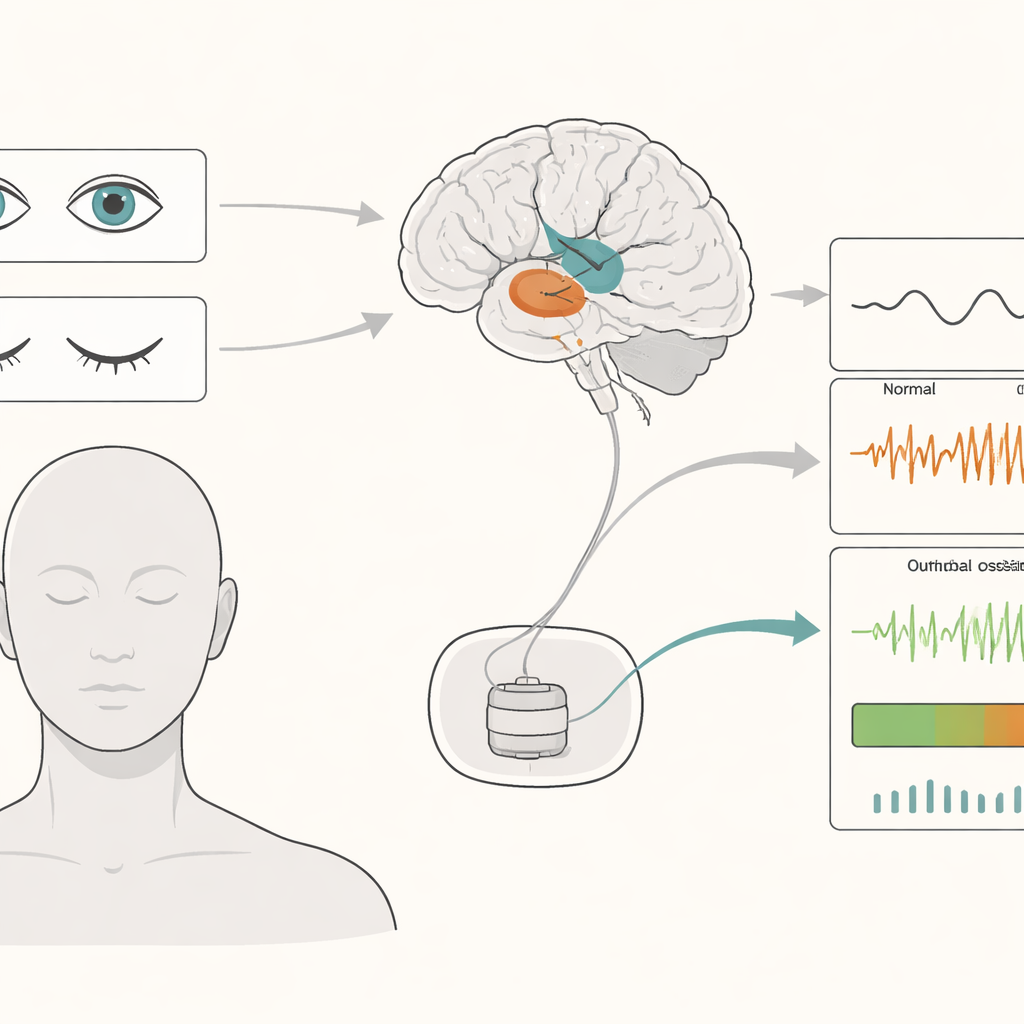
Wenn das Sehen ruht, verschieben sich tiefe Hirnrhythmen
Die Forschenden begleiteten 36 Patientinnen und Patienten – 18 mit Parkinson-Krankheit und 18 mit Dystonie – in den Tagen nach der THS-Operation. Sie zeichneten Gehirnaktivität von STN- oder GPi-Elektroden sowie vom Kopfhaut-EEG auf, während die Patienten mit offenen Augen, geschlossenen Augen oder im Schlaf ruhten. Das Schließen der Augen verstärkte konsistent langsame Rhythmen im tiefen Gehirn, besonders im Theta- und Alpha-Bereich – genau jene Signale, die viele adaptive THS-Systeme beobachten. Diese Verstärkung war im STN am ausgeprägtesten, das eng mit der äußeren „denkenden“ Hirnrinde verbunden ist, und im GPi weniger stark. Schlaf zeigte wiederum ein anderes Muster, mit besonders kräftigen sehr langsamen Wellen.
Unterschiedliche Erkrankungen, unterschiedliche Signal-Fingerabdrücke
Parkinson und Dystonie haben bereits unterschiedliche rhythmische „Fingerabdrücke“, und die Studie fand, dass das Schließen der Augen diese Fingerabdrücke auf leicht unterschiedliche Weise veränderte. In beiden Erkrankungen fielen die Leistung im Niederfrequenzbereich und im Alpha-Band, wenn die Patienten die Augen wieder öffneten. Bei Parkinson trat jedoch zusätzlich ein Abfall der Theta-Leistung auf, der bei Dystonie nicht sichtbar war. In der Folge behielten Menschen mit Dystonie nach Augenöffnung mehr Theta-Aktivität als solche mit Parkinson. Das macht deutlich, dass dasselbe tiefe Hirnsignal sowohl Krankheit als auch ganz normale Wachheits- oder Aufmerksamkeitsänderungen widerspiegeln kann, weshalb es riskant ist, einen einzelnen Rhythmus als einfachen Ein-/Ausschalter für Symptome zu behandeln.
Hirnnetzwerke kommunizieren stärker bei geschlossenen Augen
Über die Stärke der Rhythmen hinaus untersuchte das Team auch, wie synchron tiefere Strukturen und die Kortizes miteinander schwingen. Mit einer Methode, die echte Kommunikation statt bloßer gemeinsamer Rauschanteile hervorhebt, fanden sie, dass das Schließen der Augen die koordinierte Niederfrequenz- und Alpha-Aktivität zwischen STN und zentralen Kopfregionen über dem sensomotorischen Kortex erhöhte. Auch der GPi zeigte bei geschlossenen Augen stärkere Alpha-Kopplung zum Kortex, wenn auch moderater und ohne klare regionale Unterschiede. Diese Befunde deuten darauf hin, dass Ruhen mit geschlossenen Augen nicht nur die lokale Aktivität verändert, sondern die breiteren Kommunikationsmuster des Bewegungsnetzwerks.
Maschinen beibringen, innere Zustände zu erkennen
Da künftige Implantate wahrscheinlich Algorithmen einsetzen werden, um Gehirnsignale zu lesen, prüften die Forschenden, ob einfache maschinelle Lernmodelle allein anhand dieser Rhythmen zwischen offenen und geschlossenen Augen unterscheiden können. Indem sie mehrere Frequenzbänder in Klassifikatoren einspeisten, konnten sie den Augenstatus mit etwa 88 Prozent Genauigkeit anhand von STN-Signalen und 77 Prozent anhand von GPi-Signalen erkennen, sowohl bei Parkinson als auch bei Dystonie. Nichtlineare Modelle, die komplexere Muster erfassen können, schnitten noch besser ab, und die beste Dekodierung gelang aus sensomotorischen Regionen, die am direktesten mit Bewegung verknüpft sind. 
Auf dem Weg zu intelligenterer, kontextbewusster Hirnstimulation
Einfach gesagt zeigt die Studie, dass gewöhnliche, gesunde Veränderungen in Wachheit oder visueller Engagements eines Menschen die Hirnwellen, auf die adaptive THS-Systeme angewiesen sind, stark verändern können. Reagiert ein Implantat einfach jedes Mal, wenn ein Rhythmus einen festen Schwellenwert überschreitet, kann es normale Zustandswechsel fälschlich als Krankheitsschübe deuten und über- oder unterstimulieren. Die Autorinnen und Autoren plädieren dafür, dass die nächste THS-Generation zunächst den Kontext der Person – etwa offene vs. geschlossene Augen, Schlaf vs. Wachsein – erkennt und dann Krankheitssignale abhängig von diesem Zustand unterschiedlich interpretiert. Solche „zustandsbewussten“ Hirnschrittmacher könnten präziser helfen, unnötige Stimulation vermeiden und Menschen mit Bewegungsstörungen im Alltag besser unterstützen.
Zitation: Zhu, GY., Merk, T., Butenko, K. et al. Decoding the impact of visual states on adaptive deep brain stimulation feedback signals in movement disorders. npj Parkinsons Dis. 12, 61 (2026). https://doi.org/10.1038/s41531-026-01273-3
Schlüsselwörter: adaptive Tiefenhirnstimulation, Parkinson-Krankheit, Dystonie, Hirnoszillationen, Gehirn–Computer-Schnittstellen