Clear Sky Science · de
Hemmung der de-novo-Ceramid-Synthese mildert alpha-Synuclein-Pathologie in einem Parkinson-Mausmodell
Warum Fette im Gehirn für Parkinson wichtig sind
Morbus Parkinson ist vor allem für zitternde Hände und verlangsamte Bewegungen bekannt, doch tief im Gehirn spielt sich ein stilleres Drama ab. Nervenzellen, die die Bewegung steuern, sterben allmählich, während ein Protein namens Alpha‑Synuclein sich zu klebrigen Aggregate verklumpt. Diese Studie zeigt, dass eine bestimmte Fettfamilie, die Ceramide, diesen Schaden vorantreibt — und dass das Blockieren ihrer Produktion Gehirnzellen bei Mäusen und in menschlichen Zellmodellen schützen kann. Die Arbeit weist auf einen unerwarteten, medikamentös angreifbaren Weg hin, der eines Tages Parkinson nicht nur symptomatisch lindern, sondern verlangsamen oder verhindern könnte.
Hinweise aus postmortem Gehirnen
Um zu klären, ob Ceramide an Parkinson und verwandten Erkrankungen beteiligt sind, untersuchten die Forschenden zunächst postmortem Gehirngewebe von Menschen mit Lewy-Körper-Demenz, einer Störung, die dieselben toxischen Proteinaggregate wie Parkinson aufweist. Mit empfindlichen chemischen Messungen stellten sie fest, dass viele Ceramidtypen in der Mittelhirnregion deutlich erhöht waren im Vergleich zu gesunden Gehirnen, besonders solche mit langen Fettsäuren. Anschließend analysierten sie große genetische Datensätze aus menschlichen Gehirnzellen neu und entdeckten, dass die Gene, die Ceramide aufbauen und verarbeiten, in dopaminproduzierenden Neuronen von Parkinson-Patienten stärker aktiv waren — ebenso in bestimmten Stützzellen wie Astrozyten und Oligodendrozyten. Zusammengenommen deuten diese Befunde darauf hin, dass das Ceramid-Gleichgewicht in mehreren Zelltypen des erkrankten Gehirns gestört ist.
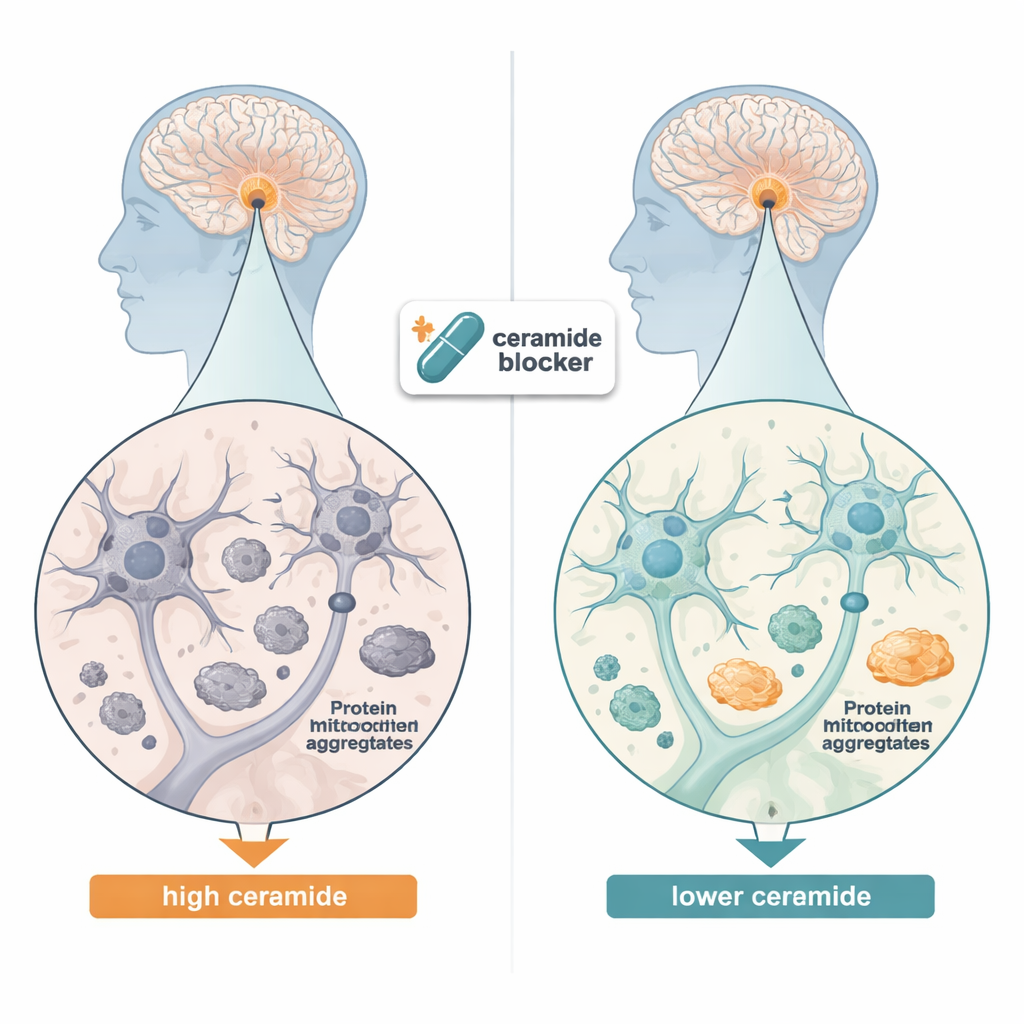
Aufräumen von Protein-Aggregaten in Zellen
Als Nächstes fragten die Forschenden, ob das Senken des Ceramidspiegels die Proteinansammlungen in nervenähnlichen Zellen im Labor reduzieren könnte. Sie verwendeten humane Neuroblastomzellen, die so verändert waren, dass sie eine mutante Form von Alpha‑Synuclein überproduzieren, die leicht verklumpt. Wenn sie den ersten Schritt der Ceramidproduktion ausschalteten — entweder durch Stilllegen des Gens für ein Schlüsselenzym oder durch Zugabe des Wirkstoffs Myriocin — sank die Menge unlöslicher Alpha‑Synuclein-Aggregate deutlich. Gleichzeitig stiegen Marker der Mitophagie, des zellspezifischen Systems zum Erkennen und Recycling beschädigter Mitochondrien, und die Maschinerie, die unerwünschte Proteine für den Abbau markiert, wurde aktiver. Diese Veränderungen legen nahe, dass überschüssige Ceramide normalerweise die zellulären Aufräumtruppen blockieren und dass das Entfernen dieser Lipidlast der Zelle ermöglicht, fehlerhafte Mitochondrien und Proteinaggregate effizienter zu beseitigen.
Schutz der Gehirnfunktion bei Mäusen
Die entscheidende Prüfung war, ob diese Strategie im lebenden Gehirn hilft. Die Forschenden behandelten ein etabliertes Mausmodell, das mutantes humanes Alpha‑Synuclein überproduziert und allmählich Bewegungsstörungen und Gedächtnisprobleme entwickelt. Ab dem mittleren Lebensalter erhielten einige Mäuse mehrere Monate lang Myriocin-Injektionen, andere erhielten ein unschädliches Vehikel. Myriocin senkte deutlich die Ceramidspiegel im Blut und im Mittelhirn der Tiere. Verhaltensprüfungen zeigten, dass behandelte Mäuse weiter liefen und in einem einfachen Labyrinth, das vom räumlichen Arbeitsgedächtnis abhängt, besser abschnitten. Gehirnschnitte dieser Tiere zeigten, dass in Schlüsselregionen mehr dopaminproduzierende Neurone überlebten und dass die Menge an phosphoryliertem, aggregationsanfälligem Alpha‑Synuclein reduziert war. Groß angelegte Genexpressionsanalysen des Mittelhirns zeigten außerdem, dass Myriocin entzündliche Signalwege drosselte und Gene wiederherstellte, die mit synaptischer Kommunikation und gesunder Mitochondrienpflege verbunden sind.
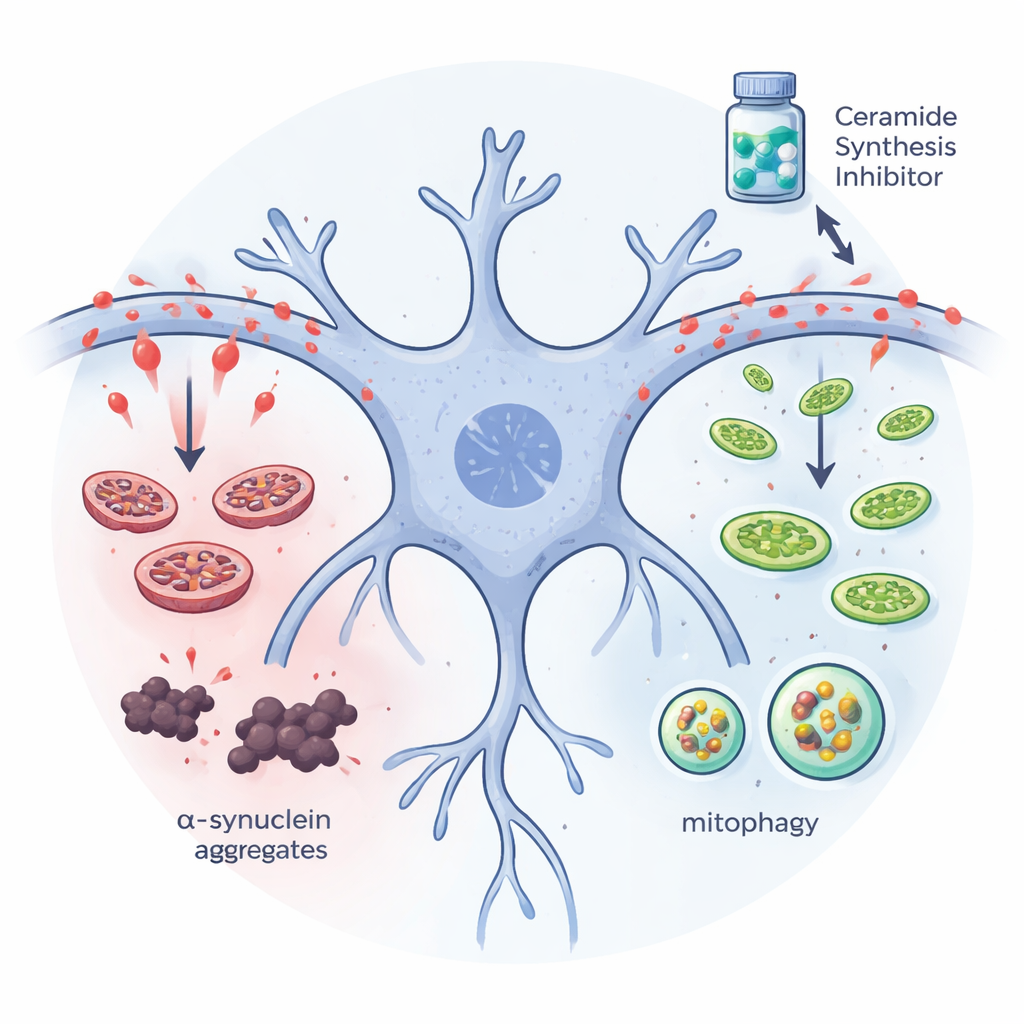
Menschen-Neuronen und Mini-Gehirne bestätigen die Ergebnisse
Um die Ergebnisse näher an die Patienten zu bringen, verwendete das Team Neuronen und dreidimensionale Mittelhirn-Organoide, die aus induzierten pluripotenten Stammzellen von Menschen mit Parkinson gezüchtet wurden. In patientenabgeleiteten Neuronen mit einem fluoreszenten Sensor für Mitophagie steigerte die Myriocin-Behandlung das Signal, das beschädigte Mitochondrien markiert, die zu den zellulären Recyclingzentren transportiert werden, und verbesserte die Architektur des Mitochondriennetzwerks. In Mittelhirn-Organoiden bewahrte Myriocin dopaminproduzierende Zellen und reduzierte schädliche Alpha‑Synuclein-Aggregate. Wenn die Forschenden diesen Mini-Gehirnen zusätzliche Ceramide zufügten, trat das Gegenteil ein: Es bildeten sich mehr Proteinaggregate und Dopaminneurone gingen verloren, insbesondere in Organoiden von Parkinson-Spendern. Diese Experimente stützen eine direkte, schädliche Rolle der Ceramid-Akkumulation in für Menschen relevanten Geweben.
Was das für künftige Therapien bedeuten könnte
Für Laien ist die Kernbotschaft klar: In mehreren Parkinson-Modellen scheint zu viel eines bestimmten Gehirnfetts Zellen zu vergiften, indem es Proteinaggregate, fehlerhafte Mitochondrien und chronische Entzündungen fördert. Das Blockieren des Hauptwegs, der diese Fette synthetisiert — mithilfe des experimentellen Wirkstoffs Myriocin — linderte diese Probleme, schützte gefährdete Neurone und verbesserte das Verhalten bei Mäusen, während es auch menschliche Neurone in vitro rettete. Die Autorinnen und Autoren betonen, dass Langzeitsicherheit und Dosierung beim Menschen unbekannt sind und dass Parkinson viele Ursachen jenseits der Ceramide hat. Dennoch eröffnet die Arbeit eine neue Angriffsroute: Statt nur das schwächer werdende Dopaminsignal zu verstärken, könnten zukünftige Therapien auch den Lipidstoffwechsel und das zelluläre Aufräumen normalisieren und den Gehirnzellen eine bessere Chance geben, dem langsamen Fortschreiten der Neurodegeneration zu widerstehen.
Zitation: Lee, E., Park, My., Park, M. et al. Inhibition of de novo ceramide synthesis mitigates alpha-synuclein pathology in a Parkinson’s disease mouse model. npj Parkinsons Dis. 12, 49 (2026). https://doi.org/10.1038/s41531-026-01263-5
Schlüsselwörter: Morbus Parkinson, Ceramid, Alpha-Synuclein, Mitophagie, Neurodegeneration