Clear Sky Science · de
Höhlenkorrosionshemmung von Edelstahl durch NaNO3: Mechanistische Einblicke in Sulfidauflösung, Depassivierung und aktive Auflösung
Warum winzige Rostflecken wichtig sind
Von Brücken und Wolkenkratzern bis zu Autos und Chemieanlagen wird Edelstahl gewählt, weil er sich normalerweise gegen Rost behauptet. Unter bestimmten Bedingungen kann er jedoch plötzlich winzige, tiefe Löcher – sogenannte Pitting‑Löcher – ausbilden, die zu gefährlichen Rissen anwachsen können. Diese Studie stellt eine praxisnahe Frage für die Industrie: Kann ein weit verbreiteter, relativ sicherer Stoff – Natriumnitrat – verhindern, dass diese Löcher überhaupt entstehen, und wenn ja, wie? Die Antwort könnte dazu beitragen, kritische Infrastruktur länger sicher zu halten und dabei Zusätze zu verwenden, die kostengünstig und weniger umweltschädlich sind. 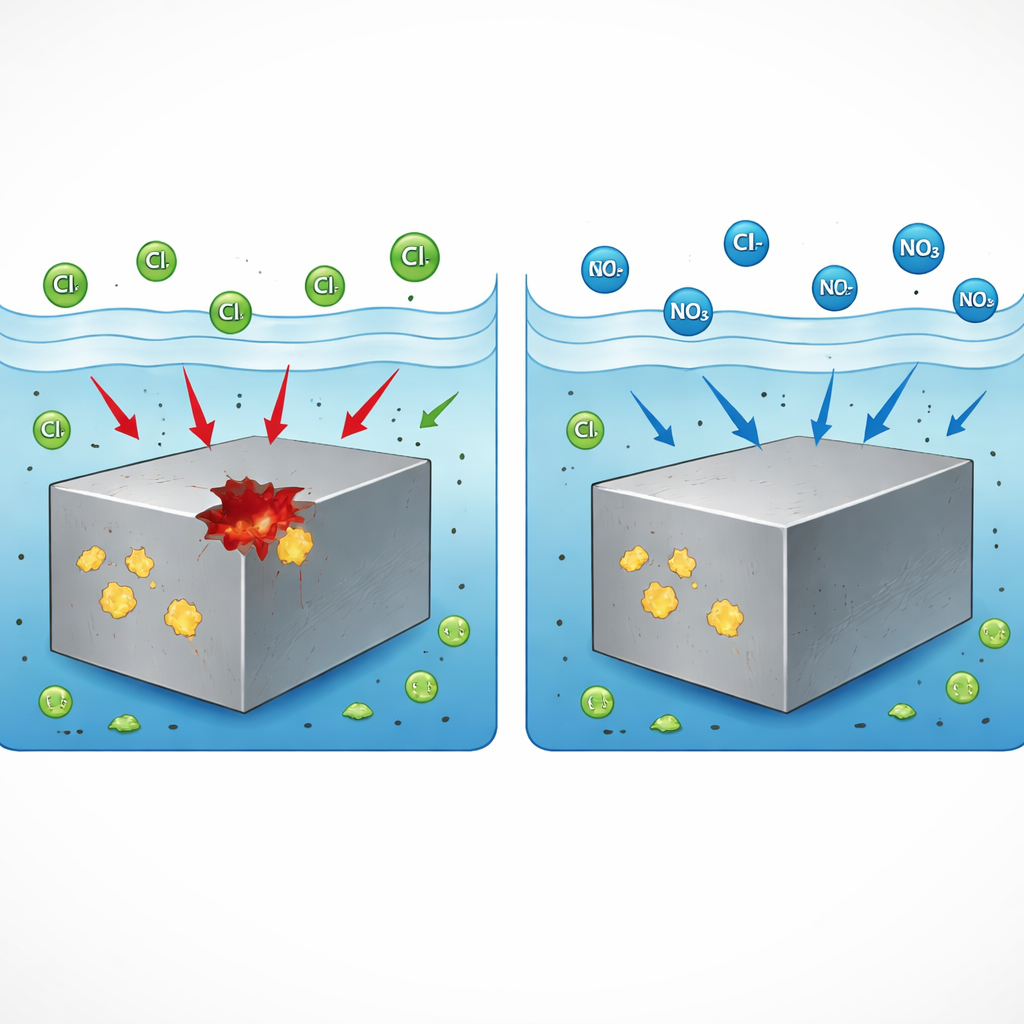
Versteckte Schwachstellen im Edelstahl
Selbst die besten Edelstähle sind nicht vollkommen einheitlich. Eingelagert finden sich mikroskopische, schwefelreiche Partikel, bekannt als Sulfideinschlüsse. Zwei wichtige Typen basieren auf Mangan (MnS) bzw. Calcium (CaS). Diese Einschlüsse wirken wie eingebaute Schwachstellen, an denen sich bevorzugt Pitting bildet, wenn chloridhaltiges Wasser, etwa Sprühnebel oder Kühlwasser, das Metall berührt. Frühere Arbeiten zeigten, dass die Bildung von Pitting einem wiederkehrenden Ablauf folgt: Das Sulfidpartikel beginnt sich aufzulösen, die Schutzschicht am benachbarten Stahl reißt ein und anschließend löst sich das umliegende Metall schnell auf und gräbt eine Grube. Die vorliegende Studie vergleicht zwei kommerzielle Typ‑304‑Edelstähle – einen mit vorwiegend MnS‑Einschlüssen und einen mit CaS‑basierten Einsprengseln – um zu verstehen, ob Nitrat diesen Ablauf an einem oder beiden Einschlusstypen unterbrechen kann.
Prüfung gängiger Zusätze in Salzwasser
Die Forschenden tauchten die Stähle in eine einfache Kochsalzlösung und trieben das Metall schrittweise in stärker korrosive Bedingungen, während sie beobachteten, wann sich stabile Pits bildeten. Sie verglichen drei Zusätze in realistischen Konzentrationen: Ammonium, Nitrit und Nitrat, jeweils als Natrium‑ oder Ammoniumsalze. Nur Nitrat zeigte eine auffällige Wirkung. In beiden, dem MnS‑reichen wie dem CaS‑reichen Stahl verhinderte bereits eine moderate Menge Natriumnitrat vollständig die Bildung stabiler Pits im getesteten Bereich, während die beiden anderen Zusätze keine Verbesserung brachten. Mikroskopische Untersuchungen bestätigten, dass ohne Nitrat Pitting tatsächlich an Sulfid‑Einschlüssen begann, während diese Einschlüsse bei Anwesenheit von Nitrat keine schädlichen Löcher mehr auslösten. Das zeigte, dass Nitrat ein breit wirksamer Pitting‑Hemmer für verschiedene Sulfidtypen ist und kein Einzelfall.
Genauer hinsehen: Was Nitrat verändert – und was nicht
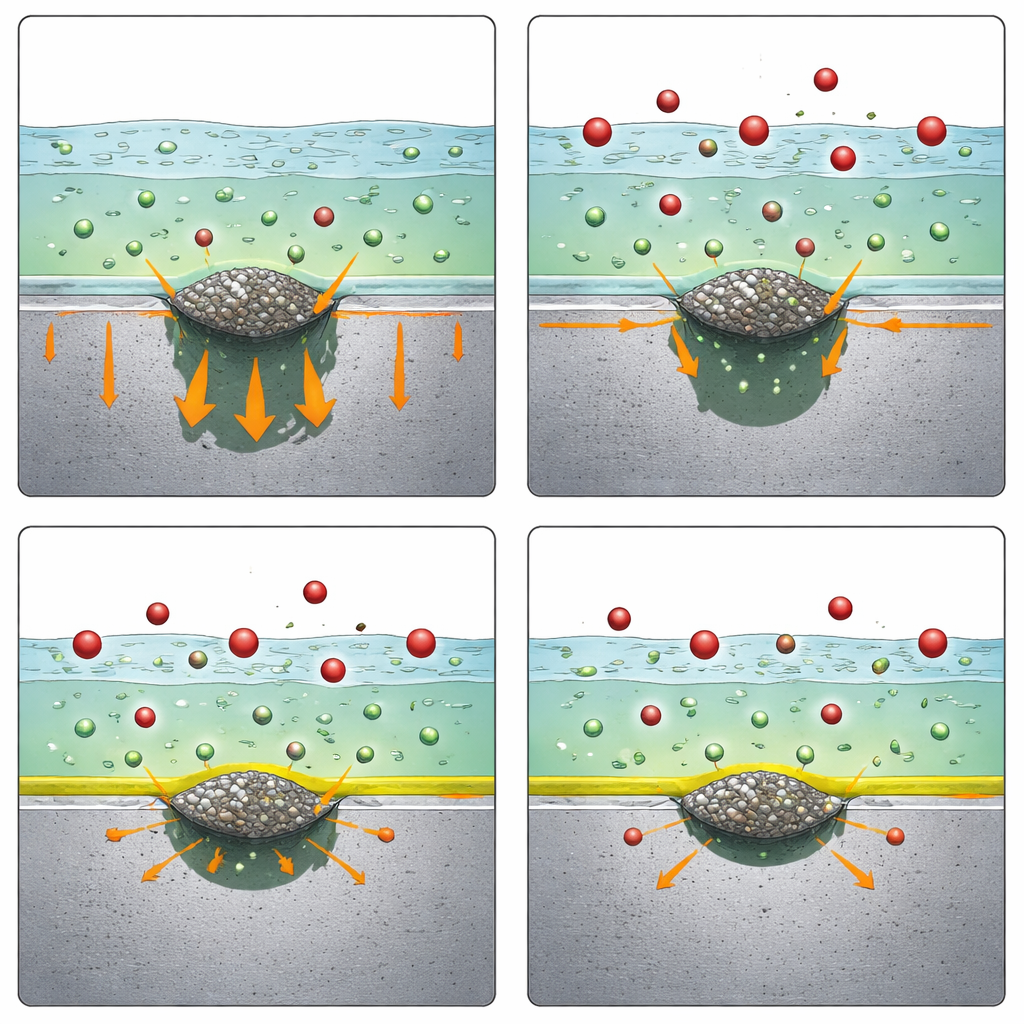
Um herauszufinden, wie Nitrat wirkt, zoomen die Forschenden in die frühen Stadien der Pitting‑Initiation um einzelne MnS‑Partikel mithilfe winziger Elektroden und hochauflösender Bildgebung. Sie beobachteten, dass Nitrat die Auflösung der MnS‑Partikel selbst nicht verhinderte, ebenso wenig veränderte es die kleinen Gräben, die an der Kontaktstelle zwischen Einschluss und umgebenem Stahl entstehen. Nitrat verschob auch nicht den pH‑Wert, bei dem die schützende Schicht des Stahls in Chloridlösung versagt. All dies deutet darauf hin, dass die ersten Schritte der Pitting‑Initiation – Schwächung und Störung rund um den Einschluss – in Gegenwart von Nitrat weitgehend unverändert ablaufen.
Das Verlangsamen der finalen Ausbreitung
Der entscheidende Unterschied zeigte sich, als die Forschenden die harte Chemie innerhalb eines bereits gebildeten Pits nachstellten: sehr sauer, chloridreich. Mit starken Säurelösungen, die die Chemie tief im Inneren eines Pits nachahmen, stellten sie fest, dass der Stahl üblicherweise zwei deutliche Ausbrüche schneller Metallauflösung zeigt, wenn die Spannung erhöht wird. Nitrat reduzierte konsistent den ersten Ausbruch der Auflösung, sowohl in reiner Säure als auch in Säure, die Schwefelarten enthielt, wie sie bei der Auflösung von MnS freigesetzt werden. Oberflächenbeobachtungen zeigten einen gleichmäßigen Angriff, jedoch mit deutlich geringerer Rate. Zusätzliche Tests, bei denen Säuregehalt und Chloridniveau variiert wurden, legen nahe, dass Nitrats Wirkung sich nicht einfach durch Verdünnung der Säure, Verdrängung von Chlorid oder Stabilisierung von Salzkrusten erklären lässt. Stattdessen deuten die Ergebnisse darauf hin, dass Nitrat das Chrom im Legierungsgefüge unterstützt, eine stabilisierende Oberflächenschicht zu bilden, die wiederum die frühe, kritischste Phase des aktiven Metallverlusts verlangsamt.
Was das für reale Stähle bedeutet
Kurz gesagt: Nitrat verhindert nicht die ersten chemischen Angriffe an winzigen Sulfidpartikeln im Edelstahl, aber es verlangsamt die finale, außer Kontrolle geratene Phase, in der eine harmlose Unvollkommenheit in ein gefährliches Pit umschlägt. Indem es diesen Ausbruch des Metallverlusts in sauren, salzhaltigen Mikro‑Umgebungen dämpft, hält Natriumnitrat den Stahl eher in einem passiven, selbstschützenden Zustand, selbst wenn Sulfid‑Einschlüsse und Chloridionen vorhanden sind. Da Nitrat relativ preiswert, weniger toxisch als viele Alternativen und bereits in industriellen Wassersystemen gebräuchlich ist, stärkt das Verständnis dieses Wirkmechanismus die Argumente für seinen wohlüberlegten Einsatz als Korrosionsschutzzusatz zur Verlängerung der Lebensdauer von Edelstahlkonstruktionen und -anlagen.
Zitation: Amatsuka, S., Nishimoto, M. & Muto, I. Pitting-corrosion inhibition in stainless steel by NaNO3: mechanistic insights on sulfide dissolution, depassivation, and active dissolution. npj Mater Degrad 10, 40 (2026). https://doi.org/10.1038/s41529-026-00753-4
Schlüsselwörter: Edelstahlkorrosion, Höhlenhemmung, Natriumnitrat, Sulfideinschlüsse, Chloridlösungen