Clear Sky Science · de
Auswirkung elektrochemischer Wasseraufbereitungsverfahren auf die Korrosion von unlegiertem Stahl im städtischen Wasserversorgungsnetz
Warum Ihre Trinkwasserleitungen wichtig sind
Elektrochemische Wasseraufbereitungssysteme werden in Städten immer häufiger eingesetzt, weil sie effizient Schadstoffe entfernen, Wasser enthärten und Keime abtöten. Dieselben elektrischen Reaktionen, die das Wasser reinigen, können jedoch zugleich das Metall der Leitungen, die das Wasser zu unseren Häusern führen, unbeachtet angreifen. Diese Studie untersucht, wie sich eine solche Behandlung auf unlegierten (Kohlenstoff-)Stahl auswirkt, einem häufigen Werkstoff für Rohrleitungen, und erklärt, warum Korrosion deutlich beschleunigt ablaufen kann, wenn elektrische Prozesse und die übliche Chemie von Leitungswasser zusammenwirken.
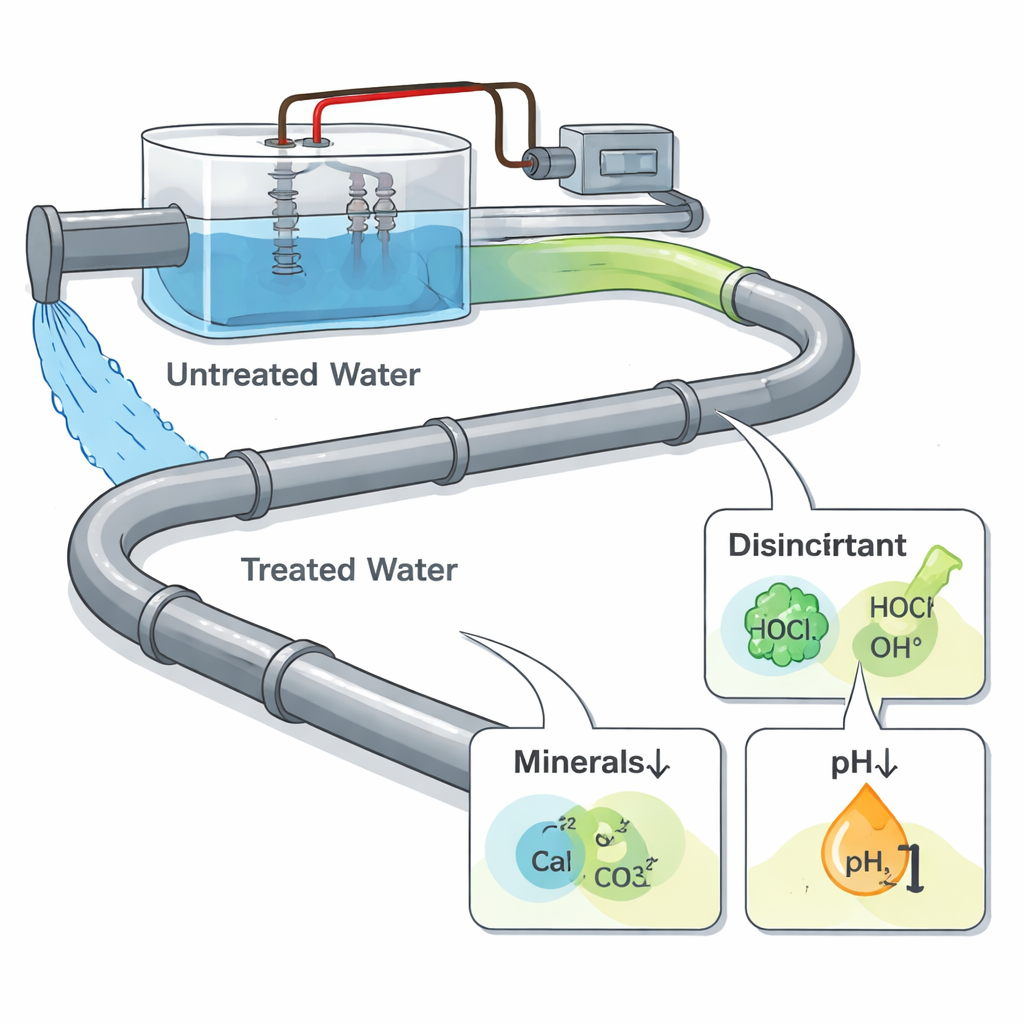
Wasserreinigung mit Strom
Bei der elektrochemischen Wasseraufbereitung wird durch das Wasser ein elektrischer Strom über Metallplatten, sogenannte Elektroden, geleitet. Dadurch lassen sich unerwünschte Ionen entfernen, organische Schadstoffe abbauen und Desinfektionsmittel erzeugen, weshalb das Verfahren für städtische und industrielle Systeme attraktiv ist. Anders als bei einer direkt angeschlossenen Elektroinstallation sind die Rohre selbst jedoch nicht Teil des Stromkreises – sie werden nur dem aus der Einheit austretenden Wasser ausgesetzt. Das bedeutet, dass zusätzliche Korrosion nicht durch direkten Stromfluss im Rohr verursacht wird, sondern durch Veränderungen der Wasserchemie: neue oxidierende Desinfektionsmittel, Verschiebungen des Säuregrads und die Verlagerung von Mineralionen, die normalerweise schützende Schichten an Rohrinnenflächen bilden.
Schnellerer Metallverlust und tiefere, verborgene Schäden
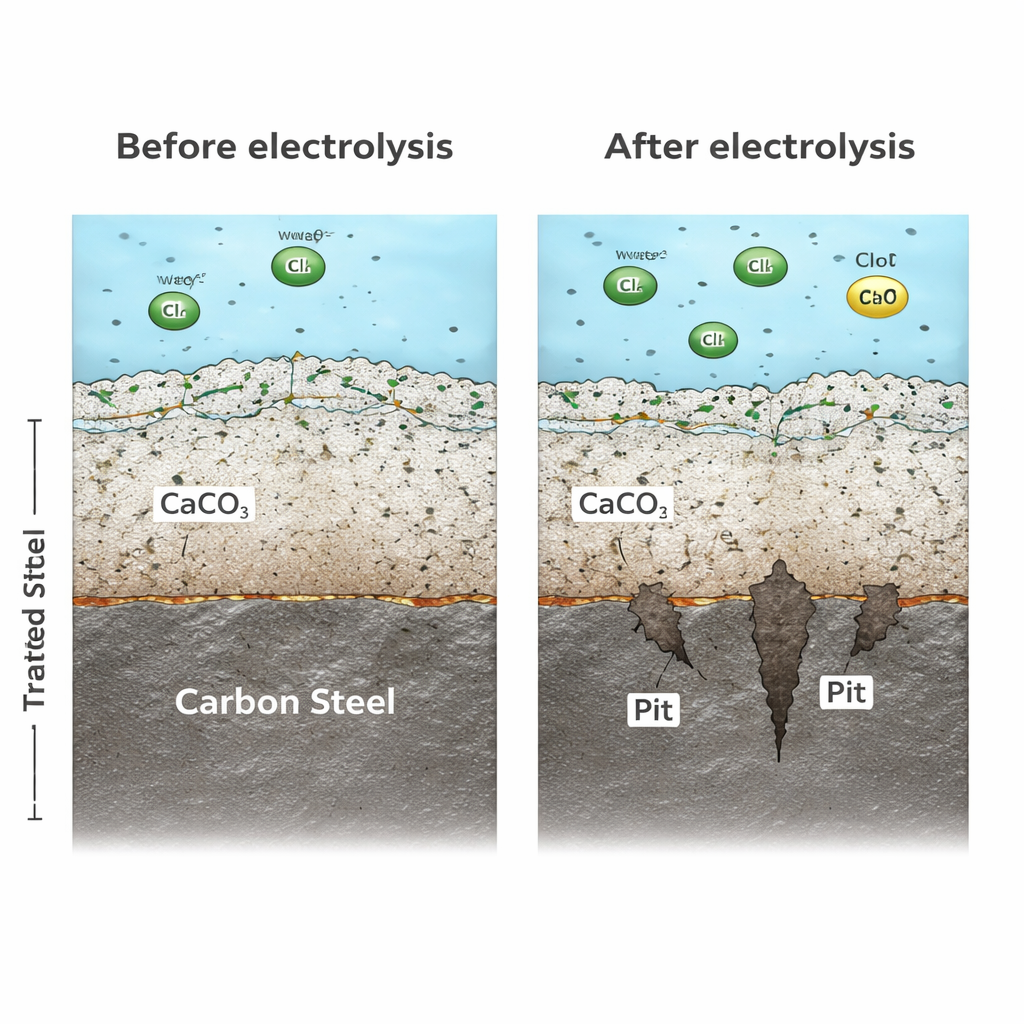
Die Forschenden führten ein 90-tägiges Experiment mit realem Stadtwasser durch und setzten Proben von unlegiertem Stahl verschiedenen Spannungen von 0 bis 9 Volt aus. Sie verfolgten Gewichtsverlust, Oberflächenschäden und elektrochemisches Verhalten. Bereits in den ersten drei Tagen verschlechterte sich die Korrosion durch eingeschaltete Elektrolyse, und mit steigender Spannung nahm der Schaden stets zu. Bei 9 Volt stieg die allgemeine Korrosionsrate mehr als 25-fach im Vergleich zu Wasser, das nicht elektrochemisch behandelt worden war. 3D-Oberflächenscans zeigten außerdem, dass winzige Löcher (Pitting) im Metall mit zunehmender Spannung deutlich tiefer wurden. Bei der höchsten Spannung waren die tiefsten Gruben fast fünfmal tiefer als in unbehandeltem Wasser, wodurch die erwartete Lebensdauer des Stahls erheblich verkürzt wird, selbst wenn der mittlere Metallverlust nicht extrem erscheint.
Warum Schutzschichten versagen
In vielen Rohrleitungen bilden Mineralien aus dem Wasser von selbst eine dünne, dichte Schicht, die das Metall abschirmt. In unbehandeltem Wasser übernimmt Calciumcarbonat häufig diese Schutzfunktion. In elektrochemisch behandeltem Wasser verschwindet dieser Mineralschutz jedoch weitgehend. Weil die Kathode in der Behandlungseinheit Calcium- und Carbonationen anzieht und dort Ablagerungen begünstigt, stehen weniger dieser Ionen zur Verfügung, um eine feste Schutzschicht an den Rohrwänden aufzubauen. Mikroskopie- und Beugungstests zeigten, dass statt einer dichten mineralischen Barriere im Stahl ein lockerer, poröser Rostüberzug mit kleinen, instabilen Kristallen entstand. Diese schwache Beschichtung ließ korrosive Spezies und Elektronen leicht passieren, sodass die Korrosion hoch blieb, anstatt im Laufe der Zeit abzubremsen.
Ein stärkerer chemischer Angriff im Wasser
Um die treibenden Faktoren für den verstärkten Angriff zu identifizieren, trennten die Forschenden verschiedene Effekte. Führten sie die Elektrolyse in einer Sulfatlösung ohne Chlorid durch, veränderten die beim Wasserspalten entstehenden Nebenprodukte – wie Sauerstoff, Wasserstoff und kurzlebige Radikale – das Korrosionsverhalten des Stahls kaum. War jedoch Chlorid, das gleiche Ion wie in gewöhnlichem Kochsalz und in vielen Wasserversorgungen, vorhanden, änderte sich das Bild. Durch Elektrolyse wurde ein Teil des Chlorids in Hypochlorit umgewandelt, ein reaktiveres Desinfektionsmittel. Elektrochemische Messungen zeigten, dass der Stahl in Chloridlösungen mit steigendem Strom deutlich anfälliger für Korrosion wurde. Computersimulationen bestätigten dies: Hypochlorit senkte die Energieschwelle dafür, dass Eisenatome die Metalloberfläche verlassen, wodurch Korrosion leichter ablaufen konnte als mit Chlorid allein. Gleichzeitig verbrauchte die schnelle Bildung von Rostprodukten Hydroxidionen und verschob so den pH-Wert des Wassers in Richtung saurerer Bedingungen, was die Korrosion weiter begünstigte.
Welche Folgen das für Wassersysteme hat
Für Nicht-Fachleute lautet die Kernbotschaft: Die Reinigung und Desinfektion von Wasser mittels Elektrizität ist nicht automatisch schonend für die Leitungen, die dieses Wasser führen. In Systemen, in denen Chlorid enthalten ist, kann die elektrochemische Aufbereitung einen Teil dieses Chlorids in ein stärkeres, korrosiveres Desinfektionsmittel umwandeln und gleichzeitig die Mineralstoffe entziehen, die zum Aufbau eines natürlichen Schutzes nötig sind. Das Ergebnis ist schnellere Metallabtragung und tiefere Pitting-Schäden, die die Lebensdauer von Rohren verkürzen und das Risiko von Lecks oder Kontamination erhöhen können. Die Autorinnen und Autoren empfehlen daher, dass Planer und Betreiber solche Systeme Korrosion als zentrales Gestaltungsproblem behandeln – etwa durch Begrenzung der Spannung, Reduktion des Chlorids vor der Behandlung, Auswahl von Elektroden, die weniger aggressive Nebenprodukte bilden, sowie durch langfristiges Monitoring von Pitting und Wasserchemie –, um sicherzustellen, dass saubereres Wasser nicht auf Kosten einer versagenden Infrastruktur geht.
Zitation: Zhao, S., Jing, Y., He, X. et al. Effect of electrochemical water treatment processes on carbon steel corrosion in urban water supply system. npj Mater Degrad 10, 23 (2026). https://doi.org/10.1038/s41529-026-00736-5
Schlüsselwörter: elektrochemische Wasseraufbereitung, Korrosion von unlegiertem Stahl, städtische Wasserleitungen, Chlorid und Hypochlorit, Haltbarkeit der Wasserinfrastruktur