Clear Sky Science · de
4A-Tetraeder-System: ein synergetischer Rahmen für panvaskuläre Interventionen ermöglicht durch flexible Elektronik
Die Versorgung unserer Blutgefäße neu denken
Panvaskuläre Erkrankungen – Schäden an Blutgefäßen im gesamten Körper – sind inzwischen die weltweit führende Todesursache. Sie können Herz, Gehirn, Nieren und Gliedmaßen betreffen und treten oft ohne Vorwarnung auf. Dieser Artikel skizziert einen mutigen neuen Plan, um diese Erkrankungen mithilfe ultradünner, biegsamer Elektronik und künstlicher Intelligenz anzugehen. Anstatt jeden Eingriff als isoliertes Ereignis zu betrachten, stellen sich die Autoren eine lebenslange, datengetriebene Partnerschaft zwischen Patient und Gerät vor – von der Diagnose über die Operation bis zur langfristigen Nachsorge.
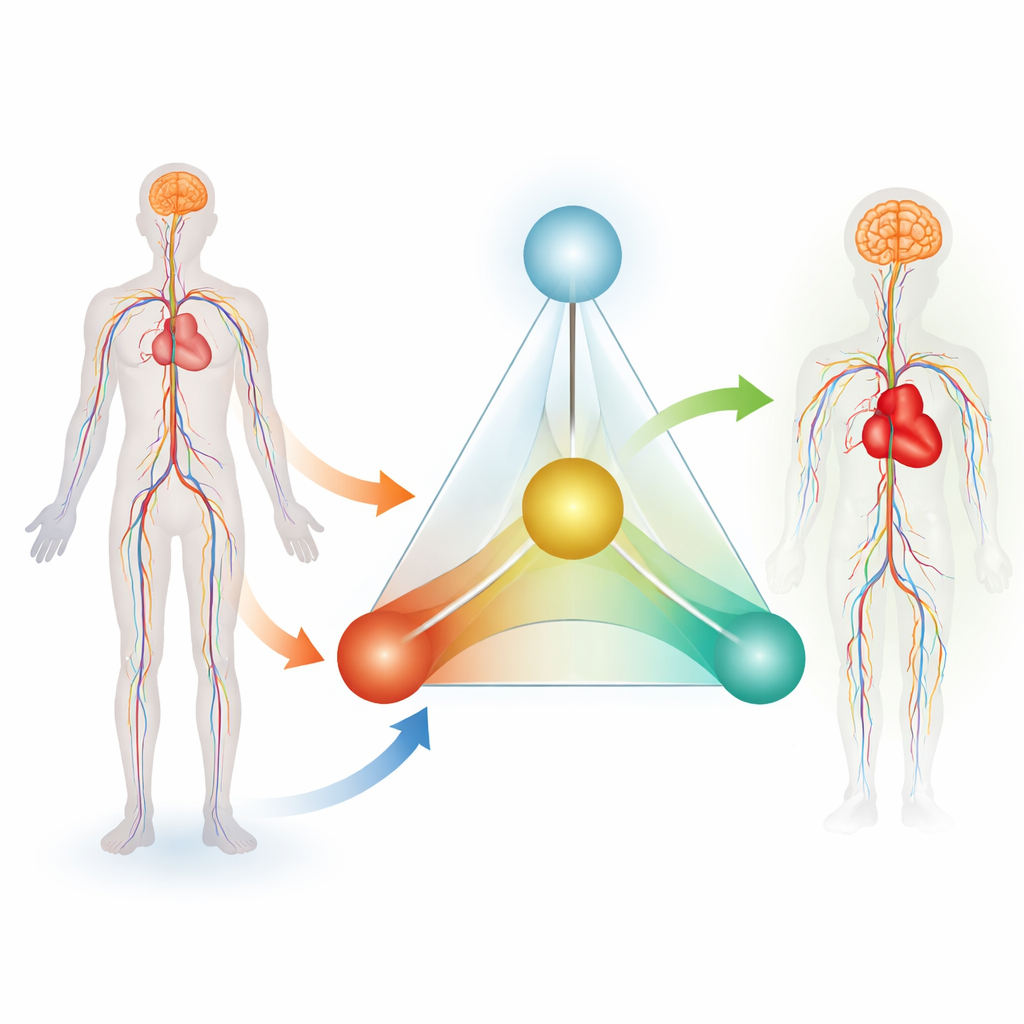
Eine große Idee auf vier Säulen
Die Autoren schlagen das sogenannte „4A-Tetraeder-System“ vor, ein vierteiliger Rahmen zur Behandlung von Gefäßerkrankungen als kontinuierlichem Prozess. Die vier A stehen für Assessment (Beurteilung), Assistance (Unterstützung), Aftercare (Nachsorge) und AI‑Retrofit (KI‑Nachrüstung). Assessment umfasst, wie Ärztinnen und Ärzte sowohl den Patienten als auch die Instrumente vor einem Eingriff bewerten. Assistance konzentriert sich darauf, Instrumente während der Operation sicher durch verschlungene Arterien und Venen zu führen. Aftercare befasst sich mit der Überwachung des Patienten danach, idealerweise rund um die Uhr. Diese drei Elemente verbindet AI‑Retrofit: Künstliche Intelligenz lernt aus allen entlang des Prozesses erzeugten Daten und speist Erkenntnisse zurück, um künftige Geräte und Entscheidungen zu verbessern. Zusammen werden diese vier Elemente als dreiseitige Basis (Assessment, Assistance, Aftercare) dargestellt, die eine Spitze (KI) trägt und so ein Tetraeder bildet, das eine geschlossene, sich selbst verbessernde Versorgungsschleife symbolisiert.
Schonende Tests und intelligentere Implantate
In der Assessment‑Phase heben die Autoren flexible Mikronadelpflaster hervor, die die Haut nur minimal durchdringen, um die interstitielle Flüssigkeit zwischen den Zellen zu entnehmen. Diese Flüssigkeit spiegelt die Blutchémie gut wider, lässt sich aber nahezu schmerzfrei anzapfen. Eingebettete Sensoren in diesen winzigen Nadeln können Marker für Entzündungen, Nierenfunktion, Blutzucker und mehr verfolgen und damit Teile des Labors auf ein auf der Haut getragenes Pflaster verlagern. Gleichzeitig beschreiben die Autoren, wie traditionelle Implantate – wie Stents, künstliche Klappen und Verschlussplugs – mit ultradünnen Druck-, Chemie‑ und Dehnungssensoren aufgerüstet werden könnten. Diese „intelligenten“ Geräte würden nicht nur verschlossene Gefäße wieder eröffnen; sie würden kontinuierlich mechanische Kräfte, Zellverhalten und das chemische Umfeld an der Implantationsstelle messen und so erkennen lassen, ob das Gefäß wirklich heilt oder sich schleichend Problemen nähert.
Instrumente von außen nach innen lenken
Die Assistance‑Phase behandelt ein häufiges Problem moderner Interventionen: das Navigieren von Führungsdrähten und Kathetern durch komplexe Gefäßnetzwerke bei gleichzeitiger Minimierung von Röntgenexposition und Kontrastmittelverbrauch. Die Autoren verweisen auf aufkommende, flexible Ultraschallpflaster und photoakustische Sonden, die Echtzeitbilder von Gefäßen ohne Strahlung liefern können. Sie beschreiben außerdem magnetisch steuerbare, weiche Führungsdrähte und Mikrokatheter, deren Spitzen durch externe Magnetfelder abgelenkt und von Roboterarmen bewegt werden können. In Kombination mit flexiblen Sensoren und intelligenter Bildgebung zielen diese Systeme darauf ab, Geräte mit Submillimeterpräzision durch haarfeine oder scharf gebogene Gefäße zu führen und so das Risiko von Gefäßrissen, Schlaganfällen oder misslungenen Eingriffen zu verringern.
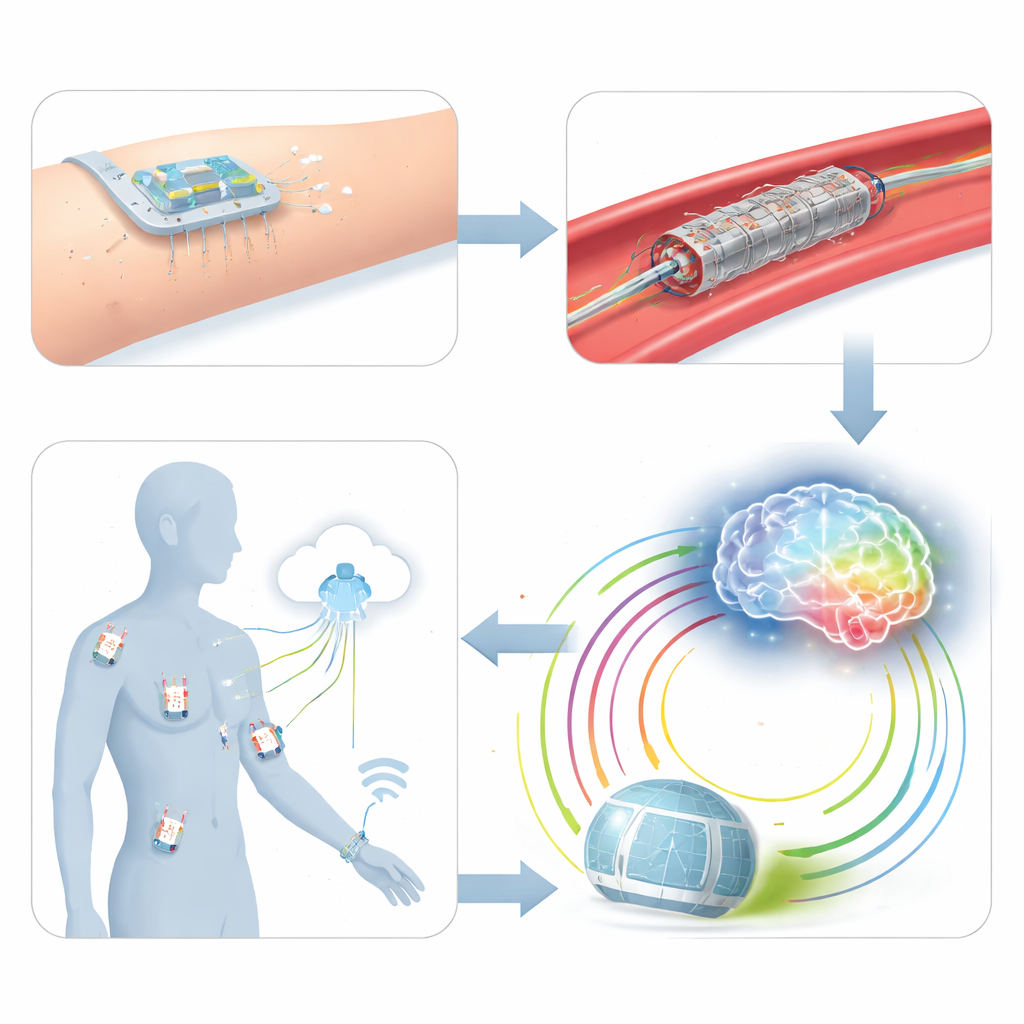
Mit einem Netzwerk stummer Wächter leben
Nach einem Eingriff kehren viele Patientinnen und Patienten heute zu sporadischen Klinikbesuchen und kurzen Kontrollen zurück, wodurch stille Restenosen oder Thromben leicht übersehen werden können. In der Aftercare‑Phase stellen sich die Autoren ein „Internet der medizinischen Dinge“ vor: ein Netz aus tragbaren, halbimplantierbaren und vollständig implantierbaren flexiblen Sensoren, verteilt über Organe und Gewebetiefen. Hautpflaster könnten Herzrhythmus und Atmung überwachen, Mikronadeln Glukose und Entzündungsmarker beobachten, und implantierte Sensoren an Stents oder Arterien würden lokalen Druck und Fluss verfolgen. All diese Daten würden drahtlos in die Cloud gesendet und ein „medizinisches drahtloses Sensornetzwerk“ bilden, das Ärztinnen und Ärzte virtuell am Krankenbett hält und erfasst, wie sich die Erkrankung im gesamten Körper und nicht nur an einer behandelten Stelle entfaltet.
Algorithmen den Kreis schließen lassen
An der Spitze des Tetraeders steht AI‑Retrofit, wo Algorithmen rohe Sensorströme in bessere Versorgung verwandeln. Machine‑Learning‑Modelle können helfen, zuverlässigere Mikronadeln und intelligentere Stents zu entwickeln, risikoreiche Muster in chemischen und Druckdaten zu erkennen, noch bevor Symptome auftreten, und chirurgische Roboter auf sichereren Bahnen zu führen. Deep Reinforcement Learning – Software, die durch Versuch und Irrtum mit historischen Daten lernt – könnte vorschlagen, wie Medikamente angepasst werden sollten oder wann für jeden einzelnen Patienten eine erneute Intervention nötig ist. Große Sprachmodelle könnten eines Tages Sensorausgaben, Bildgebung und Krankenakten zu klaren Zusammenfassungen für Klinikerinnen und Kliniker und verständlichen Erklärungen für Patientinnen und Patienten verweben. In dieser Vision speist jeder Eingriff Informationen zurück in das System und schärft so künftige Entscheidungen.
Vom Konzept zur alltäglichen Versorgung
Für eine fachfremde Leserschaft lautet die Kernbotschaft: Die Versorgung bei Gefäßerkrankungen kann sich von isolierten, reaktiven Einzelmaßnahmen zu einer intelligenten, kontinuierlichen Partnerschaft zwischen Körper, flexibler Elektronik und KI wandeln. Mikronadelpflaster machen Tests schonender, intelligente Implantate überwachen verletzliche Stellen von innen, tragbare und implantierte Sensoren behalten den ganzen Körper im Blick, und lernende Algorithmen verbinden die Informationen über Monate und Jahre. Viele Hürden bleiben – von Langzeitsicherheit und Energieversorgung bis zu Datensicherheit und Regulierung – doch die Autoren argumentieren, dass dieses 4A‑Tetraeder‑Konzept in den nächsten zehn Jahren heutige Einmal‑Gefäßverfahren in ein sich entwickelndes, personalisiertes Schutzsystem gegen die weltweit tödlichste Krankheitsgruppe verwandeln könnte.
Zitation: You, L., Qu, Y., Chen, Y. et al. 4A tetrahedron system: a synergistic framework for panvascular intervention empowered by flexible electronics. npj Flex Electron 10, 35 (2026). https://doi.org/10.1038/s41528-026-00537-5
Schlüsselwörter: flexible Elektronik, Gefäßerkrankung, intelligente Implantate, tragbare Sensoren, medizinische KI