Clear Sky Science · de
Varianten in MTNAP1 verursachen eine neurodegenerative Erkrankung durch Beeinträchtigung der mitochondrialen Stabilität
Warum diese Geschichte für die Gehirngesundheit wichtig ist
Viele Familien erleben das Herzzerreißende, einem Kind zuzusehen, wie es nach und nach Entwicklungsfähigkeiten verliert, ohne klare Diagnose. Diese Studie deckt eine neue genetische Ursache einer solchen Erkrankung auf und verfolgt den Weg von einem fehlerhaften Gen über beschädigte „Kraftwerke“ in den Gehirnzellen bis hin zu rückläufigem Hirngewebe. Das Verständnis dieser Kausalkette liefert nicht nur Antworten für betroffene Familien, sondern schärft auch unser allgemeines Bild davon, wie empfindlich die Energiesysteme des Gehirns tatsächlich sind.
Eine neu erkannte kindliche Gehirnerkrankung
Die Forschenden untersuchten drei Kinder aus zwei nicht verwandten Familien, die alle früh entwickelte Auffälligkeiten zeigten. Sie waren klein für ihr Alter, lernten später sitzen, laufen und sprechen und verloren dann allmählich einige dieser Fähigkeiten. Alle entwickelten Bewegungsstörungen wie unsicheres Gangbild, Muskelsteifheit oder niedrigen Muskeltonus sowie Anfälle. Hirnbilder zeigten ein konsistentes Muster: das Gewebe sowohl des Großhirns als auch des hinteren „Kleinhirns“ wurde mit der Zeit dünner, und eine wichtige Verbindungsbrücke von Nervenfasern, das Corpus callosum, war ungewöhnlich schmal. Diese Merkmale deuteten auf einen fortschreitenden Verlust von Nervenzellen hin und nicht auf eine einmalige Schädigung bei der Geburt.
Ein winziges Gen mit großen Folgen
Um eine erbliche Ursache zu finden, sequenzierte das Team alle protein-codierenden Gene der betroffenen Kinder und ihrer Eltern. Sie konzentrierten sich auf ein Gen namens MTNAP1, das bei der Organisation der DNA in den Mitochondrien, den Energiewerken der Zelle, hilft. Jedes Kind trug zwei defekte Kopien von MTNAP1, eine von jedem gesunden, heterozygoten Elternteil. Bei zwei Geschwistern tauschte eine einzelne „Buchstaben“-Änderung im Gen eine Aminosäure gegen eine andere und verzerrte dadurch subtil die Form des Proteins. Beim dritten Kind erzeugte ein frühes Stopp-Signal im Gen wahrscheinlich überhaupt kein funktionsfähiges Protein. Diese Veränderungen wurden nicht in großen Bevölkerungsdatenbanken beobachtet, was die Annahme stärkt, dass es sich um seltene, schädliche Varianten und nicht um harmlose Varianten handelt.
Kraftwerke unter Stress
Anschließend untersuchten die Wissenschaftler Hautzellen der Kinder und verglichen sie mit Zellen gesunder Personen. Unter dem Mikroskop zeigten normale Zellen lange, fadenförmige Mitochondrien, die ein verbundenes Netzwerk bildeten, während die Zellen der Kinder kurze, gebrochene und verklumpte Mitochondrien enthielten. Wenn die Forschenden experimentell MTNAP1 in einer menschlichen, nervenähnlichen Zelllinie reduzierten, sahen sie denselben Zerfall des mitochondrialen Netzwerks, was bestätigte, dass allein der Verlust dieses Proteins deren Struktur stören kann. Messungen der mitochondrialen Aktivität zeigten, dass Schlüsselstufen der Energieproduktion geschwächt waren und die Zellen überschüssige reaktive Sauerstoffspezies produzierten — schädliche Sauerstoffnebenprodukte, die wie molekularer Rost wirken. Die gestressten Zellen teilten sich nicht mehr richtig, blieben in einer Ruhephase stehen und aktivierten Marker vorzeitiger Zellalterung.
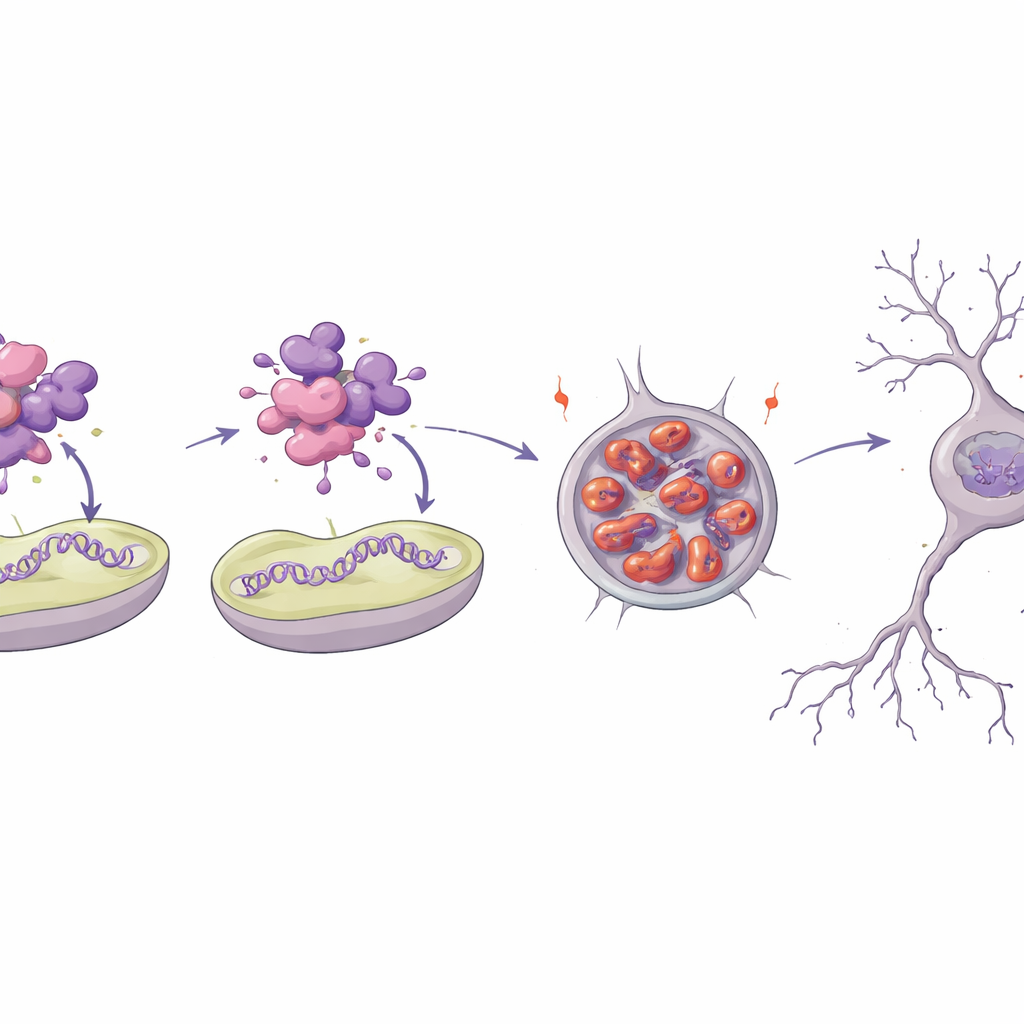
Wie eine einzelne Veränderung ein essentielles Protein zerstört
Um zu verstehen, warum eine der Varianten so schädlich ist, modellierte das Team die 3D-Struktur des MTNAP1-Proteins und stellte es im Labor nach. Die ausgetauschte Aminosäure sitzt in einer eng gepackten Helixregion, die normalerweise dem Protein hilft, mit mitochondrialer DNA und der Innenmembran zu interagieren. Computersimulationen und biophysikalische Tests zeigten, dass das mutante Protein weniger stabil ist, viel von seiner geordneten Struktur verliert und leicht verklumpt. In Reagenzglasversuchen band das normale Protein stark an kurze Stücke mitochondrialer DNA und an künstliche Membranoberflächen, während das mutante kaum wechselwirkte und stattdessen amyloidähnliche Aggregate bildete. Eingebracht in nervenähnliche Zellen, sammelte sich das Mutantprotein im Laufe der Zeit in großen perinukleären Klumpen an — ein Zeichen dafür, dass die Qualitätskontrollsysteme für Proteine überfordert sind.
Von beschädigten Mitochondrien zum versagenden Gehirn
Wenn man die Befunde zusammensetzt, skizziert die Studie ein schrittweises Modell: Fehlerhaftes MTNAP1 schwächt das Gerüst, das die Organisation der mitochondrialen DNA unterstützt und sie an die Innenmembran ankert; dies destabilisiert Mitochondrien, lässt sie fragmentieren und verringert ihre Fähigkeit, effizient Energie zu erzeugen; zunehmender oxidativer Stress und Signale für vorzeitige Zellalterung machen Nervenzellen besonders verwundbar, weil sie hohe und konstante Energiebedarfe haben und nur begrenzt erneuerbar sind. Im sich entwickelnden Gehirn führt diese langsame, andauernde Energiekrise zu aufgehobenen Entwicklungsschritten, Verlust erlernter Fähigkeiten und allmählichem Schrumpfen wichtiger Hirnregionen. Während weitere Patienten- und Tierstudien nötig sind, um das Syndrom vollständig zu kartieren, positioniert diese Arbeit MTNAP1 eindeutig als entscheidenden Wächter der mitochondrialen Stabilität und hebt die Organisation der mitochondrialen DNA als zentralen Pfeiler einer gesunden Gehirnentwicklung hervor.
Zitation: Kumar, A., Saha, S., Nasir, N. et al. Variants in MTNAP1 underlie a neurodegenerative disorder by impairing mitochondrial stability. npj Genom. Med. 11, 19 (2026). https://doi.org/10.1038/s41525-026-00554-3
Schlüsselwörter: Mitochondrien, Neurodegeneration, Pädiatrische Genetik, mitochondriale DNA, Proteinfehlfaltung