Clear Sky Science · de
Teilautomatisches genomisches Neugeborenenscreening zeigt Komplexität der Berichterstattung auf
Warum winzige Blutstropfen große Antworten verbergen können
Innerhalb weniger Tage nach der Geburt durchlaufen die meisten Babys bereits einen stillen, lebensrettenden Test: einen Fersenstich, bei dem Blut auf einer Karte aufgefangen wird. Diese Studie untersucht, was passiert, wenn man einen Schritt weitergeht und aus genau diesem Blut deutlich mehr vom genetischen Code des Babys liest. Die Forscher in Südaustralien wollten herausfinden, ob die Ergänzung routinemäßiger Neugeborenenuntersuchungen um groß angelegte DNA-Analysen mehr behandelbare Erkrankungen frühzeitig und sicher aufdecken kann – ohne Familien und Ärztinnen und Ärzten verwirrende oder nicht hilfreiche Informationen aufzubürden.
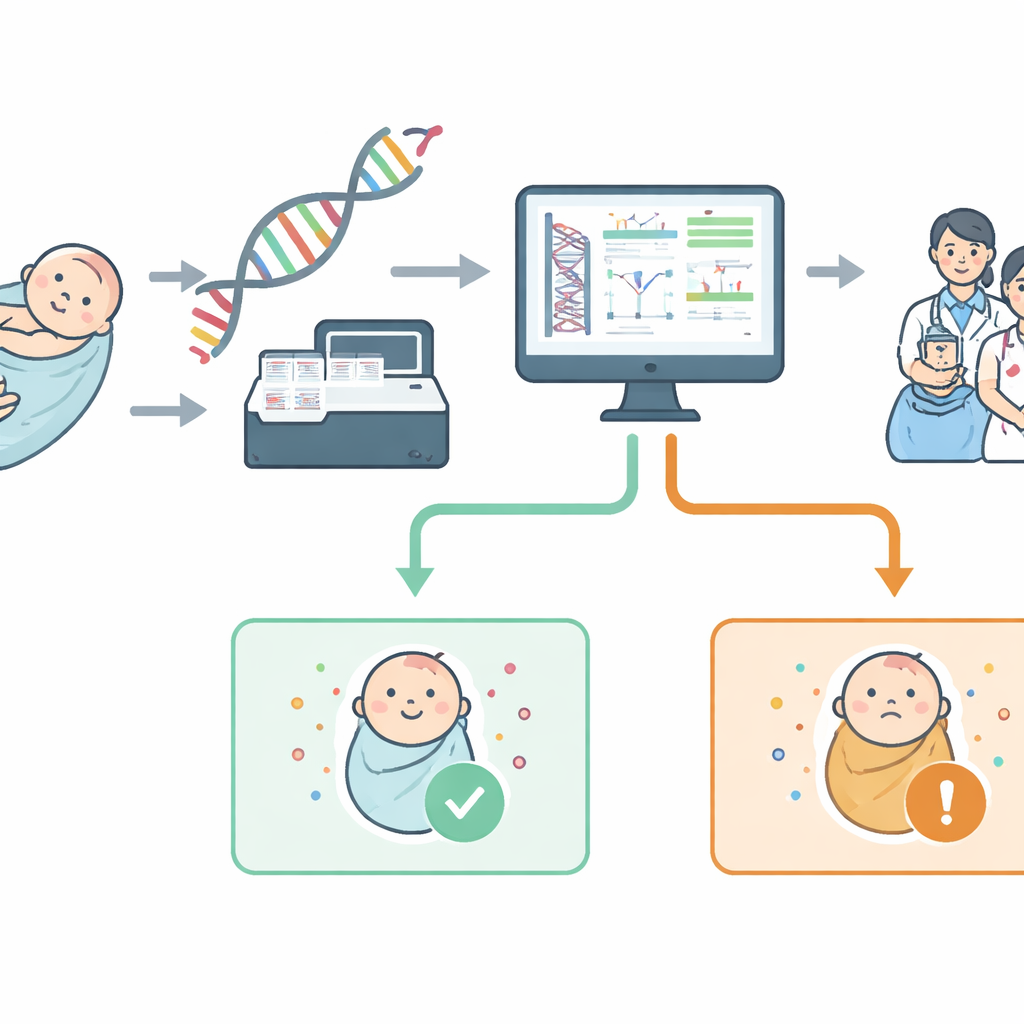
Vom Fersenstich bis zum Genomscan
Das traditionelle Neugeborenenscreening sucht durch Messung von Blutchemikalien nach einigen Dutzend Erkrankungen. Im Gegensatz dazu liest das genomische Screening Abschnitte der DNA, um direkt nach krankheitsverursachenden Veränderungen in bestimmten Genen zu suchen. Das NewbornsInSA-Projekt entwickelte einen Test auf Basis der Gesamtgenomsequenzierung, beschränkte die Suche jedoch bewusst auf ein „virtuelles“ Panel von 613 Genen. Diese Gene wurden gemeinsam mit lokalen Ärztinnen und Ärzten nach einfachen Regeln ausgewählt: Die Erkrankung sollte im Kindesalter beginnen, ernsthafte Gesundheitsprobleme verursachen, eine sinnvolle Behandlung oder Präventionsstrategie haben und im Labor zuverlässig nachweisbar sein. Öffentlichkeits- und Patientengruppen halfen anschließend, diese Erkrankungen in vertraute Körpersystem-Kategorien zu gruppieren, damit Eltern besser verstehen können, was der Test abdeckt.
Den neuen Test auf die Probe stellen
Bevor das DNA-basierte Screening neuen Familien angeboten wurde, musste das Team nachweisen, dass es funktioniert. Sie zogen 46 gelagerte Blutkarten von Kindern heran, deren genetische Diagnosen bereits bekannt, den Analytikern jedoch verborgen waren. Mithilfe von Gesamtgenomsequenzierung und zwei verschiedenen Software-Systemen prüften sie, ob ihre Pipeline Babys mit einer der Zielerkrankungen korrekt erkennen würde. Das Ergebnis war ermutigend: Der Prozess fand 97 % der wahren Fälle und erzeugte nach Expertenprüfung keine Fehlalarme. Der eine verpasste Fall machte eine zentrale Einschränkung jedes genbasierten Screenings deutlich – wenn die wissenschaftliche Grundlage für eine spezifische DNA-Veränderung unvollständig ist, können Computer und selbst Expertinnen und Experten gezwungen sein, sie als „unsicher“ zu kennzeichnen und als Nicht-Befund zu behandeln.
Die Computer die schwere Arbeit machen lassen
Das Lesen eines gesamten Genoms erzeugt für jedes Baby Tausende von Varianten, weit zu viele, als dass Menschen sie einzeln prüfen könnten. Um damit umzugehen, entwickelten die Forscher einen teilautomatisierten Arbeitsablauf. Eigene Skripte, eingebunden in eine kommerzielle Analyseplattform, scannen die annotierte Variantenliste und stufen automatisch Babys als „geringe Wahrscheinlichkeit“ ein, bei denen klar keine besorgniserregenden Befunde vorliegen. Nur Fälle mit Veränderungen, die potenziell schädlich erscheinen – wie bekannte krankheitsverursachende Varianten oder wahrscheinlich schädigende Genunterbrechungen – werden an Expertinnen und Experten zur detaillierten Überprüfung weitergegeben. Bei den ersten 100 getesteten Neugeborenen verringerte diese Automatisierung sofort die Zahl der Babys, die einer manuellen Prüfung bedurften, um mehr als die Hälfte – ein entscheidender Schritt, wenn ein solches Screening auf ganze Populationen ausgedehnt werden soll.
Echte Babys, echte Entscheidungen
Als das Team den Arbeitsablauf auf die ersten 100 eingeschriebenen Neugeborenen anwendete, erhielten fünf Babys Ergebnisse, die auf eine hohe Wahrscheinlichkeit für eine bestimmte Erkrankung hinwiesen. Dazu gehörten Herzrhythmusstörungen, die gefährliche unregelmäßige Schläge verursachen können, ein Stoffwechselproblem, das bereits durch das Standard-Screening vermutet worden war, eine Genveränderung, die bestimmte Antibiotika für das Gehör riskant macht, und eine milde Form angeborener hoher Blutzuckerwerte. In jedem Fall löste das Ergebnis maßgeschneiderte Folgemaßnahmen aus: Herzuntersuchungen und fortlaufende Überwachung, elektronische Hinweismechanismen zum Vermeiden bestimmter Medikamente oder Planung der zukünftigen Schwangerschaftsbetreuung. Gleichzeitig wurden viele andere Befunde bewusst nicht berichtet, weil sie mit milden Symptomen, erwachsenenbeginnenden Krebserkrankungen, unsicherem Risiko oder komplexen Mustern verknüpft waren, die gegenwärtiges Wissen bei einem gesunden Neugeborenen nicht zuverlässig interpretieren kann. Solche schwierigen Entscheidungen erforderten Stunden des Studiums der Fachliteratur und Diskussionen unter Genetikerinnen und Genetikern sowie Fachärztinnen und Fachärzten, was unterstreicht, dass fachliche Urteilsbildung weiterhin wichtig ist.
Das Gleichgewicht zwischen früher Hilfe und zukünftiger Belastung
Diese Arbeit zeigt, dass es technisch möglich ist, aus einem winzigen Blutstropfen Gesamtgenomdaten zu nutzen, um mehr behandelbare kindliche Erkrankungen zu erkennen als mit Standardtests, und das mit hoher Genauigkeit und Unterstützung durch clevere Software. Sie legt jedoch auch die ethische und praktische Gratwanderung offen: Jedes zusätzliche geprüfte Gen erhöht die Wahrscheinlichkeit, Informationen zu finden, die dem Baby jetzt nicht helfen, Eltern beunruhigen oder erst Jahrzehnte später relevant werden könnten. Der teilautomatisierte, sorgfältig kuratierte Ansatz des NewbornsInSA-Teams – bei dem Computer klare Negative ausschließen und Menschen sich auf nuancierte Fälle konzentrieren – bietet eine Blaupause dafür, wie genomisches Neugeborenenscreening verantwortungsvoll eingeführt werden könnte, während begleitende Studien die realen Nutzen und Risiken für Familien weiter verfolgen.
Zitation: Chowdhury, A., Marri, S., Anastasi, L. et al. Semi-automated genomic newborn screening highlights complexities in reporting. npj Genom. Med. 11, 13 (2026). https://doi.org/10.1038/s41525-026-00553-4
Schlüsselwörter: genomisches Neugeborenenscreening, Gesamtgenomsequenzierung, getrocknete Blutproben, Interpretation genetischer Varianten, Früherkennung seltener Krankheiten