Clear Sky Science · de
Transkriptomische Analyse zur Aufklärung des Mechanismus der Radiosensibilisierung von AR-positiven triple-negativen Mammakarzinomen durch AR-Hemmung
Warum diese Studie für Menschen mit Brustkrebs wichtig ist
Die Strahlentherapie ist ein Grundpfeiler der Behandlung vieler Menschen mit aggressiven Brustkrebserkrankungen, doch einige Tumoren sind von Natur aus schwerer mit Strahlung zu vernichten als andere. Diese Studie stellt eine praktische Frage mit unmittelbarer klinischer Relevanz: Können eine Klasse von Medikamenten, die männliche Hormon-Signale blockieren und bereits bei Prostatakrebs eingesetzt werden, eine Untergruppe von triple-negativen Brustkrebserkrankungen strahlungsempfindlicher machen — und warum wirkt das in manchen Fällen, in anderen aber nicht?
Eine schwer zu behandelnde Form von Brustkrebs
Triple-negative Brustkrebserkrankungen fehlen drei gängige molekulare Ziele — Östrogenrezeptoren, Progesteronrezeptoren und HER2 — sodass Patientinnen und Patienten oft allein auf Operation, Chemotherapie und Strahlentherapie angewiesen sind. Ein Teil dieser Tumoren trägt jedoch den Androgenrezeptor, ein Protein, das auf Hormone ähnlich wie Testosteron reagiert und das Tumorwachstum antreiben kann. Frühere Arbeiten zeigten, dass das Blockieren dieses Rezeptors das Wachstum verlangsamen und die Wirkung der Strahlung verstärken kann, doch die genauen Mechanismen und welche Medikamente und Tumoren am meisten profitieren, waren unklar.
Testen moderner Hormonblocker in Kombination mit Strahlung
Die Forschenden untersuchten mehrere Labormodelle von triple-negativen Brustkrebszellen, die sich hauptsächlich durch unterschiedliche Androgenrezeptor-Mengen unterschieden. Sie konzentrierten sich auf zwei neuere Anti-Androgen-Medikamente, Apalutamid und Darolutamid, und kombinierten kurze Expositionen gegenüber diesen Wirkstoffen mit Standarddosen Röntgenstrahlung. In Zellen mit hohen Androgenrezeptor-Spiegeln erhöhte Apalutamid deutlich die strahlungsbedingten Schäden, sodass weniger Zellen in der Lage waren, neue Kolonien zu bilden. Darolutamid hingegen hatte in denselben Zellen wenig bis keinen Einfluss auf die Strahlungsempfindlichkeit, und keines der beiden Medikamente half in Zellen mit sehr geringer Androgenrezeptor-Expression. Diese Befunde legen nahe, dass nicht alle Androgenblocker in Brustkrebs gleich wirken und dass Tumoren stark vom Rezeptor abhängen müssen, damit die Kombination effektiv ist.
Beobachtung eines Schlüsselproteins innerhalb der Zelle
Um zu verstehen, was nach Hormon-Signalen oder Strahlung in Krebszellen geschieht, verfolgte das Team, wo sich der Androgenrezeptor selbst befindet. Bei Exposition mit einem synthetischen Androgen wanderte der Rezeptor in den Zellkern, das Kontrollzentrum, in dem Gene an- und ausgeschaltet werden. Strahlung allein veranlasste den Rezeptor nicht, den Kern zu verlassen; tatsächlich blieb er nach der Behandlung dort und war bereit, die Genaktivität zu beeinflussen. Wenn die Zellen jedoch vor der Strahlung das Anti-Androgen Enzalutamid erhielten, sanken die Kernwerte des Rezeptors und ein größerer Anteil verblieb im Zytoplasma. Dies stützt die Vorstellung, dass das Blockieren des Kerntransports des Rezeptors dessen Fähigkeit beeinträchtigt, nach Strahlung ein schützendes Genprogramm zu starten.
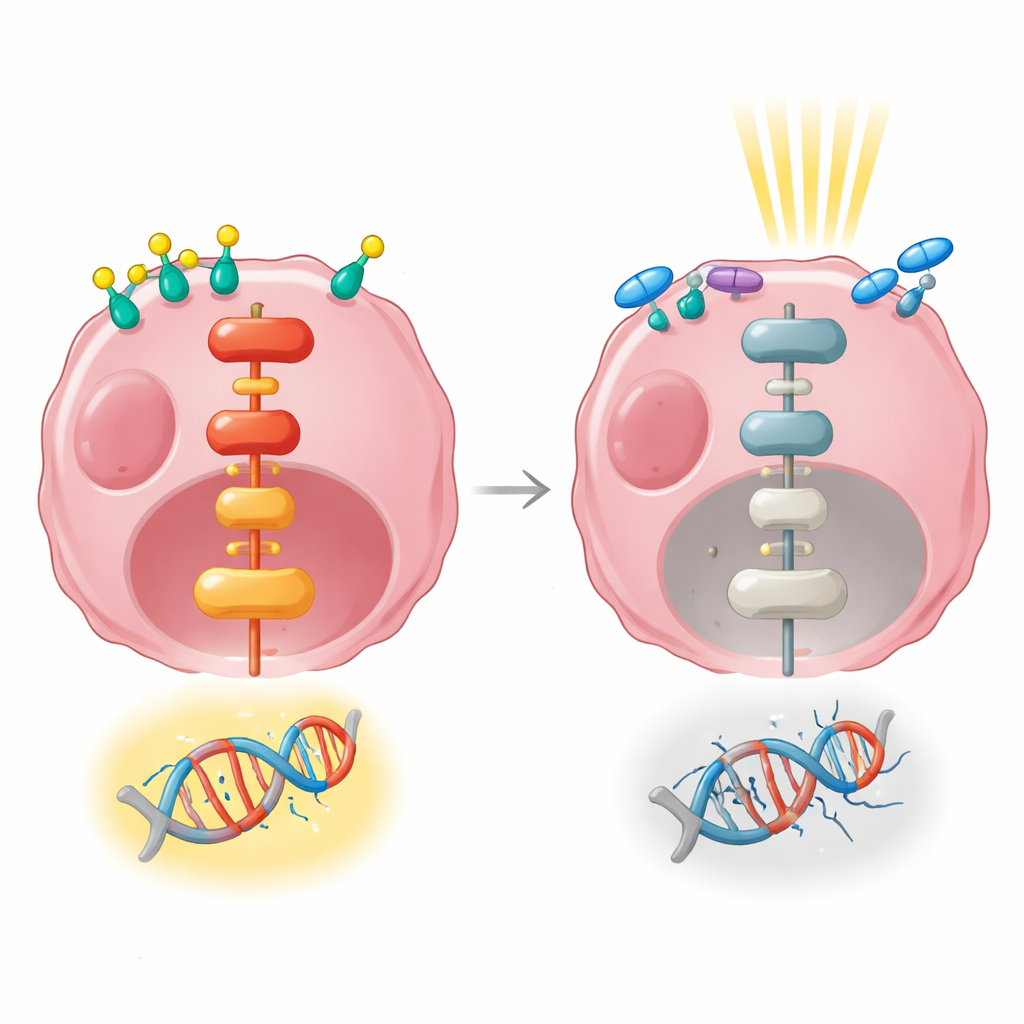
Gen-Signale, die Hormone mit Resistenz verbinden
Die Forschenden nutzten anschließend RNA-Sequenzierung, um einen breiten Überblick darüber zu erhalten, welche Gene nach Hormonstimulation, Strahlung oder beidem hoch- oder runterreguliert wurden. Allein die Hormonbehandlung veränderte die Aktivität von Hunderten von Genen und beeinflusste stark Signalwege, die Zellwachstum, Zellhaftung und Kommunikation mit der Umgebung steuern. Die Strahlung allein veränderte zu einem frühen Zeitpunkt deutlich weniger Gene. Bei Kombination von Hormonstimulation und Strahlung wurden viele derselben wachstumsbezogenen Signalwege aktiviert, einschließlich einer wichtigen Signalroute, bekannt als MAPK/ERK, die Signale von der Zelloberfläche zum Zellkern weiterleitet. Dieser Weg ist dafür bekannt, Zellen beim Überleben und bei der Reparatur von DNA-Schäden zu unterstützen.
Untersuchung eines Überlebenswegs, der die DNA schützt
Da die MAPK/ERK-Signalgebung in ihren Analysen wiederholt auftauchte, prüften die Forschenden, ob die Verstärkung dieses Weges den Nutzen der Androgenblockade bei Strahlung zunichtemachen könnte. Sie konstruierten Krebszellen so, dass diese eine ständig aktive Version von ERK überproduzierten, einem Schlüsselkomponenten des Weges, und wiederholten dann die Behandlung mit Strahlung plus Apalutamid. In diesem Setting machte Apalutamid die Zellen nicht mehr strahlungsempfindlicher: Das verstärkte ERK-Signal schien sie zu schützen. Zusammen mit Proteinmessungen deuten diese Ergebnisse darauf hin, dass die MAPK/ERK-Signalgebung eine kritische Verbindung zwischen Androgenrezeptor-Aktivität und der Fähigkeit der Zelle zur Reparatur strahlungsinduzierter DNA-Brüche darstellt.
Was das für die zukünftige Brustkrebsversorgung bedeutet
Einfach gesagt deutet diese Arbeit darauf hin, dass einige triple-negative Brustkrebse Strahlung über Androgen-abhängige Signale überleben, die einen internen Überlebensschaltkreis aktivieren, der ihnen bei der Reparatur geschädigter DNA hilft. Medikamente wie Apalutamid und Enzalutamid können diesen Schaltkreis in Tumoren unterbrechen, die stark vom Androgenrezeptor abhängig sind, und so die Wirksamkeit der Strahlung steigern, während Tumoren mit niedrigen Rezeptorwerten oder alternativen Überlebenswegen möglicherweise nicht profitieren. Indem die Studie die beteiligten Genwege — insbesondere die MAPK/ERK-Route — abbildet, legt sie die Grundlage für gezieltere Kombinationen von Hormonblockern, Signalweg-Inhibitoren und Strahlentherapie, die die Ergebnisse für Patienten mit dieser schwer zu behandelnden Brustkrebsform verbessern könnten.
Zitation: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
Schlüsselwörter: triple-negativer Brustkrebs, Androgenrezeptor, Strahlentherapie, Radiosensibilisierung, MAPK-ERK-Signalgebung