Clear Sky Science · de
Programmierbare lokale Immunochemotherapie für dreifach-negativen Brustkrebs durch räumlich-zeitlich gesteuerte Freisetzung von CpG-Oligodeoxynukleotiden, Gemcitabin und Paclitaxel
Aus einem schwierigen Brustkrebs ein lokales Ziel machen
Dreifach-negativer Brustkrebs gehört zu den schwierigsten Formen von Brustkrebs, weil er die üblichen molekularen Schalter vermissen lässt, an die viele moderne Medikamente andocken. Patientinnen und Patienten sind oft auf kraftvolle Chemotherapien angewiesen, die den ganzen Körper durchströmen, schwere Nebenwirkungen verursachen und nicht selten enttäuschende Langzeitkontrollen liefern. Diese Studie untersucht eine sehr andere Idee: Anstatt den Körper mit Medikamenten zu überfluten, könnte man ein winziges, programmierbares Medizin-Depot neben dem Tumor platzieren, das Chemo- und immunstärkende Wirkstoffe in einer sorgfältig abgestimmten Reihenfolge genau dort freisetzt, wo sie am dringendsten gebraucht werden?
Ein kleines Depot mit großen Ambitionen
Die Forschenden entwickelten eine Plattform, die sie Programmable Local Immunochemotherapy bzw. PLICT nennen. Stellen Sie sich ein weiches, injizierbares Kügelchen vor, das neben einem Brusttumor sitzt und die Behandlung über Wochen hinweg langsam abgibt. Das Kügelchen kombiniert ein wasserliebendes Gel, das schnell einen Immunstimulans und ein Chemotherapeutikum (Gemcitabin) freisetzt, mit mikroskopischen Kunststoffkugeln, die langsam ein zweites Medikament (Paclitaxel) abgeben. Der Immunstimulans, ein kurzes DNA-Stück namens CpG, soll die lokalen Immunzellen wecken, während die kombinierten Chemotherapien Tumorzellen direkt angreifen und die Tumorumgebung so umgestalten, dass Immunzellen eindringen und ihre Arbeit verrichten können.
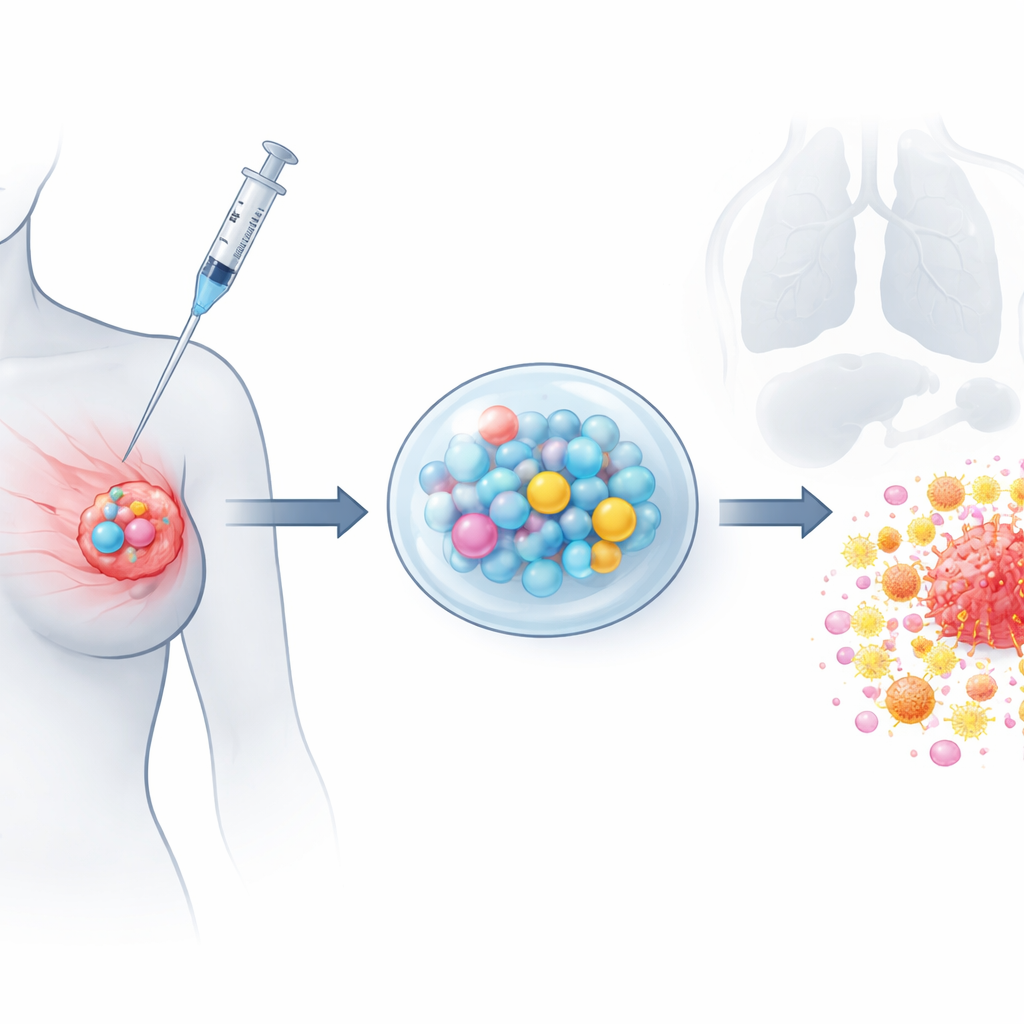
Konstruktion eines zeitgesteuerten Krebsangriffs
Um dieses System zu bauen, nutzte das Team ein Hochspannungs-„Electrospray“-Verfahren, um gleichmäßige, paclitaxel-beladene Mikrosphären aus einem biologisch abbaubaren Polymer zu formen. Bildgebende Verfahren zeigten glatte, kugelförmige Partikel von etwa einem Zehntel der Breite eines menschlichen Haares, und Labortests bestätigten, dass Paclitaxel über mindestens einen Monat gleichmäßig auslief, ohne einen frühen Ausstoß. Separat wurden Gemcitabin und CpG in ein temperaturempfindliches Gel eingebettet, das beim Kühlen flüssig ist und bei Körpertemperatur halbfest wird. Chemische Analysen bestätigten, dass beide Wirkstoffe in ihren Trägern intakt blieben. Kombiniert liefert das Gel eine schnelle, frühe Dosis von Gemcitabin und CpG, während die Mikrosphären einen anhaltenden Tropf von Paclitaxel abgeben und so die Vorteile einer langfristigen Niedrigdosis-Chemotherapie aus einer einzigen lokalen Applikation nachahmen.
Erprobung der lokalen Strategie an Mäusen
Das Team testete PLICT anschließend in einem Mausmodell des dreifach-negativen Brustkrebses. Die Mäuse entwickelten zunächst kleine Brusttumoren und erhielten dann entweder Standardinjektionen von Paclitaxel allein, Paclitaxel plus Gemcitabin oder ein einziges lokales PLICT-Implantat in Tumornähe. Über vier Wochen wuchsen die Tumoren in der Kontrollgruppe schnell, bei Standardchemotherapie wuchs das Tumorwachstum langsamer, doch die mit PLICT behandelten Tumoren waren sowohl in Größe als auch Gewicht deutlich kleiner. Bildgebende Untersuchungen des ganzen Tiers und entnommener Organe zeigten, dass PLICT auch die Ausbreitung des Krebses in entfernte Organe, insbesondere die Lungen, wirksamer verringerte als herkömmliche Medikamenteninjektionen. Messungen der Wirkstoffkonzentrationen erklärten dies: Paclitaxel war in PLICT-behandelten Tumoren hoch konzentriert, aber in entferntem Fettgewebe gering und im Blut ähnlich wie bei anderen Gruppen, was auf eine starke lokale Bindung mit weniger unerwünschter Belastung außerhalb des Zielgebiets hindeutet.
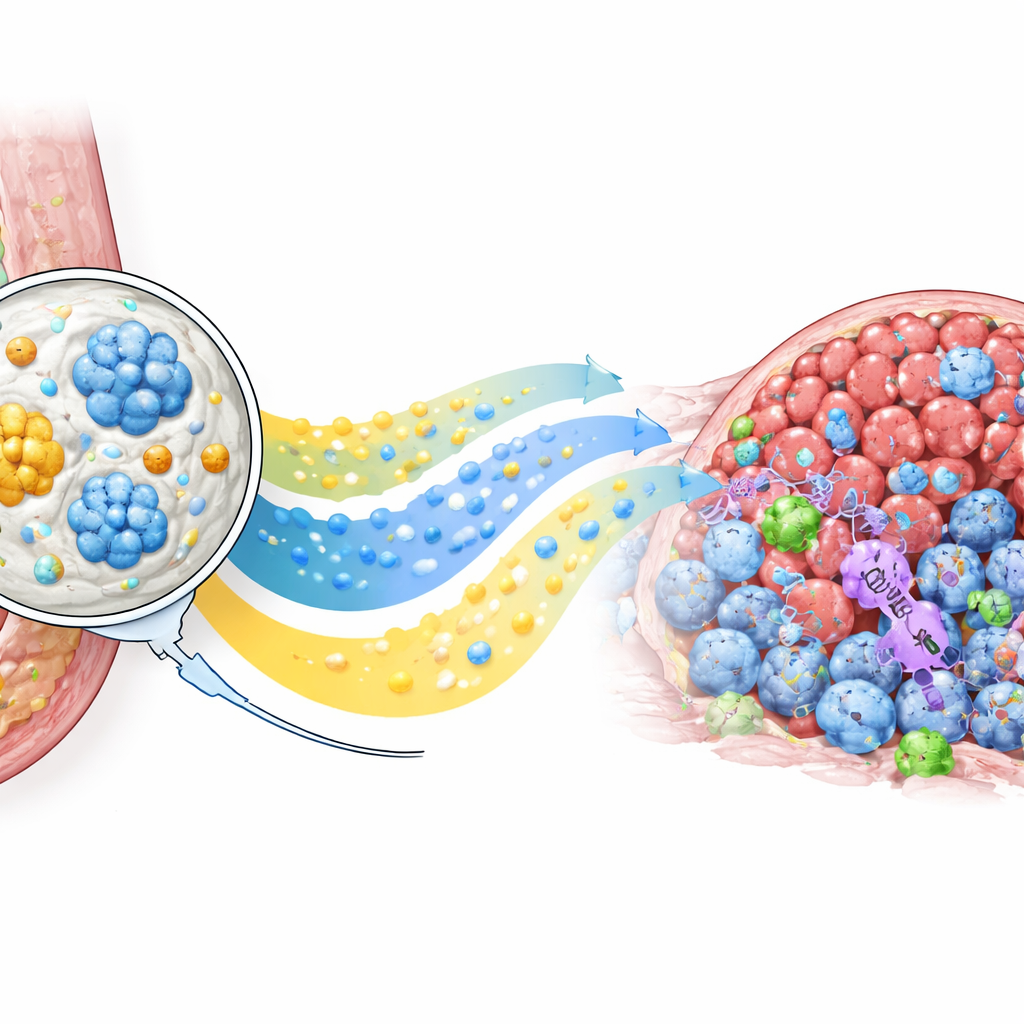
Die körpereigenen Verteidiger rekrutieren
Über die Tumorverkleinerung hinaus veränderte PLICT die Immunlandschaft darin. Detaillierte Zellanalysen zeigten einen starken Anstieg an krebsabtötenden CD8-T-Zellen in PLICT-behandelten Tumoren im Vergleich zu allen anderen Gruppen sowie einen Rückgang bestimmter regulatorischer T-Zellen, die normalerweise Immunangriffe dämpfen. Gewebeanfärbungen für CD69, einen Marker kürzlich aktivierter T-Zellen, bestätigten, dass viele dieser einwandernden Zellen aktiviert und einsatzbereit waren. Gleichzeitig verursachte die Standardchemotherapie deutliche Schädigungen des Lebergewebes, während die Organe der PLICT-behandelten Mäuse unter dem Mikroskop nahezu normal aussahen. Zusammengenommen deuten diese Befunde darauf hin, dass das lokale Depot nicht nur die direkte Wirkstoffbelastung im Tumor erhöht, sondern auch eine günstigere, weniger unterdrückte Immunantwort auslöst, ohne zusätzliche Belastung für lebenswichtige Organe zu verursachen.
Was das für die zukünftige Krebsbehandlung bedeuten könnte
Für Nichtfachleute ist die Botschaft klar: Indem Chemotherapie und Immunstimulation in einen langsamen, präzise abgestuften Tropf verwandelt werden, der direkt neben dem Tumor verabreicht wird, erzielte dieser Ansatz in Tierversuchen stärkere Tumorkontrolle und weniger systemische Nebenwirkungen als Standardmedikamenteninjektionen. Die Arbeit befindet sich noch im präklinischen Stadium, und Fragen bleiben, wie gut ein solches System beim Menschen oder in anderen Behandlungsszenarien funktionieren würde. Doch das Konzept eines injizierbaren, programmierbaren „Medikamentendepots“, das mehrere Wirkstoffe nacheinander freisetzt, könnte neue Wege eröffnen, aggressive Tumore wie dreifach-negativen Brustkrebs gezielter zu behandeln — den Kampf dort zu konzentrieren, wo er am wichtigsten ist, und den Rest des Körpers zu schonen.
Zitation: Hsieh, CH., Hsu, MY., Lin, CF. et al. Programmable local immunochemotherapy for triple-negative breast cancer via spatiotemporally controlled release of CpG oligodeoxynucleotides, gemcitabine, and paclitaxel. npj Breast Cancer 12, 45 (2026). https://doi.org/10.1038/s41523-026-00910-7
Schlüsselwörter: dreifach-negativer Brustkrebs, lokale Arzneimittelabgabe, Immuntherapie, kontrollierte Freisetzung, Hydrogel-Mikrosphären