Clear Sky Science · de
Die Expression von Zielgenen des Östrogenrezeptors β enthüllt neuartige repressive Funktionen beim aggressiven Mammakarzinom
Warum diese Forschung wichtig ist
Inflammatorisches Mammakarzinom zählt zu den aggressivsten und tödlichsten Formen von Brustkrebs: Es breitet sich häufig schnell aus und bietet Betroffenen wenige gezielte Behandlungsoptionen. Diese Studie untersucht einen weniger bekannten Hormon-Sensor in Brustzellen, den Östrogenrezeptor Beta, und zeigt, wie er als natürlicher Bremsmechanismus gegen Tumorstreuung wirken kann. Das Verständnis dieser eingebauten Bremse könnte den Weg für neue Wirkstoffe öffnen, die Metastasen verlangsamen oder verhindern — gerade für Patientinnen, die bisher nur sehr eingeschränkte Möglichkeiten haben.
Eine andere Seite des inflammatorischen Mammakarzinoms
Im Gegensatz zu vielen Brusttumoren, die vom klassischen Östrogenrezeptor Alpha abhängig sind, fehlt dieser Rezeptor beim inflammatorischen Mammakarzinom häufig, weshalb Standard-Hormontherapien wenig wirksam sind. Die Autorinnen und Autoren richten den Fokus stattdessen auf den zweiten Östrogenrezeptor, Östrogenrezeptor Beta (ERβ), den sie bereits zuvor mit geringerer Metastasenhäufigkeit bei Patientinnen und Mausmodellen in Verbindung gebracht hatten. Frühere Arbeiten deuteten darauf hin, dass ERβ die zelluläre Gerüst- und Bewegungsmaschinerie verlangsamt. In dieser Studie wollten die Forschenden genomweit kartieren, wie ERβ die Genaktivität verändert und welche nachgeschalteten Moleküle seine schützende, anti-metastatische Wirkung vermitteln könnten.
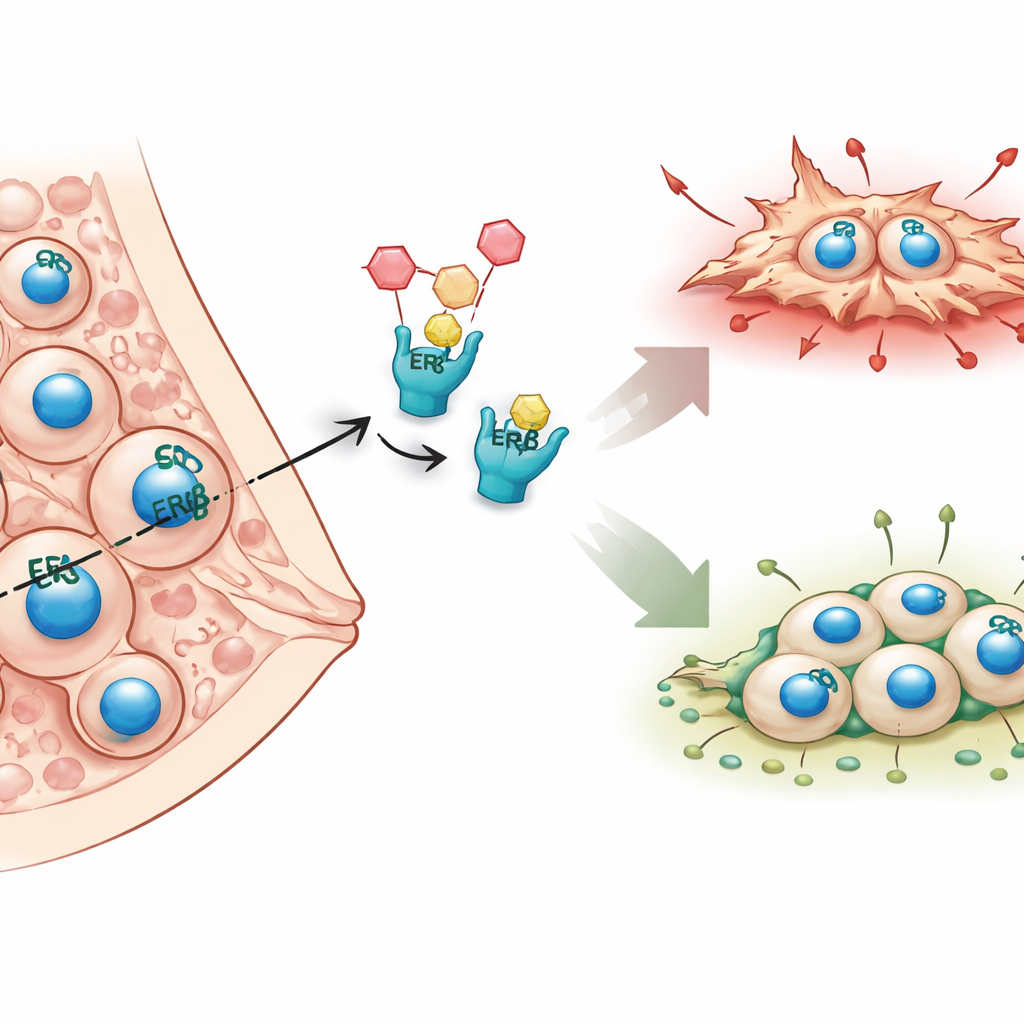
Das Bedienungsbuch der Krebszelle lesen
Um den Einfluss von ERβ aufzudecken, setzten die Forschenden zwei leistungsfähige Sequenzieransätze in inflammatorischen Brustkrebszelllinien ein. Eine Methode, ChIP-seq, zeigt genau, wo ERβ an die DNA bindet — wie das Setzen von Markierungen auf bestimmte Seiten und Zeilen im Bedienungsbuch der Zelle. Die andere Methode, RNA-seq, misst, welche Gene hoch- oder runterreguliert werden, wenn ERβ vorhanden, entfernt oder durch ein selektives Mittel aktiviert ist. Beim Vergleich dieser Datensätze fanden sie Tausende von DNA-Stellen, an denen ERβ bindet; die meisten davon liegen nicht nur an klassischen Gen-Schaltern, sondern tief innerhalb oder zwischen Genen, was auf eine breit angelegte Steuerung hindeutet. Außerdem entdeckten sie, dass ERβ häufig mit Familien anderer Transkriptionsfaktoren zusammenwirkt und Komplexe bildet, die gemeinsam entscheiden, welche Gene gedämpft oder aktiviert werden.
Umlenkung von Wachstum, Bewegung und Stoffwechsel
Die integrierte Analyse zeigte, dass ERβ tendenziell Gene dämpft, die Bewegung, Formveränderung und Invasion der Zelle fördern — insbesondere solche, die mit dem Aktin-Zytoskelett und der Rho-GTPase-Signalgebung zusammenhängen, also Signalwegen, die für Metastasenbildung bekannt sind. Gleichzeitig unterstützt ERβ Genprogramme, die mit Gewebeentwicklung und Zell-Differenzierung verknüpft sind und die Krebszellen in einen sesshafteren, weniger aggressiven Zustand drängen. Die Studie offenbarte zudem eine überraschende Rolle von ERβ bei der Anpassung von Stoffwechselwegen, speziell solchen, die Fettsäuren und Phospholipide betreffen — zentrale Treibstoffe und Bausteine für schnell wachsende Tumoren. Wichtig ist, dass diese Effekte nicht nur in Zellen beobachtet wurden, die künstlich hohe ERβ-Spiegel aufweisen, sondern auch in Zellen mit natürlichen Rezeptorleveln, was die Relevanz für reale Tumoren unterstreicht.
Kleine RNA-Boten und klinische Bedeutung
Über proteinkodierende Gene hinaus analysierte das Team MicroRNAs — winzige RNA-Moleküle, die die Genexpression feinjustieren. Sie fanden Dutzende MicroRNAs, deren Spiegel sich veränderten, wenn ERβ entfernt oder wiederhergestellt wurde; viele hiervon stehen in Verbindung mit Tumorsuppressorwirkung beim Brustkrebs. Durch das Verknüpfen dieser MicroRNAs mit ihren Zielgenen zeigten die Autorinnen und Autoren, dass ERβ einige Krebs-Treiber indirekt über ein geschichtetes Regulationsnetz kontrolliert. Anschließend werteten sie Patientendaten aus und untersuchten Tumoren von Personen mit inflammatorischem und nicht-inflammatorischem Brustkrebs. Mehrere ERβ-regulierte Gene standen in starkem Zusammenhang mit dem Überleben: Hohe Spiegel mancher Gene (wie SERPINA1 und HSPB8) sagten bessere Ergebnisse voraus, während hohe Spiegel anderer (wie PITX1 und HOMER3) mit schlechterem Überleben verknüpft waren. Damit rücken diese nachgeschalteten Moleküle als potenzielle Prognosemarker und zukünftige Wirkstoffziele in den Fokus.
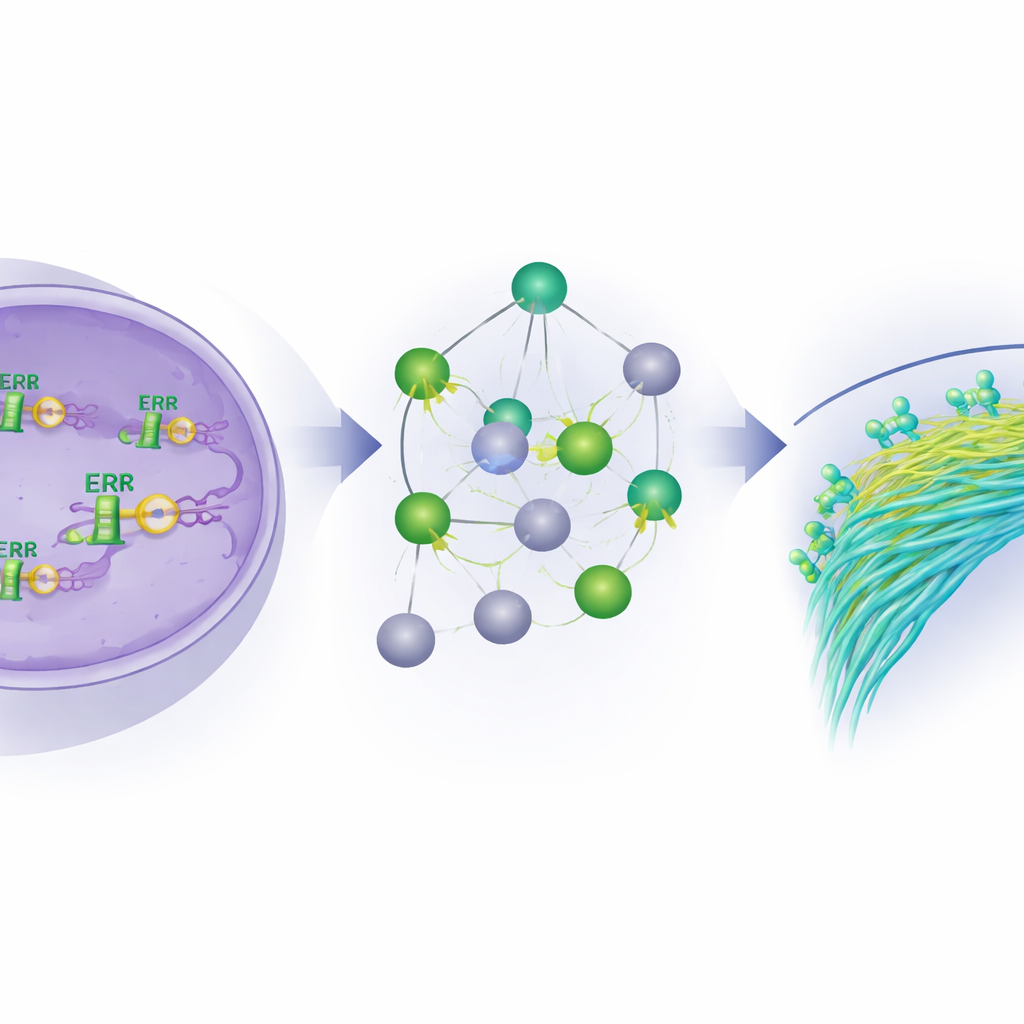
Von der molekularen Bremse zu künftigen Therapien
Insgesamt zeichnet die Studie ERβ als zentrale Bremse für das invasive Verhalten inflammatorischer Brustkrebszellen. Durch DNA-Bindung, Kooperation mit anderen Regulatoren sowie die Gestaltung sowohl von Gen- als auch MicroRNA-Netzen dämpft ERβ Programme, die Zellmigration und Metastasen antreiben, fördert gleichzeitig stabilere, differenziertere Zustände und verändert den Krebsstoffwechsel. Für Patientinnen bedeutet das, dass Wirkstoffe, die ERβ aktivieren oder seine wichtigen nachgeschalteten Ziele hemmen — besonders solche, die an Zellbewegung und Fettsäurenutzung beteiligt sind — die Grundlage neuer, präziserer Therapien gegen diese schwer behandelbare Erkrankung bilden könnten.
Zitation: Tastsoglou, S., Karagounis, I.V., Miliotis, M. et al. Estrogen receptor β target gene expression reveals novel repressive functions in aggressive breast cancer. npj Breast Cancer 12, 38 (2026). https://doi.org/10.1038/s41523-026-00905-4
Schlüsselwörter: inflammatorisches Mammakarzinom, Östrogenrezeptor Beta, Metastase, Genregulation, Krebsstoffwechsel