Clear Sky Science · de
Die CXCL10/CXCR3‑Achse ist essenziell für die Aufrechterhaltung immunologischer Dormanz beim triple-negativen Mammakarzinom
Warum manche Krebszellen schlafen, statt sich auszubreiten
Mammakarzinome können sich manchmal wie Schläferagenten verhalten. Nach der Erstbehandlung verstecken sich einige Krebszellen über Jahre im Körper, wachsen nicht genug, um in Bildgebungen sichtbar zu sein — sind aber dennoch fähig, später aufzuwachen und lebensbedrohliche Metastasen zu verursachen. Dieser Artikel untersucht, warum dieser „Schlaf“-Zustand, genannt Dormanz, bei einer besonders aggressiven Form der Erkrankung, dem triple‑negativen Mammakarzinom, auftritt, und identifiziert ein chemisches Signal, das dem Immunsystem hilft, diese Zellen in Schach zu halten.
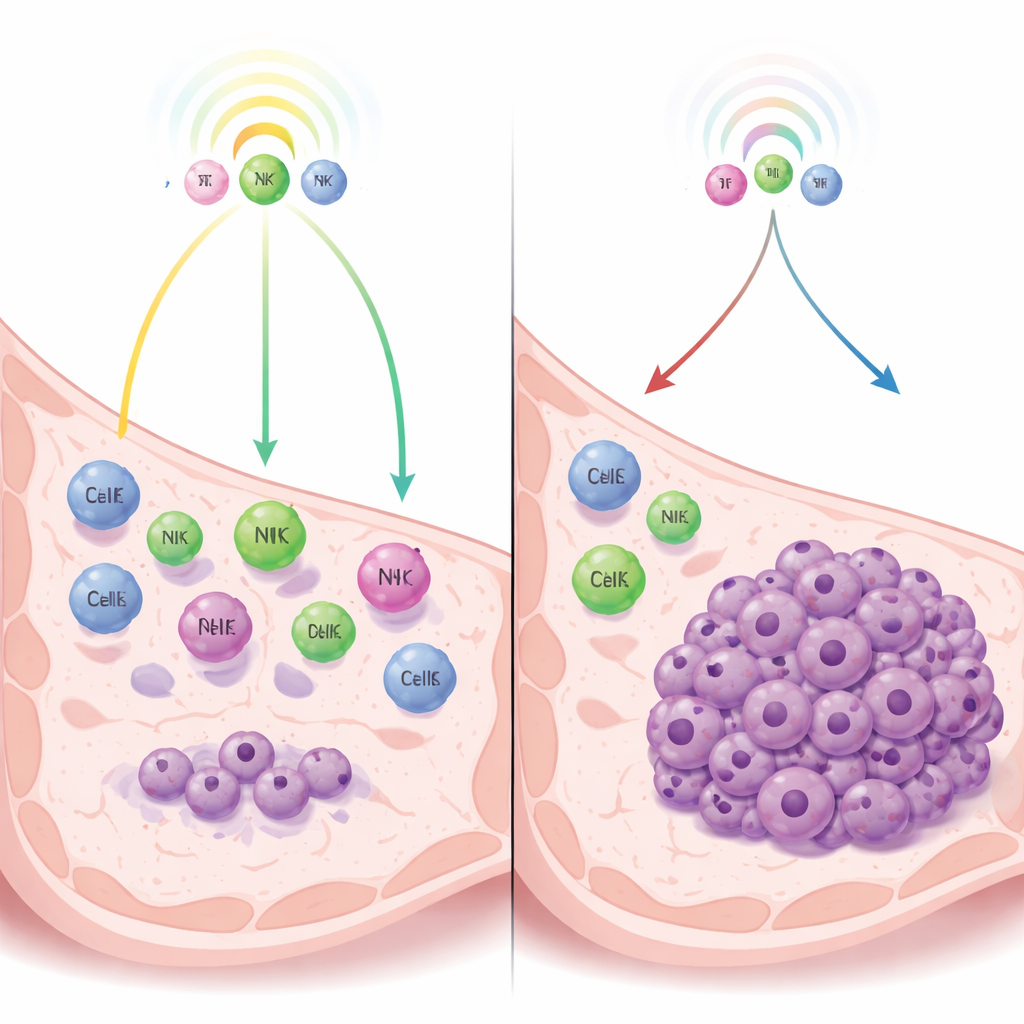
Zerren zwischen Krebs und Immunsystem
Die Autoren konzentrieren sich auf eine Form der Dormanz, die nicht durch fehlende Blutversorgung oder interne Zellbremsen gesteuert wird, sondern durch Immunüberwachung — die ständige Wachsamkeit von Immunzellen, die Tumoren in Schach halten können, ohne sie vollständig zu eliminieren. An Mausmodellen des triple‑negativen Mammakarzinoms vergleichen sie Tumorzellen, die von Natur aus dormant bleiben, mit eng verwandten Zellen, die schnell wachsende Tumore bilden. Durch die Untersuchung aktivierter Gene stellen sie fest, dass dormant bleibende Zellen Interferon‑Signalwege stark hochfahren — Immunalarm‑Systeme, die die Freisetzung chemischer Botenstoffe anregen, welche Immunzellen in den Tumorbereich locken.
Ein Schlüsselbotenstoff, der Tumore ruhig hält
Unter den zahlreichen Molekülen, die in dormanten Zellen hochreguliert sind, sticht eines besonders hervor: CXCL10, ein kleines Protein, das als Leuchtsignal für Immunzellen wirkt, die seinen Partnerrezeptor CXCR3 tragen. Dormante Krebszellen produzieren deutlich mehr CXCL10 als ihre aggressiven Gegenstücke. Schalten die Forschenden CXCL10 gezielt in dormanten Zellen aus und implantieren diese in immunkompetente Mäuse, bilden die zuvor ruhenden Zellen rasch Tumore. Das Blockieren des CXCR3‑Rezeptors mit einem Antikörper zeigt einen ähnlichen Effekt. In beiden Fällen entkommen die Krebszellen dem immunologischen Patt und beginnen zu wachsen, was zeigt, dass die CXCL10/CXCR3‑Achse nicht nur mit Dormanz korreliert, sondern für deren Aufrechterhaltung erforderlich ist.
Wie Veränderungen in der lokalen Umgebung das Gleichgewicht kippen
Die Reduktion von CXCL10 bewirkt mehr als die Veränderung eines einzelnen Signalwegs; sie formt die gesamte lokale Immunlandschaft um. In Tumoren, die CXCL10 verloren haben, sind hilfreiche CD4‑ und CD8‑T‑Zellen vermindert, während bestimmte myeloide Zellen, die Immunreaktionen unterdrücken können, vermehrt auftreten. Auch natürliche Killerzellen und dendritische Zellen ändern in ihrer Häufigkeit. Dieses Muster zeigt sich sowohl in Primärtumoren als auch in der Lunge, wohin Krebszellen wandern und sich verstecken können. Selbst wenn Lungenmetastasen zu klein sind, um sie mikroskopisch zu erkennen, zeigen molekulare Marker, dass mehr Krebszellen die Lunge besiedeln, wenn CXCL10 fehlt, und weniger T‑Zellen in diese Gewebe eindringen. In Mäusen ohne funktionierendes Immunsystem macht das Entfernen von CXCL10 hingegen keinen Unterschied — dormant bleibende Zellen wachsen unabhängig weiter — was unterstreicht, dass dieses Signal über Immunkontrolle wirkt und nicht als direkte Wachstumsbremse auf Krebszellen dient.
Warum mehr Signal hilfreich, aber kein Zauberschalter ist
Das Team prüft auch die Gegenfrage: Kann eine Verstärkung von CXCL10 einen aggressiven Tumor in einen dormant‑zustand überführen? Wenn sie schnell wachsende Krebszellen so verändern, dass sie zusätzliches CXCL10 produzieren, wachsen die Tumore langsamer und treten später auf, und bestimmte Immunzelltypen im Blut nehmen zu. Eine vollständige Dormanz entsteht jedoch nicht; letztlich bilden alle Mäuse dennoch Tumore. Das deutet darauf hin, dass CXCL10 zwar für die Aufrechterhaltung von Dormanz notwendig ist, sofern die übrige Immunmaschinerie intakt ist, es aber allein nicht ausreicht, um diesen komplexen Zustand aus dem Nichts zu erzeugen. Weitere Signalwege müssen zusammenwirken, um ein langfristiges Gleichgewicht zwischen Immunangriff und Überleben der Krebszellen zu ermöglichen.
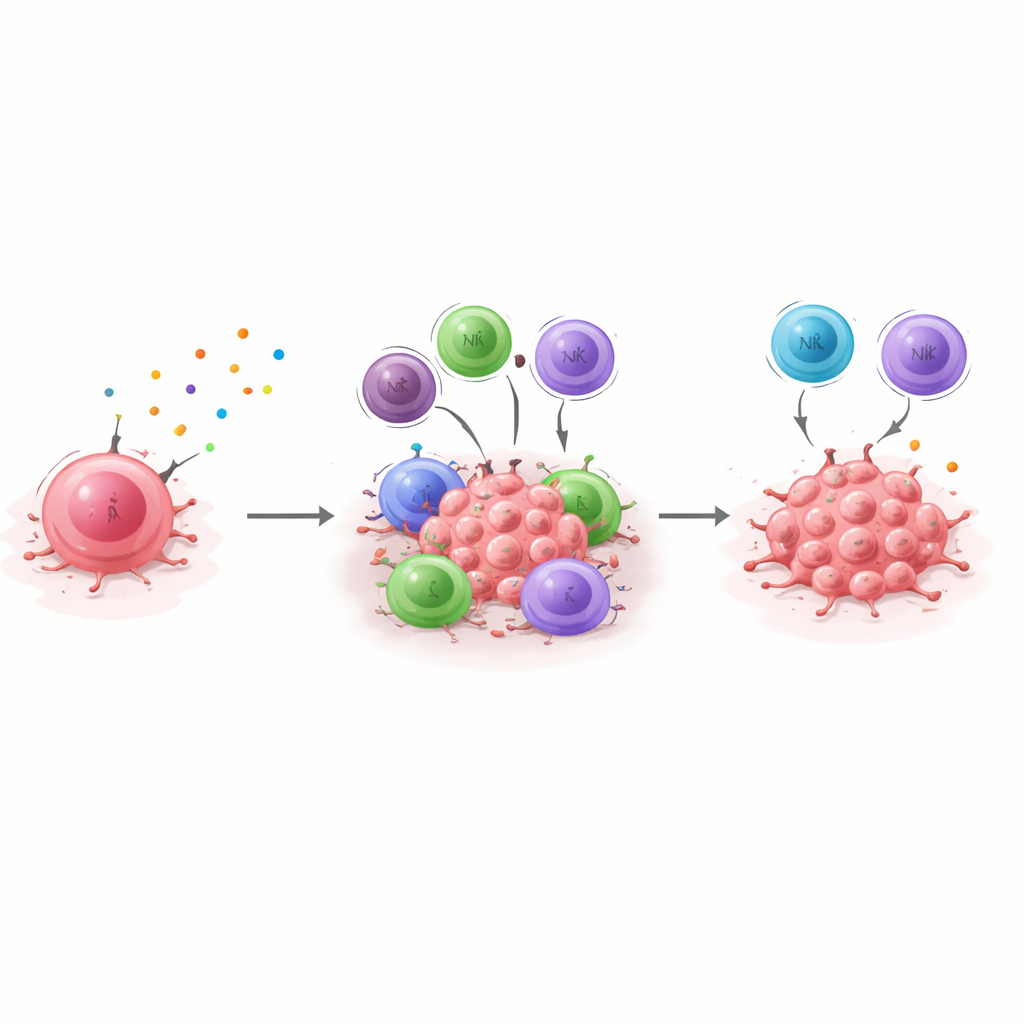
Von Mausversuchen zur Patientenprognose
Um ihre Ergebnisse auf den Menschen zu übertragen, leiten die Forschenden eine „Dormanz‑Signatur“ ab — ein Set von Genen, das in dormanten Zellen konstant höher exprimiert ist und bei Abschaltung von CXCL10 abfällt. Anschließend analysieren sie große Datensätze von Brustkrebs‑Patientinnen und prüfen, wie diese Signatur mit dem Überleben zusammenhängt. Beim triple‑negativen Mammakarzinom leben Patientinnen, deren Tumoren diese Dormanz‑Signatur stärker exprimieren, insgesamt länger und bleiben tendenziell länger rezidivfrei, was mit einem durch das Immunsystem kontrollierten dormant‑Zustand übereinstimmt, der Rezidive hinauszögert. Dieser Effekt zeigt sich nicht in gleicher Weise bei hormonpositiven Tumoren, was die biologischen Unterschiede zwischen Brustkrebs‑Subtypen hervorhebt. Insgesamt deuten die Ergebnisse darauf hin, dass die CXCL10/CXCR3‑Achse eine zentrale Säule der immunvermittelten Dormanz beim triple‑negativen Mammakarzinom ist und dass die Messung dieser Dormanz‑Signatur helfen könnte, Patientinnen zu identifizieren, die eher von Therapien profitieren, die die Immun‑Kontrolle stärken — oder umgekehrt solche, die aufgrund unzureichender Kontrolle eine engmaschigere Langzeitüberwachung benötigen.
Zitation: Yilmaz, A., Haerri, L., Granda, M.E. et al. The CXCL10/CXCR3 axis is essential for sustaining immunological dormancy in triple-negative breast cancer. npj Breast Cancer 12, 36 (2026). https://doi.org/10.1038/s41523-026-00903-6
Schlüsselwörter: triple-negatives Mammakarzinom, Tumor‑Dormanz, Immunüberwachung, Chemokin‑Signalgebung, CXCL10 CXCR3‑Achse