Clear Sky Science · de
Räumliche Genexpressionsanalyse enthüllt Treiber extrem früher Lymphknotenmetastasierung bei Brustkrebs
Warum winzige reisende Krebszellen wichtig sind
Wenn Brustkrebs sich außerhalb der Brust ausbreitet, bleibt er häufig zuerst in benachbarten Lymphknoten hängen — kleinen Filtern, die bei der Bekämpfung von Infektionen helfen. Ärztinnen und Ärzte wissen, dass das Auffinden von Krebs in diesen Knoten meist auf ein höheres Rückfallrisiko hindeutet. Was in den allerersten Momenten passiert, wenn nur eine Handvoll Zellen in einem Lymphknoten ankommt, war bei echten Patientinnen und Patienten jedoch nahezu nicht sichtbar. In dieser Studie nutzte man eine neue Art mikroskopischer „Karte“ der Genaktivität, um diese frühesten Schritte in beispielloser Detailtiefe zu beobachten und zu zeigen, welche Zellen erfolgreich sind, welche scheitern und warum das die Patientenprognose beeinflusst.
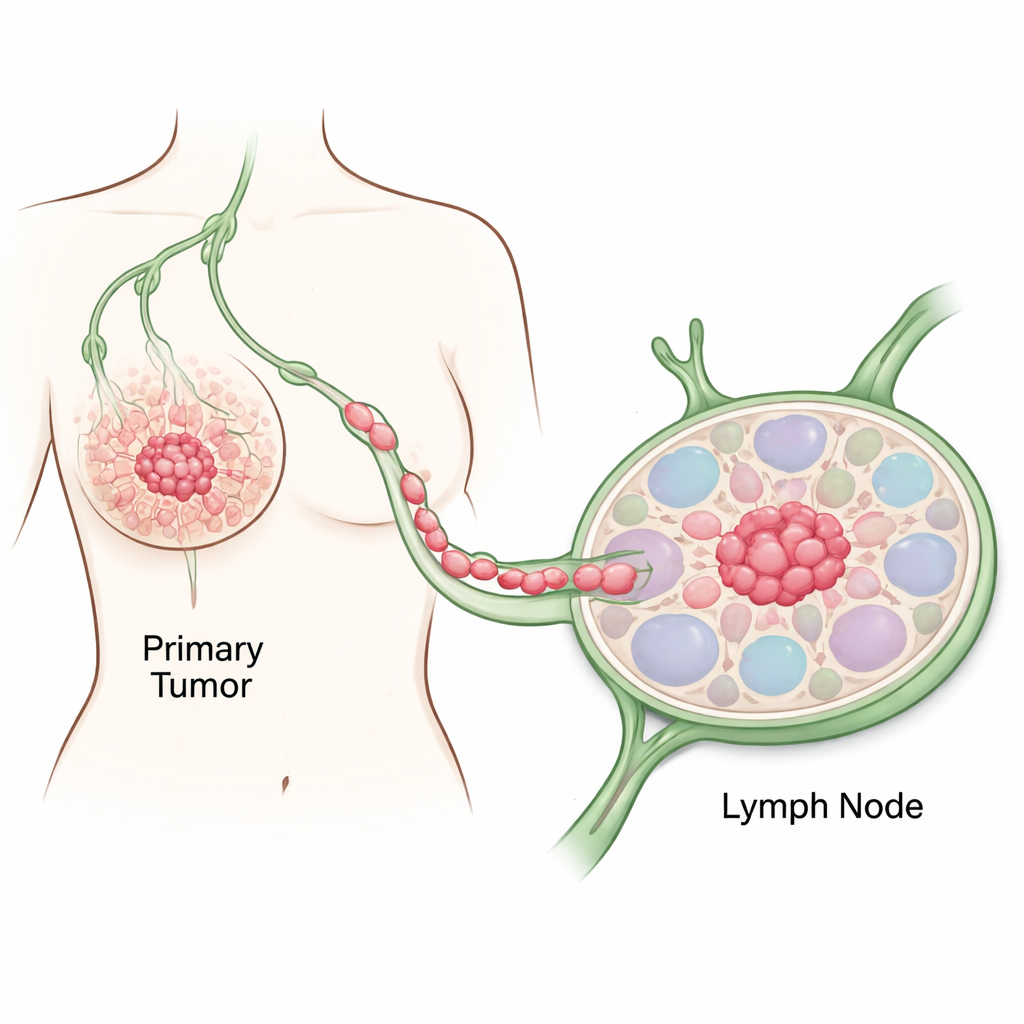
Den ersten Schritten des Krebses folgen
Die Forschenden konzentrierten sich auf Gewebe einer 80-jährigen Frau mit einem aggressiven, HER2-positiven Brustkrebs. Sie entnahmen Proben sowohl aus normal aussehenden Brustbereichen als auch aus nahe gelegenen Tumorregionen und nutzten mehrere DNA- und RNA-Tests, um nachzuvollziehen, wie normale Zellen krebsartig wurden. Im Vergleich zu gesundem Gewebe zeigten die Tumorregionen klassische Kennzeichen von Krebs: gestörte Zelladhäsion, überaktive Zellteilung, großflächige Veränderungen der DNA-Methylierung und wichtige Mutationen in Genen, die Wachstum und Genomstabilität steuern. Diese molekularen Veränderungen stimmten mit den Befunden überein, die Pathologinnen und Pathologen unter dem Mikroskop sahen, und bestätigten einen schrittweisen Übergang von normalen Brustzellen zu vollständig malignen Zellen.
Gestaltwandelnde Zellen auf dem Weg
Um zu verstehen, wie Tumorzellen beginnen, sich zu bewegen, verwendete das Team eine hochauflösende Methode, die die Genaktivität einzelner Zellen liest und gleichzeitig deren genaue Position im Gewebe erhält. Dadurch konnten sie rekonstruieren, wie Krebszellen ihre Identität veränderten, als sie normale Bruststrukturen verließen und sich der Metastasierung näherten. Sie fanden heraus, dass der Krebs offenbar von einem bestimmten Typ ausgereifter Brustzellen ausging, der dann allmählich Merkmale eines Prozesses annahm, der epithelial-mesenchymale Transition (EMT) genannt wird — eine Art Gestaltwandel, der Zellen hilft, sich zu lösen, zu bewegen und in angrenzendes Gewebe einzudringen. Statt eines einfachen Ein/Aus-Schalters befanden sich die Zellen auf einem Kontinuum gemischter Zustände, die „epitheliale“ Eigenschaften (geordnet, zusammenhaftend) mit „mesenchymalen“ Eigenschaften (beweglich, invasiv) kombinierten. Einige dieser hybriden Zellen verstreuten sich durch den Tumor, andere bildeten Cluster fortgeschrittenerer Krebsgruppen, die darauf vorbereitet waren, in Lymphknoten zu streuen.
Der erste entfernte Brückenkopf in einem Lymphknoten
In einem Lymphknoten, der anhand standardmäßiger klinischer Tests als metastasenfrei eingestuft worden war, entdeckten die Wissenschaftlerinnen und Wissenschaftler etwas Bemerkenswertes: nur 30 vereinzelte Tumorzellen, die eine Region von nur etwa 200 Mikrometern Breite belegten — grob das Doppelte der Dicke eines menschlichen Haares. Diese isolierten Tumorzellen stammten aus mehreren verschiedenen Hybridzuständen, jeder mit eigenem Genaktivitätsmuster. Durch die Gruppierung verwandter Krebszellen definierte das Team sechs Subtypen mit unterschiedlichen Rollen. Ein Subtyp, stark „mesenchymal“, schien besonders gut darin, Zelltod zu widerstehen und Angriffen des Immunsystems zu entkommen. Ein anderer Subtyp, der wieder mehr epitheliale Merkmale annahm, zeigte eine auffällige Umstellung seines Energiestoffwechsels hin zu Fettsäuremetabolismus. Nur diese metabolisch umgeschaltete, stärker epithelial geprägte Gruppe bildete erfolgreich kleine Kolonien in Lymphknoten, was darauf hindeutet, dass die Wahl der Energiequelle — nicht nur Invasivität — mitbestimmt, ob frühe Ankömmlinge Fuß fassen können.
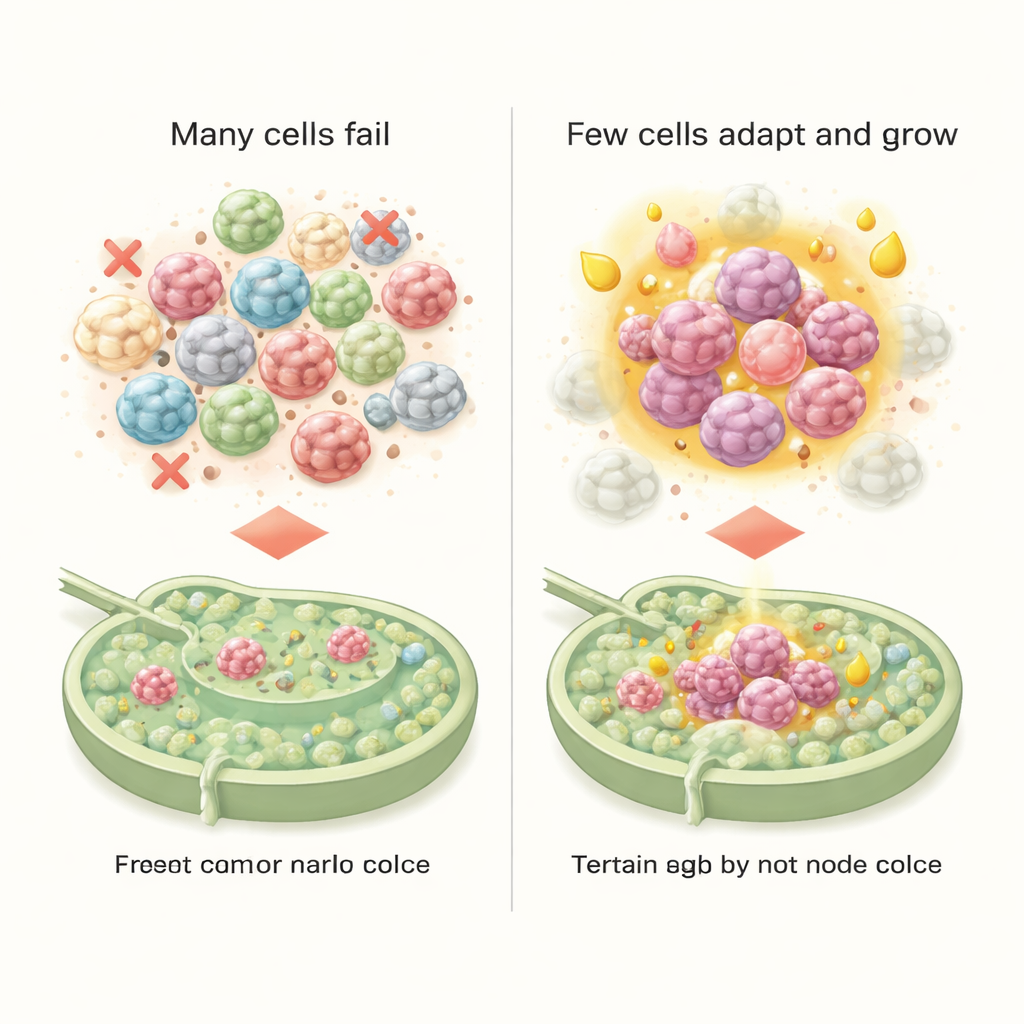
Ein Lymphknoten, der dem Krebs stillschweigend hilft
Die Studie untersuchte auch, wie die Lymphknotenumgebung auf diese Eindringlinge reagierte. Noch bevor eine sichtbare Metastase entstanden war, sendeten Immunzellen, Endothelzellen der Blutgefäße und Bindegewebszellen bereits Signale, die Immunreaktionen dämpften und das Tumorüberleben unterstützten. Bestimmte Rezeptor–Ligand-Paare zwischen Immunzellen deuteten auf frühe Immuntoleranz hin, während andere neues Blutgefäßwachstum förderten und das Gewebegerüst umgestalteten. Zusammen schufen diese Veränderungen eine Nische, die für die metabolisch angepassten Krebszellen überraschend einladend war und ihnen half, zu überleben, zu wachsen und möglicherweise weitere Ausbreitung zu begründen.
Was das für Patientinnen und Patienten bedeutet
Indem sie ihre Ergebnisse mit großen, bereits vorhandenen Patientendatensätzen verglichen, machten die Forschenden eine kontraintuitive Entdeckung. Die Zellen, die am besten frühe Lymphknotenkolonien bildeten, und selbst solche mit den stärksten mesenchymalen Merkmalen, entsprachen nicht den schlechtesten klinischen Verläufen. Stattdessen hatten Patientinnen und Patienten die schlechteste Prognose, wenn ihre Tumoren bestimmte aggressive Hybridzelltypen enthielten, die durch hohe Zellzyklusaktivität und zuckerverwertende (Glykolyse-)Programme gekennzeichnet waren, angetrieben von Genen wie MYC. Mit anderen Worten scheinen sich verschiedene gestaltgeänderte Zellzustände zu spezialisieren: Einige sind darauf spezialisiert, still und heimlich neue Standorte zu kolonisieren, andere treiben rasanteres Wachstum und Rückfälle voran. Das Verständnis und die gezielte Bekämpfung dieser unterschiedlichen Zellzustände und ihrer metabolischen Vorlieben könnten zu präziseren Therapien führen — solchen, die nicht nur das früheste Ausbreiten zuverlässiger erkennen, sondern auch die Tumorzelltypen ausschalten, die am ehesten tödliche Rückfälle verursachen.
Zitation: Nagasawa, S., Kajiya, K., Ishikawa, E. et al. Spatial gene expression analysis reveals drivers of extremely early lymph node metastasis in breast cancer. npj Breast Cancer 12, 28 (2026). https://doi.org/10.1038/s41523-026-00897-1
Schlüsselwörter: Brustkrebsmetastasen, Lymphknoten, epithelial-mesenchymale Transition, räumliche Transkriptomik, Krebsstoffwechsel