Clear Sky Science · de
Normalgewebe der Brust (NBT)-Klassifikatoren: Fortschritte bei der Kompartimentklassifikation in der normalen Brusthistologie
Auf der Suche nach frühen Hinweisen im „normalen“ Brustgewebe
Brustkrebs-Screenings konzentrieren sich meist auf Tumoren oder verdächtige Knoten, doch wichtige Warnsignale können lange vor der Tumorbildung verborgen liegen. Diese Studie stellt eine einfache Frage mit großen Konsequenzen: Kann künstliche Intelligenz (KI) erlernen, wie wirklich gesundes Brustgewebe aussieht, sodass selbst kleinste frühe Veränderungen deutlicher hervorstechen? Indem Computer die Hauptbestandteile des normalen Brustgewebes erkennen lernen, wollen die Forscher eine robustere Referenzkarte schaffen, um die allerersten Schritte in Richtung Krebs besser zu erkennen.
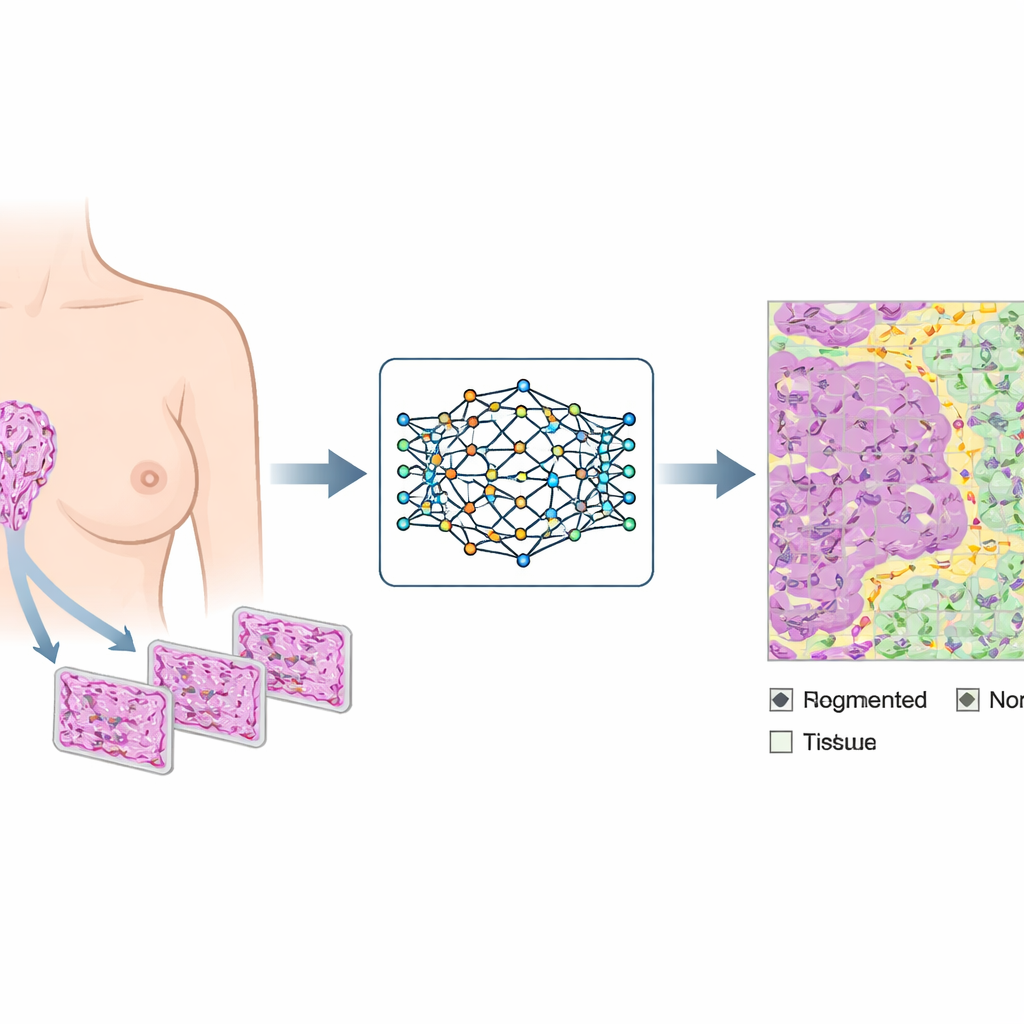
Warum normales Brustgewebe wichtig ist
Ein Großteil der Brustkrebsforschung konzentriert sich auf erkranktes Gewebe, dabei entsteht Krebs in Gewebe, das unter dem Mikroskop normal aussieht. In der Brust liegen milchproduzierende Strukturen und ihr umgebendes Stützgewebe im Gefüge aus faserigen Arealen und Fett. Feine Verschiebungen in diesen Regionen, besonders um Lobuli (die kleinen Bläschen, in denen Milch gebildet wird) und das umliegende Stroma (das stützende Bindegewebe), können ein erhöhtes Krebsrisiko ankündigen. Das ist besonders relevant für Frauen mit erblichen BRCA1- oder BRCA2-Mutationen oder für solche, die sich einer risikomindernden Operation unterziehen. Um diese stillen Signale zu lesen, brauchen Wissenschaftler präzise, quantitative Methoden, um darzustellen, wie „normal“ bei vielen verschiedenen Frauen und in unterschiedlichen medizinischen Zentren aussieht.
Aufbau einer vielfältigen Bibliothek gesunder Präparate
Das Team sammelte 70 hochauflösende digitale Bilder von normalem Brustgewebe aus fünf Einrichtungen im Vereinigten Königreich, den Niederlanden, der Schweiz und einer öffentlichen Gewebebank. Die Proben stammten von Frauen im Alter von 16 bis 74 Jahren mit unterschiedlichen Hintergründen, darunter gesunde Freiwillige, Frauen, die eine Brustverkleinerung hatten, Personen mit erblichen Hochrisiko-Genveränderungen und Frauen mit Krebs in der gegenüberliegenden Brust. Expertinnen und Experten der Pathologie markierten auf jedem Objektträger sorgfältig drei zentrale Komponenten: Epithel (die Zellschichten, die Gänge und Lobuli auskleiden), Stroma (faseriges und Bindegewebe) und Adipozyten (Fettzellen). Diese arbeitsintensive Annotation erzeugte einen reichhaltig variierenden Referenzsatz, der reale Unterschiede in Gewebeaufbereitung, Färbung und Digitalisierung widerspiegelt.
Dem Computer beibringen, Gewebetypen zu sehen
Mithilfe dieser annotierten Bibliothek trainierten die Forschenden Deep-Learning-Modelle – die sogenannten NBT-Klassifikatoren –, die drei Gewebetypen zu erkennen, indem sie kleine Bildausschnitte der größeren Objektträger analysierten. Sie testeten verschiedene Patch-Größen und technische Einstellungen, etwa wie die Färbung standardisiert werden sollte und welche Netzwerkarchitektur am besten funktioniert, und fanden schließlich eine optimale Kombination. Bei der Bewertung an völlig separaten Sammlungen normaler Objektträger aus anderen Einrichtungen unterschieden die Modelle Epithel, Stroma und Fett mit nahezu perfekter Genauigkeit. Visuelle „Heatmaps“ zeigten, dass die KI sich auf biologisch sinnvolle Strukturen konzentrierte, wie zellreiche Bereiche, Kollagenfasern und Ränder von Fettzellen – ähnlich dem Blick humaner Pathologinnen und Pathologen.
Was normales Gewebe normal erscheinen lässt
Um zu prüfen, ob das Training ausschließlich mit gesundem Gewebe einen Vorteil bringt, verglichen die Autorinnen und Autoren ihr Modell mit einem bestehenden Werkzeug, das auf einer Mischung aus normalem, präkanzerösem und kanzerösem Material trainiert wurde. Beide konnten grobe Gewebetypen identifizieren, doch die neuen NBT-Klassifikatoren erfassten die feingliedrige Architektur des wirklich normalen Brustepithels besser. In Proben, die frühe Läsionen und Tumoren enthielten, trennte das nur auf Normalität trainierte Modell gesunde von abnormen Bereichen verlässlicher. Das deutet darauf hin, dass es eine schärfere Definition von normal gelernt hat, was helfen kann, subtile Abweichungen zu betonen, die mit frühen Krankheitsstadien einhergehen.
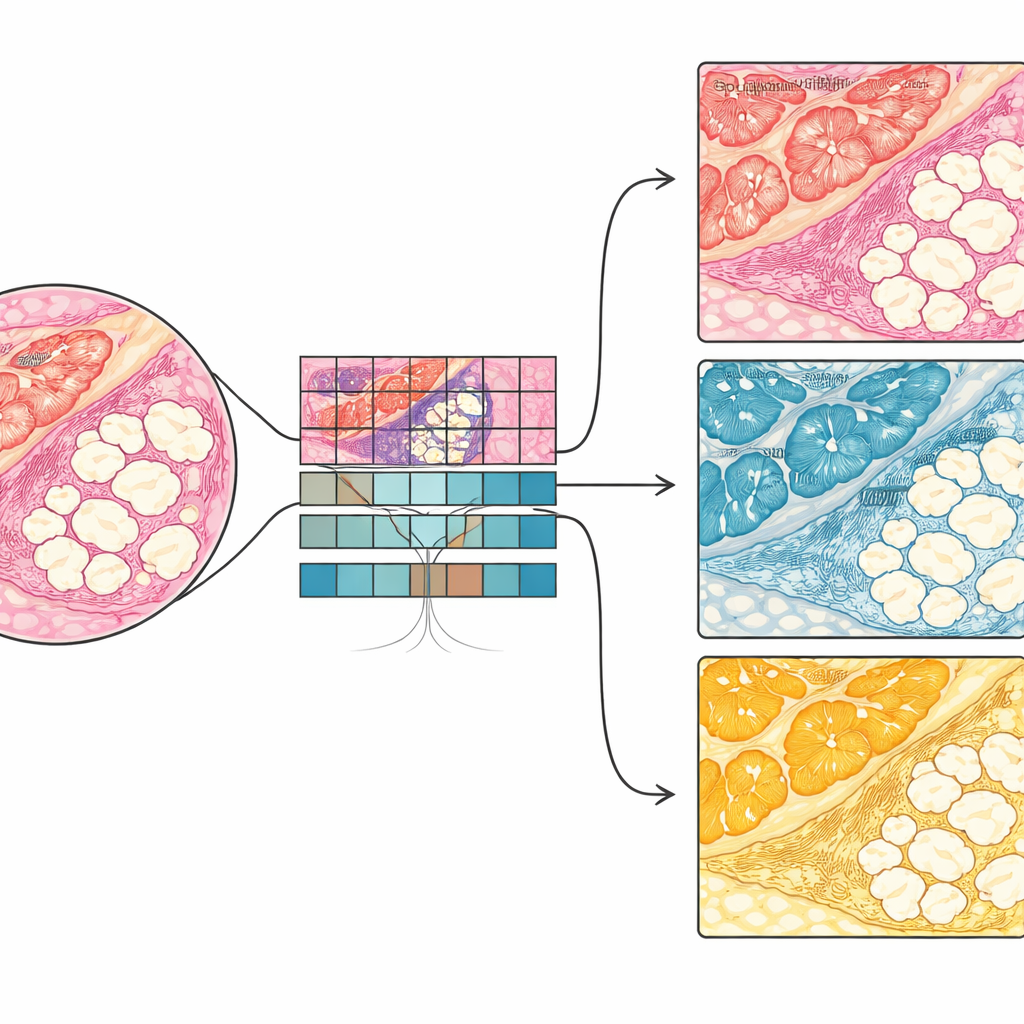
Von ganzen Objektträgern zu gezielten Regionen
Weil die Modelle auf Patch-Ebene arbeiten, lassen sie sich auf komplette digitale Objektträger anwenden und färben automatisch jede kleine Fläche als Epithel, Stroma oder Fett ein. Die Forschenden bauten eine End-to-End-Pipeline, die zunächst erkennt, wo sich Gewebe auf einem Objektträger befindet, und dann die NBT-Klassifikatoren ausführt, um detaillierte Karten der Gewebekompartimente zu erstellen. Aus diesen Karten kann das System einzelne Lobuli und ihre unmittelbare Umgebung lokalisieren, Masken für weitergehende Messungen erzeugen und ausgewählte Regionen an fortgeschrittenere Analysetools zur Weiterverarbeitung übergeben. Das erleichtert das Studium spezifischer Mikroumgebungen – etwa des Stromas direkt außerhalb von Lobuli – in denen frühe, krebsbezogene Veränderungen auftreten können, und die Kombination struktureller Merkmale mit anderen Datentypen wie räumlichen Gen- oder Proteinkarten in künftigen Arbeiten.
Was das für die Prävention von Brustkrebs bedeutet
Kurz gesagt zeigt diese Studie, dass sich KI darauf trainieren lässt, die Bausteine gesunden Brustgewebes mit bemerkenswerter Präzision und in einer für Pathologinnen und Pathologen interpretierbaren Weise zu erkennen. Indem riesige, komplexe digitale Objektträger in strukturierte Karten von epithelialen, faserigen und fetthaltigen Bereichen verwandelt werden, schaffen NBT-Klassifikatoren eine verlässliche Basis dafür, wie Normalität bei vielen Frauen und Einrichtungen aussieht. Dieses klarere Bild der Normalität könnte es erleichtern, die schwachen Spuren der Krebsentstehung früher als bisher zu entdecken, und damit zukünftige Werkzeuge unterstützen, die helfen, Frauen mit erhöhtem Risiko zu identifizieren und Präventionsstrategien zu steuern, bevor sichtbare Tumoren entstehen.
Zitation: Chen, S., Parreno-Centeno, M., Booker, G. et al. Normal breast tissue (NBT)-classifiers: advancing compartment classification in normal breast histology. npj Breast Cancer 12, 41 (2026). https://doi.org/10.1038/s41523-026-00896-2
Schlüsselwörter: normales Brustgewebe, computationale Pathologie, Deep Learning, früher Krebsnachweis, digitale Histologie