Clear Sky Science · de
CD52-Signalgebung über Makrophagen-Siglec-G stellt ein therapeutisches Ziel für die Krebsimmuntherapie dar
Warum sich einige Brustkrebse dem Immunsystem entziehen
Der triple‑negative Brustkrebs gehört zu den gefährlichsten Formen von Brustkrebs, weil er sich schnell ausbreitet und viele der üblichen Behandlungsziele fehlen. Diese Studie untersucht einen neu entdeckten Mechanismus, mit dem diese Tumoren sich der Abwehr des Körpers entziehen können, und zeigt, wie das Blockieren dieser Fluchtroute immunbasierte Therapien wirkungsvoller machen könnte.
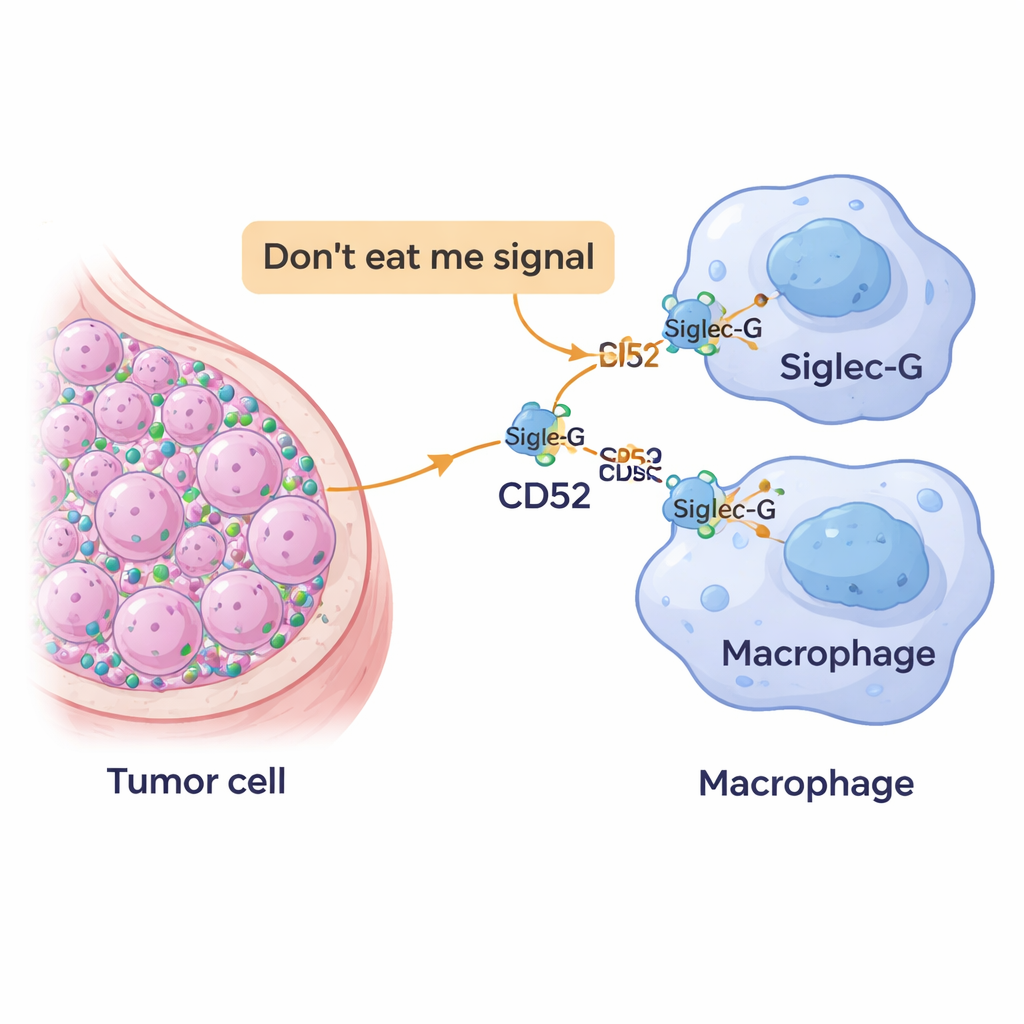
Eine neue "Nicht fressen"‑Marke auf Krebszellen
Unser Immunsystem verlässt sich auf Fresszellen, sogenannte Makrophagen, die Gewebe überwachen und gefährliche oder abnorme Zellen verschlingen. Um nicht fälschlicherweise zerstört zu werden, zeigen gesunde Zellen Oberflächenmarker, die im Grunde signalisieren: „Ich gehöre hierher.“ Krebszellen kapern dieses System oft, indem sie solche Schutzsignale übernutzen und daraus mächtige „Nicht fressen“‑Flaggen machen. Die Forschenden konzentrierten sich auf ein Molekül namens CD52, das bereits aus Blutkrebserkrankungen und Autoimmunerkrankungen bekannt ist, und fragten, ob Brusttumorzellen es ebenfalls nutzen, um dem Angriff der Makrophagen zu entgehen.
Nachweis von CD52 in aggressiven Brusttumoren
Das Team analysierte große öffentliche Krebsdatenbanken und Gewebeproben von Patientinnen. Sie fanden, dass Brusttumoren, insbesondere triple‑negative, mehr CD52 produzierten als normales Brustgewebe. Darüber hinaus waren Tumoren mit höherem CD52 tendenziell weniger gut differenziert, ein Merkmal, das oft mit aggressiverer Erkrankung einhergeht. Gleichzeitig trugen Immunzellen in und um die Tumoren hohe Mengen eines Partnermoleküls namens Siglec‑10 (und dessen Mäusependant Siglec‑G), das auf Makrophagen sitzt und beruhigende Signale in diesen Zellen auslösen kann. Zusammengenommen deuteten diese Befunde darauf hin, dass CD52 auf Tumorzellen direkt mit Siglec‑G auf Makrophagen kommunizieren könnte, um deren Aktivität zu dämpfen.
CD52 ausschalten, um Makrophagen zu befreien
Um diese Idee zu prüfen, verwendeten die Wissenschaftler Geneditierungstools, um CD52 aus mouse triple‑negativen Brustkrebszellen zu entfernen. Wenn diese veränderten Zellen im Labor mit Makrophagen gemischt wurden, verschlangen die Makrophagen deutlich mehr Tumorzellen als bei unveränderten Krebszellen. Wichtig ist, dass sich das Wachstum oder das Überleben der Krebszellen nach dem Verlust von CD52 nicht veränderte, was darauf hinweist, dass der entscheidende Effekt auf die Immunerkennung und nicht auf die Biologie der Tumorzellen selbst zurückzuführen war. Wurden dieselben Tumorzellen in Mäuse eingebracht, bildeten die ohne CD52 kleinere Tumoren und waren von Makrophagen umgeben, die stärker darauf hindeuteten, Krebszellen gefressen zu haben. Wenn Makrophagen aus den Mäusen entfernt wurden, verschwand dieser Wachstumsnachteil, was bestätigte, dass CD52 vor allem der Abschirmung der Tumoren gegen das Verschlingen diente.
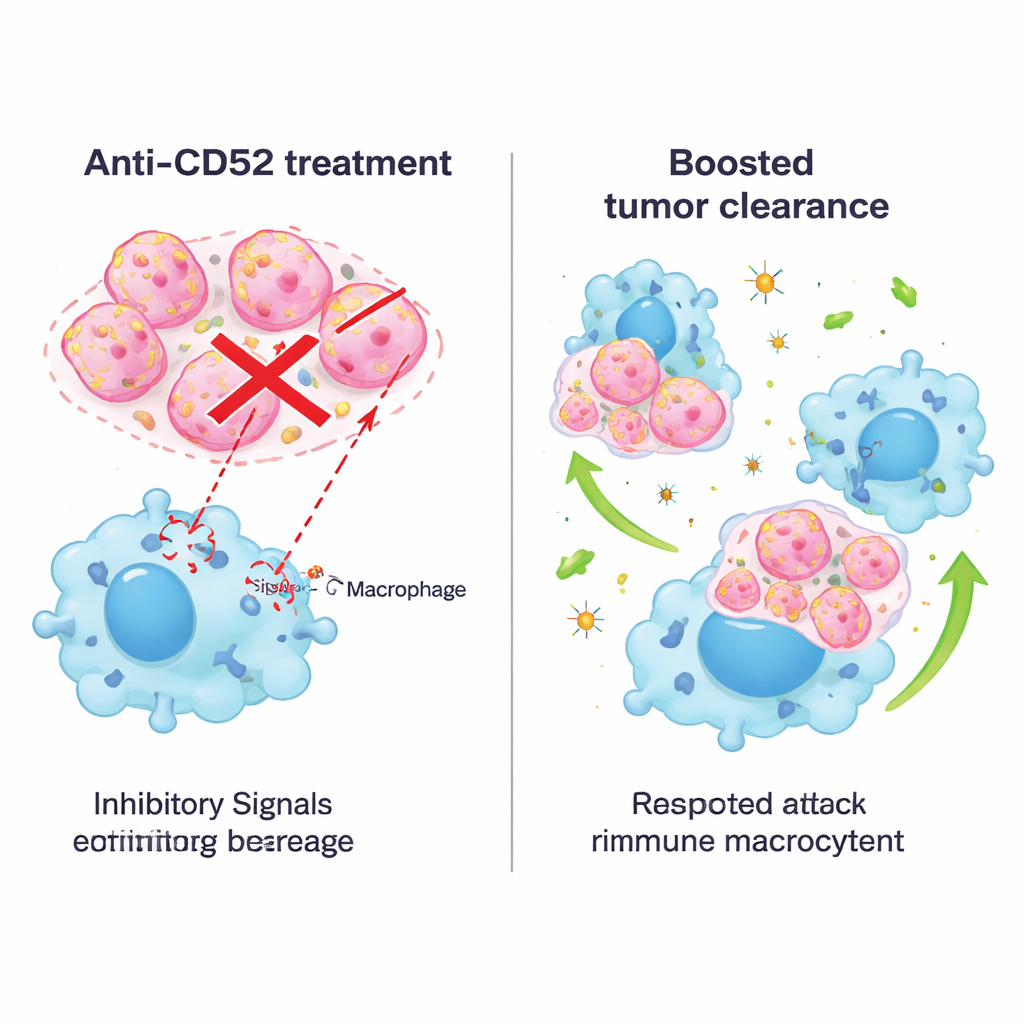
Das Signal mit Antikörpern blockieren und Behandlungen kombinieren
Da Medikamente, die CD52 anvisieren, bereits bei anderen Erkrankungen eingesetzt werden, testeten die Forschenden anschließend einen blockierenden Antikörper in Mausmodellen. Die Behandlung tumorbefallener Mäuse mit einem Anti‑CD52‑Antikörper verringerte das Tumorwachstum, verlängerte das Überleben und verursachte keine offensichtlichen Organschäden oder Gewichtsverluste. In Zellkulturen stärkten ähnliche Antikörper die Fähigkeit sowohl von Maus‑ als auch menschlichen Makrophagen, Brustkrebszellen verschiedener Subtypen zu verschlingen, nicht nur triple‑negative. Das Team kombinierte dann die CD52‑Blockade mit Anti‑PD‑1‑Therapie, einem weit verbreiteten Checkpoint‑Medikament, das auf T‑Zellen abzielt. In einem spontanen Mausmodell des triple‑negativen Brustkrebses funktionierte die Kombination besser als jede Einzeltherapie: Tumoren schrumpften stärker, Makrophagen wurden entzündlicher und aktiver, und mehr effektive krebsbekämpfende T‑Zellen drangen in den Tumor ein, während weniger erschöpfte T‑Zellen verblieben.
Was das für die zukünftige Brustkrebsversorgung bedeutet
Diese Arbeit enthüllt CD52 als bisher unerkannte „Nicht fressen“‑Signal, das triple‑negative Brustkrebszellen nutzen, um sich vor Makrophagen zu schützen. Indem die Kommunikation zwischen CD52 auf Tumorzellen und Siglec‑G auf Makrophagen unterbrochen wurde, gelang es den Forschenden, sowohl die angeborenen Immunzellen als auch indirekt T‑Zellen wieder zu aktivieren, insbesondere in Kombination mit einer PD‑1‑Blockade. Zwar sind weitere Sicherheits‑ und klinische Studien nötig — da CD52 auch auf vielen normalen Immunzellen vorkommt —, doch deuten die Befunde auf eine vielversprechende Dual‑Checkpoint‑Strategie hin, die schwer behandelbare, immunresistente Brusttumoren in solche verwandeln könnte, die besser auf Immuntherapie ansprechen.
Zitation: Qin, X., Chang, Y., Qiu, Y. et al. CD52 signaling via macrophage Siglec-G represents a therapeutic target for cancer immunotherapy. npj Breast Cancer 12, 29 (2026). https://doi.org/10.1038/s41523-026-00895-3
Schlüsselwörter: triple-negativer Brustkrebs, Makrophagen, Immuntherapie, CD52, Checkpoint-Blockade