Clear Sky Science · de
Gleichzeitige Abgabe des Chemokins CXCL9 und des kostimulatorischen Liganden TNFSF9 durch mesenchymale Stammzellen reprogrammiert das immunologische Mikroumfeld bei Triple-negativem Brustkrebs
Warum dieser neue Ansatz bei Brustkrebs wichtig ist
Triple-negativer Brustkrebs gehört zu den gefährlichsten Formen von Brustkrebs, weil er schnell wächst, früh metastasiert und die üblichen Hormonziele fehlt, auf die viele Medikamente abzielen. Die Immuntherapie weckt Hoffnungen, doch bei vielen Patientinnen dringen die Abwehrzellen nicht in ausreichender Zahl in den Tumor ein, um Wirkung zu zeigen. Diese Studie untersucht eine einfallsreiche Strategie: lebende Trägerzellen als gesteuerte „Lieferwagen“ zu verwenden, die immunstärkende Signale direkt in schwer zugängliche Tumore bringen und so potenziell mehr Patientinnen für wirkungsvolle immunbasierte Behandlungen zugänglich machen.
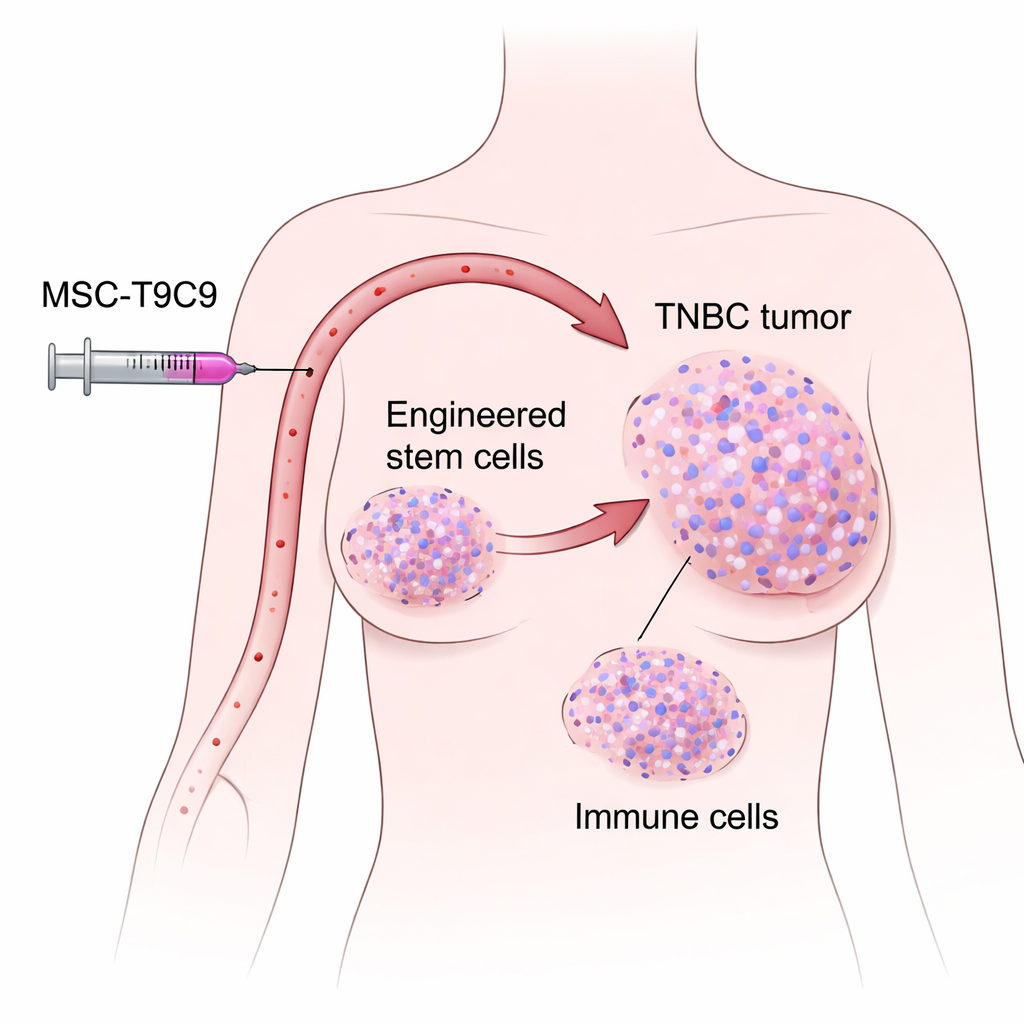
Ein hartnäckiger Krebs mit zu wenig immuner Unterstützung
Standardbehandlungen für triple-negativen Brustkrebs – Operation, Chemotherapie und Strahlung – verhindern oft kein Wiederauftreten, und das mittlere Überleben bei fortgeschrittener Erkrankung liegt weiterhin unter zwei Jahren. Ein wichtiger Grund ist, dass viele dieser Tumoren „kalt“ sind, also nur wenige krebsbekämpfende Immunzellen enthalten. Große Patientendatenbanken zeigten, dass Personen, deren Tumoren von Natur aus höhere Mengen zweier immunbezogener Moleküle, CXCL9 und TNFSF9, produzieren, tendenziell länger leben und mehr T‑Zellen sowie natürliche Killer‑(NK‑)Zellen in ihren Tumoren haben. CXCL9 ist ein chemisches Signal, das Immunzellen ins Gewebe lockt, während TNFSF9 wie ein zusätzlicher „Startschalter“ wirkt, der diesen Zellen stärkere Angriffsbereitschaft verleiht. Das Muster deutete darauf hin, dass die Erhöhung beider Signale direkt im Tumor das Gleichgewicht zugunsten des Immunsystems verschieben könnte.
Stammzellen zu intelligenten Lieferwagen machen
Die Forscher konzentrierten sich auf mesenchymale Stammzellen aus gespendeten menschlichen Nabelschnüren. Diese Zellen haben eine nützliche Eigenschaft: Werden sie Mäusen mit Brusttumoren in den Blutkreislauf injiziert, wandern sie natürlicherweise zu Tumorstellen und verweilen dort Tage lang, während sie normale Organe weitgehend meiden. Das Team gentechnisch so veränderte, dass die Stammzellen CXCL9 ausschütten und TNFSF9 an ihrer Oberfläche präsentieren, und schuf damit eine zweifach wirksame Zelltherapie, die sie MSC‑T9C9 nennen. Labortests zeigten, dass die modifizierten Zellen hohe Mengen CXCL9 abgaben und Mäuse‑T‑Zellen sowie NK‑Zellen stark aktivierten, ohne ihr eigenes Wachstum zu verändern oder selbst Tumore zu verursachen. Das machte sie zu vielversprechenden Kandidaten als gezielte Immunverstärker.
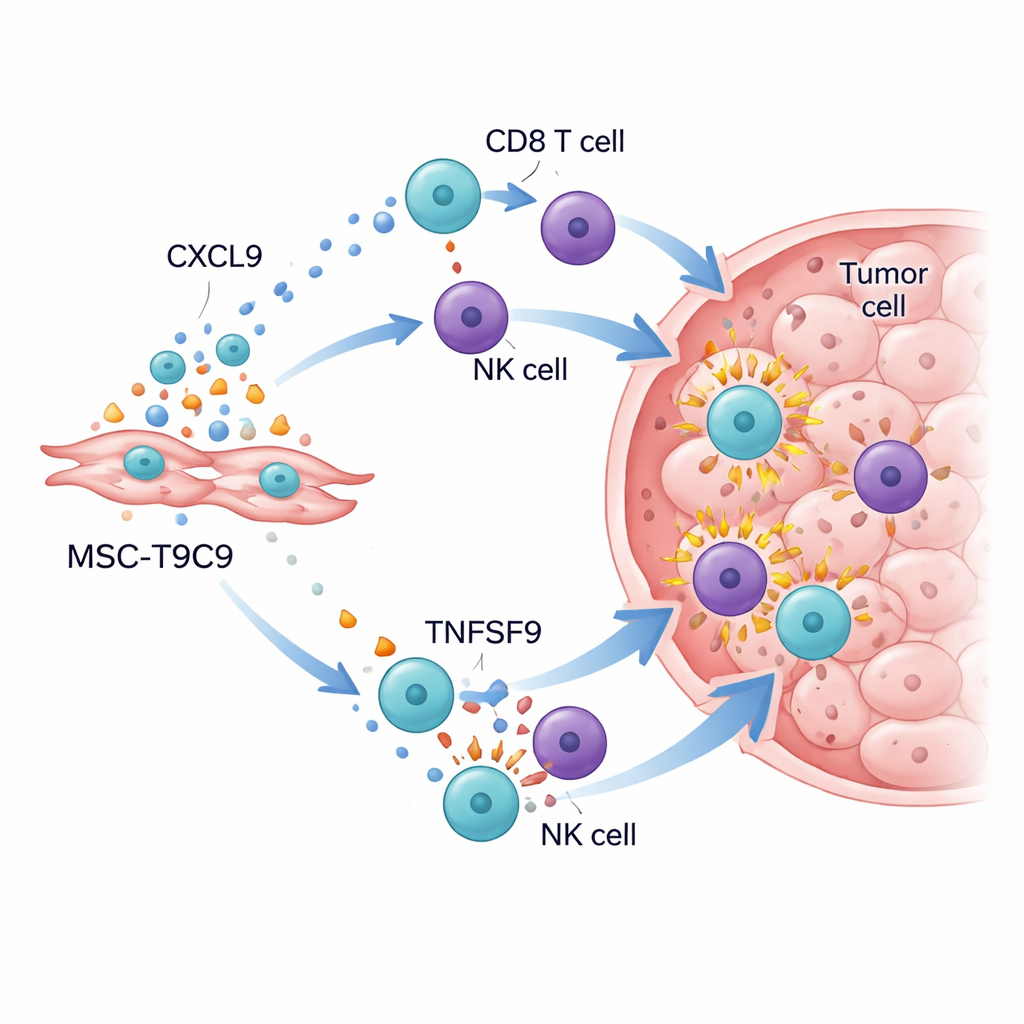
Das immunologische Schlachtfeld im Tumor wecken
Wurden die gentechnisch veränderten Zellen Mäusen mit triple-negativen Brusttumoren verabreicht, waren die Ergebnisse deutlich. Bei immunkompetenten Mäusen verlangsamten wiederholte Injektionen von MSC‑T9C9 das Tumorwachstum deutlich und erhöhten den Tumorzelluntergang, während Kontrollstammzellen kaum Wirkung zeigten. Detaillierte Analysen der Tumoren offenbarten einen dramatischen Anstieg der Zahl von CD8‑„Killer“‑T‑Zellen und NK‑Zellen sowie höhere Spiegel starker Angriffsmoleküle wie Granzyme B, Interferon‑γ, Tumornekrosefaktor‑α und Interleukin‑2. Gleichzeitig verschob sich das Tumormilieu weg von einem unterdrückenden Zustand: hilfreiche entzündliche Makrophagen nahmen zu, und obwohl regulatorische T‑Zellen weiterhin vorhanden waren, wurden sie von der neuen Kämpferwelle in den Hintergrund gedrängt. In immunsupprimierten Mäusen, denen T‑ und NK‑Zellen fehlen, verlangsamte MSC‑T9C9 das Tumorwachstum nicht, was bestätigt, dass der Nutzen von der Mobilisierung der körpereigenen Abwehr abhängt.
Tumore für Checkpoint‑Therapie vorbereiten
Moderne Immuntherapien wie Anti‑PD‑1‑Antikörper lösen molekulare „Bremsen“ an T‑Zellen, funktionieren aber am besten, wenn bereits genügend T‑Zellen im Tumor vorhanden sind. Die Studie fand, dass MSC‑T9C9 nicht nur mehr CD8‑T‑Zellen in die Tumoren zog, sondern diese auch in einen hochaktiven, jedoch bremsensensiblen Zustand versetzte, der durch den PD‑1‑Rezeptor gekennzeichnet ist. In einem Mausmodell führte die Kombination von MSC‑T9C9 mit einem Anti‑PD‑1‑Medikament zur stärksten Tumorverkleinerung und längsten Überlebenszeit im Vergleich zu jeder Behandlung allein. Analysen humaner Krebsdatensätze stützten diese Idee: Patientinnen mit höheren kombinierten Spiegeln von TNFSF9 und CXCL9 profitierten eher von Checkpoint‑Blocker‑Therapien, was dafür spricht, dass dieselbe Biologie auch beim Menschen gelten könnte.
Sicherheit und künftiges Potenzial
Jede Behandlung, die die Immunität steigert, wirft Bedenken hinsichtlich gefährlicher Nebenwirkungen wie weitreichender Entzündungen oder Organschäden auf. Erfreulicherweise zeigten Mäuse, die MSC‑T9C9 erhielten, normales Gewicht und normales Verhalten, keine offensichtlichen Verletzungen wichtiger Organe sowie unauffällige Blut‑ und Leber‑Nieren‑Laborwerte. Wichtig ist, dass der Anstieg der Immunaktivität weitgehend auf den Tumor beschränkt war und sich entzündliche Signale im Blut nicht erhöhten. Während vor Studien am Menschen noch weitere Arbeit nötig ist – einschließlich Tests in realitätsnäheren Modellen und einer sorgfältigen Dosisfindung – deutet diese Studie darauf hin, dass das gezielte Lenken gentechnisch veränderter Stammzellen zu Tumoren, um Immunzellen heranzurufen und zu aktivieren, einen zielgerichteten, potenziell sichereren Weg bieten könnte, „kalte“ triple‑negative Brustkrebse in „heiße“ Tumoren zu verwandeln, die besser auf Immuntherapien ansprechen.
Zitation: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Schlüsselwörter: triple-negativer Brustkrebs, Immuntherapie, mesenchymale Stammzellen, tumorales Mikroumfeld, Checkpoint‑Blockade