Clear Sky Science · de
Vom Wirt stammendes Interleukin-1α fördert Tumorimmununterdrückung durch Umprogrammierung tumornaher myeloider Zellen
Warum diese Forschung für Krebspatienten wichtig ist
Die Immuntherapie hat die Behandlung einiger Krebsarten revolutioniert, doch viele Brusttumoren entziehen sich weiterhin dem Immunsystem. Dieses Paper beleuchtet einen weniger bekannten Verursacher: ein Signalmolekül namens Interleukin‑1 alpha (IL‑1α), das nicht von den Krebszellen selbst, sondern von normalen Körperzellen gebildet wird. Die Autoren zeigen, dass vom Wirt stammendes IL‑1α Immunzellen still und leise zu Verbündeten des Tumors machen kann und dass die Blockade dieses Signals bei Mäusen dazu führen kann, dass Brusttumoren schrumpfen oder verschwinden. Das Verständnis dieses Schalters könnte Ärzten helfen, Therapien zu entwickeln, die die Wirksamkeit der Immuntherapie bei Brustkrebs verbessern.
Ein versteckter Einflussnehmer in der Tumornachbarschaft
Krebs wächst nicht isoliert; er lebt in einer belebten „Nachbarschaft“ aus Immunzellen, Blutgefäßen und Bindegewebe, bekannt als Tumormikroumgebung. Zu den wichtigsten Bewohnern gehören myeloide Zellen, besonders Makrophagen, die Tumoren entweder angreifen oder schützen können. Klassische Lehrbücher unterteilen Makrophagen in M1 (tumorbekämpfend) und M2 (tumorunterstützend), doch reale Tumoren enthalten viele Abstufungen dazwischen. Die Autoren konzentrierten sich auf IL‑1α, ein Molekül, das normalerweise von nicht‑karzinösen Geweben produziert wird, um zu untersuchen, ob dieses vom Wirt stammende Signal eintreffende myeloide Zellen in hilfreiche oder schädliche Rollen innerhalb von Brusttumoren steuert.
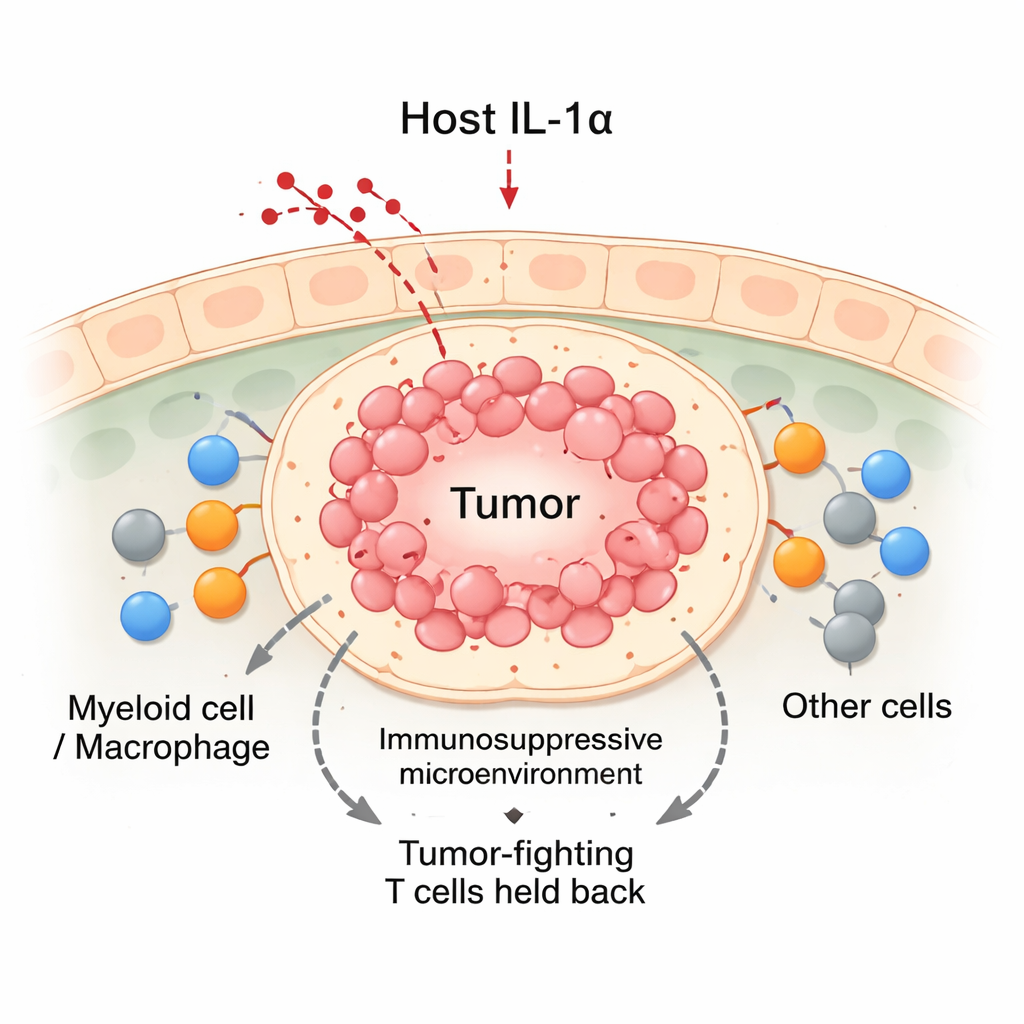
Das Abschalten von IL‑1α kippt die Balance zugunsten des Tumors
Mit Mausmodellen des Brustkrebses verglich das Team normale Tiere mit genetisch veränderten Mäusen, die kein IL‑1α produzieren. Wurden Brustkrebszellen in die Mammadrüsen transplantiert, wuchsen die Tumoren in normalen Mäusen kontinuierlich. Im Gegensatz dazu wuchsen Tumoren in IL‑1α‑defizienten Mäusen zunächst etwa zwei Wochen und regredierten dann häufig. Diese regressiven Tumoren enthielten insgesamt mehr Immunzellen, darunter einen starken Anstieg an CD8‑„Killer“‑T‑Zellen und myeloiden Zellen. Obwohl IL‑1α‑defiziente Mäuse weniger weiße Blutkörperchen im Blut hatten, sammelten sich deutlich mehr Immunzellen am Tumorort. Detaillierte Analysen zeigten, dass die infiltrierenden CD8‑T‑Zellen in IL‑1α‑defizienten Tumoren aktiver waren, höhere Mengen tumorabtötender Moleküle produzierten und weniger Erschöpfungsmerkmale zeigten.
Wie IL‑1α tumornahen myeloiden Zellen die Form gibt
Um zu verstehen, was IL‑1α auf zellulärer Ebene bewirkt, nutzten die Forscher Einzelzell‑RNA-Sequenzierung, um Tausende einzelner Zellen aus Tumoren zu untersuchen. Sie entdeckten, dass nur eine kleine Untergruppe tumornaher Makrophagen—gekennzeichnet durch einen Rezeptor namens CX3CR1—IL‑1α produzierte. In normalen Mäusen reiften viele eintreffende Monozyten zu diesen CX3CR1‑positiven Makrophagen heran, die mit immunsuppressivem Verhalten verknüpft waren. In Mäusen ohne IL‑1α war dieser Reifungsweg gestört. Stattdessen tendierten myeloide Zellen eher dazu, iNOS‑positive inflammatorische Makrophagen zu werden, ein Profil, das mit anti‑tumoraler Aktivität assoziiert ist. Funktionell waren myeloide Zellen aus IL‑1α‑defizienten Tumoren weniger fähig, Bremsen wie PD‑1 und CTLA‑4 auf T‑Zellen zu induzieren, und zeigten eine geringere Kapazität, die T‑Zell‑Proliferation zu dämpfen.
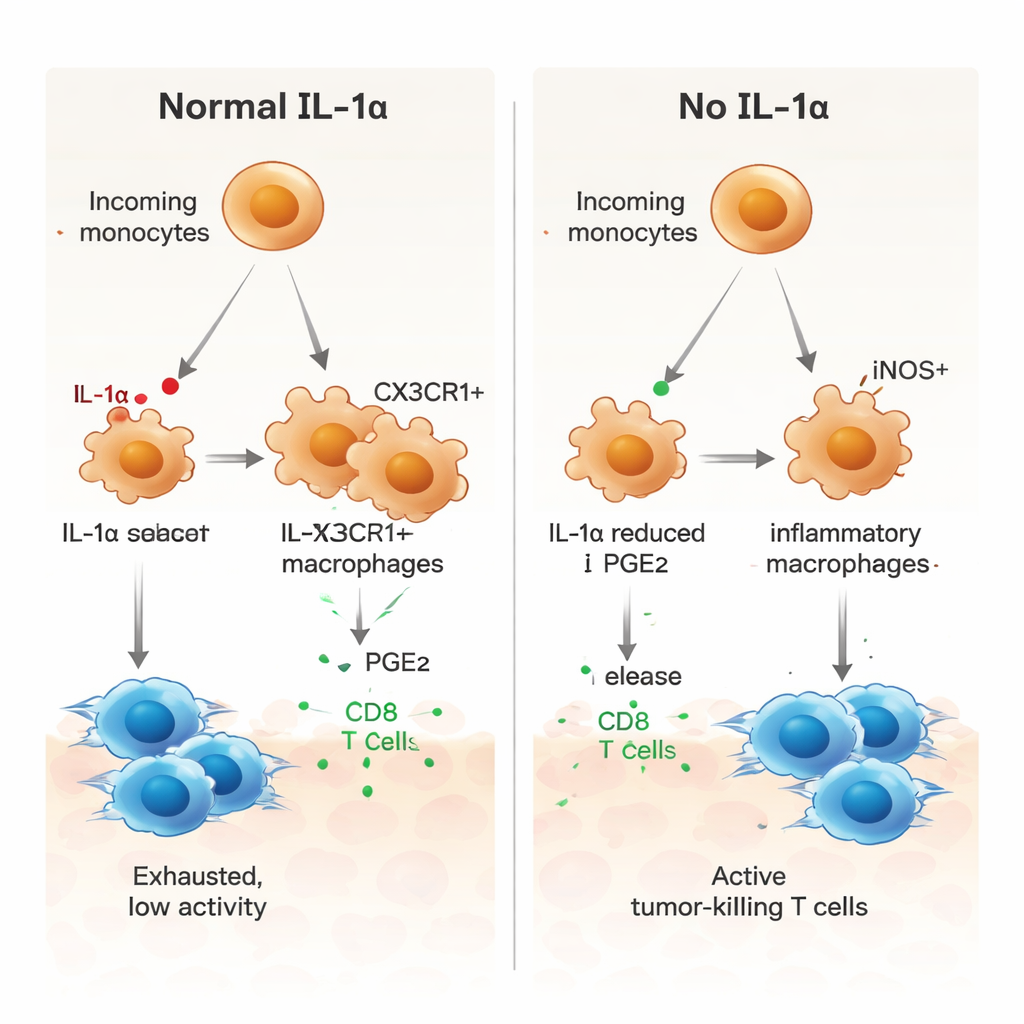
Eine Schlüsselrolle für einen Lipidbotenstoff, PGE2
Die Autoren fragten dann, wie IL‑1α myeloide Zellen in einen tumorfördernden Zustand treibt. Die Kommunikationsanalyse der Einzelzelldaten wies auf mehrere Signalwege hin, darunter einen mit Prostaglandin E2 (PGE2), einem Lipidmediator, der bekannt dafür ist, Immunsuppression zu fördern. In Tumoren ohne IL‑1α exprimierten Makrophagen geringere Mengen an Rezeptoren für makrophagen‑wachstumsfördernde Faktoren (M‑CSF), TGF‑β‑Rezeptoren und einen PGE2‑Rezeptor, und umliegende Stromazellen produzierten weniger der Enzyme, die PGE2 herstellen. In Labor‑Kulturen zeigten Knochenmark‑abgeleitete Makrophagen aus IL‑1α‑defizienten Mäusen ein stärker inflammatorisches Profil mit höherem iNOS und niedrigerem CX3CR1. Die Zugabe von PGE2 kehrte diese Verschiebung um und stellte ein stärker suppressives Muster wieder her, während die Blockade von PGE2 in normalen Makrophagen sie in Richtung eines pro‑inflammatorischen Zustands drängte. Makrophagen ohne IL‑1α stimulierten auch stärker die tumorspezifische CD8‑T‑Zell‑Proliferation—ein Effekt, der abgeschwächt wurde, wenn PGE2 wieder zugegeben wurde.
Die Übertragung von Mausbefunden auf die menschliche Immunität
Um zu prüfen, ob ihre Mausergebnisse der menschlichen Biologie entsprechen, verglich das Team Gen‑Signaturen der unterschiedlichen Maus‑Makrophagen‑Untergruppen mit einem großen Panel humaner myeloider Zellen, die im Labor in verschiedene Zustände getrieben worden waren. Makrophagencluster aus Tumoren normaler Mäuse ähnelten menschlichen Zellen, die durch Moleküle wie IL‑10, IL‑4 und Glukokortikoide in M2‑ähnliche, immundämpfende Zustände gedrängt wurden. Im Gegensatz dazu entsprachen die gleichen Cluster aus IL‑1α‑defizienten Tumoren menschlichen Zellen in stärker inflammatorischen, weniger suppressiven Zuständen. Bemerkenswert war, dass Genmuster, die mit PGE2‑Signalgebung verknüpft sind, in IL‑1α‑abhängigen Makrophagen angereichert waren, aber fehlten, wenn IL‑1α nicht vorhanden war—dies untermauert die Idee, dass IL‑1α und PGE2 zusammenarbeiten, um eine immunsuppressive Nische zu schaffen.
Was das für die zukünftige Brustkrebstherapie bedeuten könnte
Kurz gesagt deutet diese Studie darauf hin, dass ein vom Wirt stammendes Molekül, IL‑1α, bestimmte Makrophagen still dazu bringen kann, den Tumor zu schützen und Killer‑T‑Zellen in Schach zu halten, zum Teil über PGE2‑Signalgebung. Wird IL‑1α bei Mäusen entfernt, verschieben sich Makrophagen in einen entzündlicheren, tumorangreifenden Zustand, CD8‑T‑Zellen werden aktiver und transplantierte Brusttumoren werden häufig abgestoßen. Da aktuelle Immuntherapien bereits darauf abzielen, erschöpfte T‑Zellen wiederzubeleben, könnte die Kombination mit Ansätzen, die IL‑1α oder seinen nachgeschalteten PGE2‑Weg blockieren, die Tumormikroumgebung noch stärker zugunsten des Immunsystems des Patienten kippen. Zwar sind weitere Studien zur Prüfung von Sicherheit und Wirksamkeit beim Menschen nötig, doch heben diese Befunde IL‑1α als vielversprechendes neues Ziel hervor, um Brustkrebs gegenüber immunologischen Angriffen verwundbarer zu machen.
Zitation: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Schlüsselwörter: Immuntherapie bei Brustkrebs, Tumormikroumgebung, Makrophagen, Interleukin-1 alpha, Prostaglandin E2